Roberto Renzetti
NOTE BIOGRAFICHE ED OPERA DI JULIUS ROBERT VON MAYER
Mayer rappresenta l’inizio dell’emergere della scienza in Germania, Paese che in breve tempo diventerà una vera potenza scientifica. Qui siamo ancora con un approccio piuttosto isolato ed addirittura da parte di un appassionato di scienza ma poco preparato in matematica. Questo fatto condizionerà la conoscenza dei suoi lavori e la priorità sulla scoperta della conservazione dell’energia, almeno in un dato ambito (equivalenza lavoro e calore in ciclo chiuso).
Mayer nacque a Heilbronn (Baden-Württemberg) nel 1814 da famiglia borghese di un farmacista. Era un anno speciale perché Napoleone si ritirava dalla Russia e nei land tedeschi si svegliavano spiriti nazionalisti. Fece studi regolari prima al ginnasio della sua città quindi alla scuola superiore nel seminario della città di Schöntal ed infine iscrivendosi (1832) a medicina presso l’Università di Tubinga, dove si laureò nel 1838 (essendo stato sospeso per un anno per aver fatto parte di un’organizzazione fuorilegge). Dopo un soggiorno parigino ed in

Svizzera, presa l’abilitazione professionale a Stoccarda, si arruolò come medico nel servizio coloniale olandese. Nel 1840 si imbarcò sul trealberi mercantile Giava diretto a Batavia (l’odierna Giacarta), seguendo la pratica dei viaggi verso lontane terre che all’epoca vari studiosi facevano (il primo viaggio di Darwin sul Beagle fu realizzato tra il 1831 ed il 1836). Durante il lungo viaggio (più di tre mesi) si dedicò a leggere alcuni libri di fisica che però non lo convincevano riguardo ad alcune questioni che sembravano non rispettare la connessione causa – effetto. Ebbe anche modo di fare molte osservazioni su svariati fenomeni che andavano dalla temperatura più elevata dell’acqua del mare dopo una tempesta rispetto a quando era calmo, alla differente colorazione, più chiara, che assumeva il sangue dei passeggeri della nave appena giunti in quelle regioni tropicali. Riuscì ad interpretare quest’ultimo fenomeno con la teoria avanzata da Lavoisier sul calore animale che sarebbe originato da processi di combustione. Mayer ragionò nel modo seguente: per mantenere costante la temperatura corporea con una temperatura ambientale elevata, devono rallentare i processi di combustione che, tra l’altro, determinano la colorazione del sangue poiché in esso vi sarà maggiore quantità di ossigeno non bruciato. Voleva verificare la cosa e per farlo dovette porsi il problema se fare la misura con persone immobili (produzione propria di calore) o farla su persone sotto sforzo. Qui si pose un ulteriore problema perché il sotto sforzo vuol dire camminare, sollevare pesi, … Si tratta quindi di un calore meccanico che si aggiunge al calore proprio. IL corpo umano è quindi in grado, alimentandosi, di produrre sia calore che lavoro e, sempre nel corpo, l’uno si trasforma nell’altro, a seconda delle azioni che si fanno. Ciò lo portò a concludere, in un modo coraggioso tipico dei neofiti e degli outsider, che due entità così diverse come il lavoro meccanico ed il calore erano due aspetti della stessa realtà fisica, trasformabili l’uno nell’altro(1). Le sue riflessioni sulle mancanze di cause ed effetti, su cui si era soffermato quando veleggiava verso Giacarta, sembrarono chiarirsi. Ma c’è molto di più perché questa idea divenne per Mayer una sorta di religione alla quale dedicò l’intera vita, lavorando solo su di essa.

Nel 1841 egli tornò nella sua città dove andò maturando la sua idea ed elaborò la teoria dell’equivalenza tra calore prodotto e lavoro meccanico che lo produce. Fu a questo punto che venne fuori la sua impotenza nel descrivere ciò che aveva in mente in una forma accettabile da un pubblico di scienziati. Egli sapeva poco di fisica ed ancora meno di matematica. Scrisse una memoria, Erhaltungssatz der Kraft (Sulla determinazione della forza)(2),in cui vi erano molti errori anche elementari. Vediamo il principale. Quando aveva creato un parallelo tra nozione chimica di sostanza e nozione fisica di forza egli prese come effetto della forza non il lavoro ma il il movimento e misurò la forza mediante la quantità di moto mv . E continuò sulla strada dell’errore ragionando in termini di conservazione della quantità di morto nell’urto centrale non elastico tra due corpi con stessa massa e velocità. In questo fenomeno le quantità di moto di segno opposto, + mv e – mv, si annullano nell’urto e si sviluppa calore. Si può comprendere quanto occorresse studiare di fisica elementare per togliere di torno queste gravi lacune (ricompaiono le difficoltà che 150 anni prima erano state di Descartes e Leibniz. Quanto sostenuto da Descartes era errato perché non aveva una concezione vettoriale della quantità di moto. Infatti, la quantità di moto non può essere presa come misura della forza in quanto, con masse differenti, a dei lavori uguali non corrispondono delle quantità di moto uguali ma delle forze vive uguali ½mv2 ).
Inviò questo scritto ad una rivista di prestigio quale erano gli Annalen der Physik und der Chemie di J. C. Poggendorf che lo rifiutò e non rispose mai alle continue sollecitazioni di Mayer (alla morte di Poggendorf, il manoscritto fu trovato fra le carte del defunto).
Mayer comprese comunque di avere grosse lacune e si mise a studiare fisica e matematica con lezioni private di un professore di tale disciplina al Politecnico di Stoccarda, Carl Baur, mentre tentava altre vie di pubblicazione, sempre senza successo. In quel periodo iniziò una corrispondenza con Baur, divenuto suo amico, molto interessante per seguire gli sviluppi del suo pensiero. Mayer scriveva:
Il principio fondamentale della chimica è che la materia è indistruttibile e che gli elementi componenti ed i composti hanno tra loro dei rapporti definiti […]. Bisogna assolutamente applicare gli stessi principi alle forze; allo stesso modo della materia esse sono indistruttibili, si combinano le une con le altre, una perde la sua vecchia sembianza (diventa quantitativamente nulla) per riconquistarla sotto altra forma, ed i rapporti della sembianza primitiva con la forma acquistata sono essenziali … come nelle combinazioni chimiche. Le forze sono movimenti, elettricità e calore.
Queste dunque erano le idee di fondo dalle quali muoveva ma dall’ avere una tale concezione a tradurla in un linguaggio matematico la cosa risultava molto complessa, soprattutto a chi non conosceva né fisica né matematica. Dalle lettere si segue l’evoluzione del pensiero di Mayer. Ad un certo punto egli si propone di calcolare la relazione esistente tra forza e calore partendo dai fenomeni che sviluppano calore nei gas e, nel contempo, compare come effetto della forza, non più il movimento ma il lavoro fatto dalla forza di gravità ed espresso mediante il prodotto del peso di un corpo per l’altezza a cui si trova, anche se non ci fa capire come abbia abbandonato la relazione tra forza e quantità di moto. Più avanti, mostrando la frenesia che metteva nello studiarsi tutta la letteratura che potesse aiutarlo, egli parla delle esperienze di Gay-Lussac sullo sviluppo di calore per la compressione e dilatazione dell’aria. Forse questa strada può aiutarlo ma non sa come abbordarla dal punto di vista matematico e chiede aiuto al suo amico che volentieri glielo fornisce.
Philipp Johann Gustav von Jolly, un professore di matematica, fisica e tecnologia ad Heidelberg, lo convinse a riscrivere il tutto in forma più sintetica eliminando alcune parti (gli errori erano stati sistemati con Baur). In questa forma lo scritto, Bemerkungen über die Kräfte der unbelebten Natur (Osservazioni sulle forze della natura inanimata), fu accettato nel 1842 dai famosi chimici Justus von Liebig (1803 – 1873) e Friedrich Wöhler (1800 – 1882) per la rivista che dirigevano, gli Annalen der Chemie und Pharmacie. Ma il luogo di pubblicazione non intercettava chi avrebbe potuto cogliere il contributo ed elaborarlo, con l’aggravante che Liebig utilizzò alcune idee di Mayer senza citarlo. Fatto notevole di questo articolo è che in esso Mayer ricavava quello che oggi conosciamo come equivalente meccanico della caloria. Solo in epoca più tarda egli spiegherà in dettaglio il modo in cui aveva tratto le sue conclusioni.
Vediamo alcuni passi della sua prima memoria, osservando che in essa Mayer afferma che nella macchina a vapore non è la caduta di calorico che produce lavoro meccanico ma la trasformazione di calore in lavoro.. Egli inizia con il discutere la cosa che lo interessa di più, la forza, quasi per chiarire a se stesso il concetto.
Le forze sono cause: si può quindi applicare loro, in forma pIena, il principio secondo cui “causa aequat effectum”. […] In una catena di cause e effetti, un elemento o una parte di esso non può mai annullarsi, come risulta con chiarezza dalla natura stessa di una equazione. E chiameremo questa prima proprietà di tutte le cause la loro “indistruttibilità”.
E’ una sorta di programma dal sapore metafisico che prosegue per qualche pagina:
La capacità di assumere forme diverse costituisce la seconda proprietà essenziale di tutte le cause. Considerando insieme entrambe le proprietà è lecito affermare che le cause sono oggetti “indistruttibili” dal punto di vista quantitativo e reciprocamente trasformabili dal punto di vista qualitativo.
Mayer passa ad esemplificare qualche trasformazione di forze con la relativa indistruttibilità:
Le Forze, quindi, sono oggetti imponderabili indistruttibili e reciprocamente trasformabili. […] Una causa che genera l’innalzamento di un peso è una forza, e il suo effetto (il peso innalzato) è, conseguentemente, egualmente una forza. Si può esprimere questa relazione in una forma più generale, sostenendo che la separazione entro lo spazio di oggetti ponderabili è una forza: e poiché questa forza è causa della caduta dei corpi, la possiamo chiamare forza di caduta. La forza di caduta e la caduta stessa, oppure, in forma ancor più generale, la forza di caduta e il movimento, sono forze le quali sono l’una rispetto all’altra connesse come causa ed effetto, come forze che sono trasformabili l’una nell’altra, come due forme distinte di uno stesso oggetto unico.
Occorre ora passare ad introdurre il calore e Mayer lo fa attraverso il fenomeno d’attrito:
Quando, ad esempio, soffreghiamo a lungo e l’uno contro l’altro due dischi metallici, noi gradualmente causiamo la cessazione di una immensa quantità di movimento: ma potrà capitare di andar mai alla ricerca della più piccola traccia della forza che è scomparsa nelle polveri metalliche che potremmo raccogliere, per tentare di ricostituirla nuovamente? […] Senza il riconoscimento di una connessione causale tra movimento e calore, la difficoltà di spiegare la produzione di calore è pari a quella di fornire una qualche ragione per il movimento che scompare. [ … ]
Delineata la sua teoria Mayer passa a chiudere il suo lavoro con una domanda che porterà alla sua determinazione dell’equivalente meccanico della caloria. Egli scrive:
«Quanto è grande la quantità di calore che corrisponde ad una data quantità di movimento o di forza di caduta?». Ad esempio, dobbiamo accertare a quale altezza debba essere innalzato un dato peso rispetto al suolo, affinché la sua forza di caduta possa essere equivalente all’aumento di temperatura di un eguale peso d’acqua da 0° a 1°C. [ … ] Applicando, alle relazioni che esistono tra la temperatura e il volume dei gas, i principi che sono stati esposti troviamo che l’abbassamento di una colonna di mercurio che comprime un certo gas è equivalente alla quantità di calore liberata dalla compressione; ed allora, se si considera che il rapporto tra le capacità dell’aria per il calore a pressione costante e a volume costante è eguale a 1,421, segue che il riscaldamento di un dato peso d’acqua da 0° a 1°C corrisponde alla caduta di un eguale peso dall’altezza di circa 365 metri. Se confrontiamo questo risultato con l’operare delle nostre migliori macchine a vapore vediamo quanto sia piccola quella parte del calore applicato alla caldaia che viene realmente trasformata in movimento o in sollevamento di pesi; e tutto ciò può servire come una giustificazione dei tentativi di produrre movimento in modo più redditizio per mezzo di metodi diversi da quelli relativi alla dissipazione della differenza chimica che vi è tra il carbone e l’ossigeno – ovvero, più in particolare, per mezzo della trasformazione in movimento dell’elettricità ottenuta mediante mezzi chimici.
Come si può vedere in questa parte finale Mayer riprende le discussioni che erano state di Carnot e Clapeyron ed anche il valore 1,421 per il rapporto g tra i calori specifici a pressione costante Cp e a volume costante Cv (ricordo che il valore accettato all’epoca di Carnot era 1,44 mentre Carnot utilizzava 1,3748), uno dei punti delicati della teoria di Carnot e molto sofferto in quella di Clapeyron. Seguiamo lo schema di ragionamento fatto da Mayer servendoci di un linguaggio moderno.
Facciamo l’ipotesi che l’aria si comporti come un gas perfetto (buona approssimazione se si è in condizioni normali). Se consideriamo i valori di Cp e Cv per l’aria, scopriamo che il primo è maggiore del secondo perché quando si scalda l’aria essa si espande compiendo un lavoro P0.ΔV, dove P0 è la pressione prima dell’espansione e ΔV è l’aumento di volume. L’espansione (e quindi il lavoro meccanico) è originata dal calore che è stato fornito all’aria per riscaldarla. Visti i risultati di Gay-Lussac, si sa che l’aria non cambia di temperatura quando si espande nel vuoto senza fare lavoro. Possiamo allora scrivere:
Cp – Cv = P0.Δ V
e servirci del risultato sperimentale che, per la differenza tra i calori specifici suddetti, fornisce: 1,99 cal/(mol.C°). Utilizziamo ora l’equazione di stato dei gas ricavata da Clapeyron nel 1834 (sostituisco al 267 che utilizzava Clapeyron il 273 trovato più tardi e che discuterò diffusamente più oltre; inoltre assegno a t0 il valore di 0°C): P.V = PoVo /273.(t + 273) e il dato sperimentale or ora fornito. Variando la temperatura di 1 C° e mantenendo costante la pressione, come fa Mayer, si trova l’identità P0.DV = P0V0/273. Questa espressione si può calcolare utilizzando unità meccaniche sapendo che P0 = 1 atm e V0 = 22,421 litri (valore trovato da Avogadro nel 1820), si ha P0V0/273 = 8,31 joule/mol.C° (faccio notare che questa quantità è quella che noi oggi conosciamo come costante universale dei gas) da cui segue che una sola caloria vale 4,18 joule.
Poiché i dati sperimentali dell’epoca non erano accurati come quelli che usiamo oggi, il risultato travato da Mayer differisce da quello che ho ora fornito (tra l’altro, come evidente, egli usava unità di misura diverse). L’equivalente meccanico della caloria trovato da Mayer era di 3, 65 Kgm (leggi: chilogrammetri) mentre quello accettato oggi è si 4,78 Kgm.
L’anno 1842, in cui scriveva al suo amico fisico Griesinger: La forza di caduta, il movimento, il calore, la luce, l’elettricità e la differenza chimica tra i corpi ponderabili costituiscono un solo oggetto sotto apparenze diverse, fu un grande anno per Mayer. Fu promosso a ispettore chirurgo ed acquistò una clientela facoltosa; il suo amico Baur si trasferì a Heibronn; si sposò.
Ma Mayer lavorava con l’unico scopo della sua vita. Voleva tornare alla composizione originale delle sue idee che comprendevano non solo i corpi inanimati. Si mise quindi al lavoro con l’aiuto di amici fisici (Bauer e Griesinger) per la stesura di una pubblicazione che descrivesse con completezza le sue teorie trattando anche dei fenomeni organici che erano stati messi da parte, come consigliato da Jolly, nella prima pubblicazione. Il libro vide la luce ad Heilbronn nel 1845 con il titolo Die organische Bewegung im Zusammenhang mit dem Stoffwechsel (Sul moto del corpo in relazione al suo metabolismo). Le idee sostenute in questo lavoro prendono le mosse ancora dalle sue esperienze a Giacarta. Si sostiene l’impossibilità di creare qualcosa dal nulla o distruggere una qualunque cosa; a questa regola non sfuggono movimento e calore che non si possono creare o distruggere ma trasformarsi l’uno nell’altro. Si introducono alcune considerazioni nuove (la cosa gli era stata consigliata da Griesinger: introdurre sempre aspetti nuovi delle sue idee fondamentali e pubblicarle sotto forme diverse in modo che tali idee abbiano un impatto reale sul pubblico). Mayer fornisce il primo quadro sistematico delle energie note ed afferma che ogni energia messa in moto sulla Terra dagli esseri viventi proviene dai raggi solari che vengono immagazzinati dalle piante sotto forma di energia chimica. E’ un’importante estensione delle sue idee che sulla conservazione dell’energia ma è anche un delineare l’economia dell’energia della Terra. Nella seconda parte del libro, si fanno osservazioni molto dettagliate sulla fisiologia a partire dagli alimenti che forniscono l’energia chimica necessaria per ogni attività degli animali e dell’uomo. Mayer calcola il rapporto esistente tra lavoro meccanico fatto da uomini ed animali e il calore di combustione degli alimenti. Al fine di attirare l’attenzione sul suo lavoro montò una polemica garbata con Liebig ma il tentativo non ebbe successo.
Benché fosse molto abbattuto si mise di nuovo al lavoro per migliorare il suo lavoro, per perfezionarlo, per aggiungervi altri argomenti. In particolare un problema lo assillava: avendo individuato nel Sole l’origine delle energie animali, occorreva chiudere l’argomento con cosa fornisse energia al Sole per dare il suo calore alla Terra. Iniziò con il pensare a straordinarie energie cosmiche ma abbandonò subito l’idea. Si indirizzò allora sulle energie cinetiche delle masse che costituiscono il cosmo, energie che in qualche modo il Sole raccoglieva. Si servì anche di una formula che fornisce la velocità che possiede un corpo che cade dall’infinito verso un corpo che lo attrae ma se così fosse stato, allora la Terra avrebbe dovuto perdere la sua energia cinetica diminuendo continuamente la sua velocità intorno al Sole. Non credo sia il caso di andare oltre perché non esce nulla di buono da questi discorsi che mostrano una grande fantasia, un impegno ammirevole ma che non potevano sfociare in nulla. Queste lavoro fu pubblicato ad Heilbronn nel 1848 sotto il titolo Beiträge zur Dynamik des Himmels in populärer Durstellung (Contributo alla dinamica del cielo in forma popolare), proprio nell’anno in cui si ebbe una ventata rivoluzionaria che lo spaventò (egli era un conservatore) ed in cui si aprì la polemica con Joule sulla priorità della scoperta dell’equivalenza tra calore e lavoro, come vedremo più avanti. Qui basti dire che la polemica fu durissima soprattutto perché, anche in Germania, pochissimi conoscevano i suoi lavori, misconosciuti a maggior ragione all’estero. Nessuno quindi, se ci riferiamo a presone di prestigio, assunse le sue difese. Attacchi durissimi vennero anche dalla stampa dove un tal dottor Otto Seyffer lo insultò affermando che le cose che aveva scritto erano solo parole parole non sostenute da esperienze condotte con i metodi classici della fisica. Sull’Augsburger Allgemeinen Zeitung, arrivò ad affermare che il vero fisico era Faraday mentre lui non era altro che un fantasista. A Mayer non fu data la possibilità di rispondere su quel giornale (scrisse lettere e fece personali appelli all’editore ma invano) e questo avvenimento lo abbatté profondamente anche perché nella sua piccola Heilbronn iniziarono a considerarlo un megalomane che si attribuiva meriti altrui, ma non lo fece rinunciare. Si mise a lavorare con lena ancora intorno alle sue idee perfezionandole e chiarendole al massimo grado fino a presentarle in una forma classica priva di ogni possibile difetto. Il lavoro fu pubblicato nel 1851 ad Heilbronn con il titolo Bemerkungen uber das mecanische Aequivalent der Wärme (Osservazioni sull’Equivalente meccanico del Calore).

La fatica e l’angoscia iniziarono a farsi sentire minando il fisico di Mayer. Iniziò ad avere disturbi nervosi e psichici. Fonti biografiche dell’epoca parlano di infiammazione cerebrale. Nel maggio 1850, in un attacco di delirio, si gettò dalla finestra riportando fratture, traumi e ferite che lo resero claudicante per il resto della sua vita. Restò per mesi a letto poi, pano piano, riprese il suo lavoro di medico. Ma i postumi furono durissimi e passarono anche attraverso una sua patologica esaltazione religiosa. La sua infiammazione si aggravò (1851) fino al punto da farlo internare in un manicomio per quasi due anni. Quando ne uscì, nel 1853, non era più lo stesso. Dovette rinunciare al suo impiego pubblico e perse gran parte della sua clientela privata. Si può dire che Mayer andò in miseria. E neanche a dire che la moglie lo aiutasse. Sembra che non abbia fatto nulla per lenire almeno la malattia.
Per molto tempo non si parlò più di Mayer. Solo Liebig, in un discorso tenuto a Monaco nel 1858 menzionò la scoperta di Mayer come fondamentale aggiungendo che l’autore della scoperta era morto in una casa di salute.
Il riconoscimento ufficiale dei suoi meriti non venne dalla Germania ma dalla Gran Bretagna, la patria di Joule, dove, nel 1862, il fisico irlandese John Tyndall (1820 – 1893), successore di Faraday alla Royal Institution, sollevando molte polemiche nel suo Paese, assegnò la priorità della scoperta dell’equivalenza calore-lavoro a Mayer. In Germania, Helmholtz lo trattò per anni con disprezzo, e pur avendogli tributato onori nel congresso dei naturalisti tedeschi ad Innsbruck (1869), attaccò Eugen Dühring Dühring (il filosofo ed economista contro il quale Friedrich Engels scrisse l’ Anti-Dühring: Herr Eugen Dühring’s Revolution in Science, ovvero: Anti-Dühring: la scienza sovvertita del sig. Eugen Dühring, 1878)che nella sua Kritische Geschichte der allgemeinen Principien der Mechanik (Storia critica dei Principi della Meccanica, 1872) aveva riconosciuto meriti e priorità di Mayer. In altro scritto, Robert Mayer der Galilei des neunzehnten Jahrhunderts, I-II, 1878-1895, Dühring definì Mayer il Galileo del XIX secolo. Helmholtz sosteneva che le belle idee possono essere di chiunque, e Mayer ebbe belle idee, ma poi sostenerle con prove è altra cosa.
Mayer, che rifiutò la teoria di Darwin per motivi religiosi, passò il resto della sua vita scrivendo articoli di poca importanza e con ulteriori polemiche. Si spense a Heilbronn nel 1878.
ALCUNE NOTE STORICO-FILOSOFICHE
Prima però di passare ad altro autore, conviene accennare ad alcuni rivolgimenti di natura filosofica, ma anche ad avvenimenti economico-politici, che si produssero in Germania a partire dalla fine del Settecento, fino a buona parte dell’Ottocento. Credo che ciò serva a chiarire alcune difficoltà, oltre a quelle oggettive discusse, di carattere più generale che non erano solo di Mayer ma di molti scienziati e filosofi del suo tempo: quelle legate alla comprensione dell’esatta natura, non solo in termini fisici, della forza.
In questo periodo, in Germania, si ebbe un notevolissimo risveglio della vita culturale in netto contrasto con l’arretratezza di fondo delle strutture economiche, politiche e sociali. Siamo alla fine del XVIII secolo che vede l’emergere di questo Paese che va, via via, a collocarsi al centro del pensiero filosofico europeo. Il primo movimento di rottura con il pur evanescente Illuminismo tedesco è quello dello Sturm und Drang. Gli appartenenti ad esso (gli sturmer) ebbero molto in comune con gli illuministi, soprattutto divisero con loro la dura condanna per l’ancien regime, l’interesse per la natura e lo spirito laico; nel contempo, però, si distaccarono radicalmente da essi nel sostituire la categoria del genio a quella della razionalità. Ma l’autentico superamento dell’Illuminismo tedesco sarà rappresentato dal criticismo kantiano. Kant, che si muoveva all’interno dell’Illuminismo (essendone un appassionato difensore), si impadronì delle esigenze di razionalità di esso, studiò i fondamenti di tali esigenze ed arrivò a scoprirne i limiti. Sulla strada aperta da Kant iniziò a muoversi J.G. Fichte (1762- 1814) che ben presto si distaccherà dal maestro per imboccare la strada della filosofia idealista che in poco tempo si imporrà a tutta la Germania. Non è certo questa la sede per indagare la complessità, e l’eterogeneità del pensiero tedesco, delle posizioni assunte, dei temi affrontati e degli sviluppi che, in sede speculativa, ne conseguirono. Basti solo dire che i principali indirizzi di pensiero assunsero caratteristiche sempre più antilluministiche e nazionalistiche. E se da una parte Fichte, facendo confluire il suo idealismo nei temi più spiccatamente romantici, si rivolgerà. alla nazione tedesca perché insorgesse contro le truppe napoleoniche che invadevano la Germania, dall’altra il barbaro Hegel (1770 – 1831) pretenderà, di determinare le leggi della natura a priori, ricavandole semplicemente su basi metafisiche. A lato di ciò, negli spiriti migliori i temi romantici si legavano alle legittime aspirazioni di libertà, ed indipendenza dei popoli. La Germania era un paese diviso in una miriade di piccoli Stati. Ma già nei primi decenni del secolo si faceva avanti la Prussia, il più industrializzato tra gli Stati tedeschi, come polo di aggregazione. Della complicata storia della nascita dello stato tedesco (un’unione doganale si ebbe nel 1832 e l’unità dello Stato nel 1870), elemento importante fu la fondazione (da parte dell’ imperatore Federico Guglielmo III) dell’ Università di Berlino (1810). Questa Università, insieme all’ attività dei filosofi della natura che si ispiravano direttamente alla Naturphilosophie di Schelling fu alla base della rinascita culturale della Germania e della successiva acquisizione da parte di questo Paese del primato scientifico su tutto il mondo. Fu proprio Oken, uno dei filosofi della natura, che fondò nel 1822 la prima società scientifica che rappresentò la rinascita della ricerca tedesca, su basi più empiriche e sperimentali di quanto fino allora aveva comportato l’eredità di Leibniz. Sulla strada da lui aperta altri si mossero e ben presto, ad imitazione della Francia, sorsero una miriade di scuole politecniche. Cattedre di scienze cominciarono a venir istituite in tutte le università tedesche e, a partire dalla metà del secolo, le scuole sia industriali che commerciali iniziarono a sfornare una gran quantità di tecnici altamente specializzati. E tutto ciò era proprio finalizzato allo sviluppo dell’ industrializzazione del Paese che, al contrario di quanto avvenuto in Gran Bretagna, non fu promossa da privati ma per diretta iniziativa dello Stato che contemporaneamente, mediante lo sviluppo massiccio dell’ istruzione pubblica, cercava da un lato “di elevare il livello culturale del popolo per incrementarne i bisogni materiali e spirituali e per portare il semplice operaio a comprendere i nuovi sistemi di produzione meccanizzati; d’altro lato di formare una categoria di tecnici in grado di soddisfare le maggiori esigenze tecniche e scientifiche poste dall’ industria” [Klemm]. In questa dialettica tra Stato, imprenditori privati, popolo, sviluppo industriale ed istruzione, via via si realizzò una maggiore partecipazione della borghesia industriale alle scelte politiche del paese e conseguentemente si conquistarono importanti riforme costituzionali. In definitiva, intorno alla metà dell’ ‘800, è la borghesia industriale che detiene ovunque il potere economico. La pressione di questa borghesia per avere in mano anche il potere politico porterà alle vicende del ’48 che sancirono, praticamente ovunque, il suo trionfo. Con il terreno preparato per il decollo della seconda Rivoluzione Industriale si erano creati profondi cambiamenti economici e sociali che se da una parte avevano definitivamente affrancato l’Europa dall’ Ancien Régime, dall’altro avevano creato i presupposti per l’emergere di una nuova classe sociale: il proletariato, l’esercito degli operai dell’industria che dispongono solo della propria forza lavoro. L’affermazione della borghesia aveva creato la sua classe antagonista che, proprio a partire dal ’48, dette vita a tutti quei moti di ribellione sociale per migliori condizioni di vita che schematicamente si possono riportare alla nascita del socialismo scientifico di Marx (1818-1883) ed Engels (1820-1895).
Da un punto di vista più strettamente filosofico, I. Kant (1724 – 1804), profondo conoscitore di Newton, nella sua Allgemeine Naturgeschichte und Theorie des Himmels (Storia naturale generale e teoria del cielo, 1755), partendo da una critica generale della conoscenza ed in particolare dei principi del meccanicismo fece avanzare notevolmente il «sistema del mondo» ideato da Newton escludendo il concetto di Dio dalla spiegazione dei fatti naturali che appunto, secondo Kant, si possono spiegare mediante leggi generali che la natura stessa suggerisce: il mondo non è stato creato da Dio così come è, esso ha avuto origine dal moto vorticoso di una nebulosa (la stessa ipotesi verrà ripresa e sviluppata da Laplace nel 1796 nella Exposition du système du monde). Il concetto di vortice usato da Kant si lega però piuttosto a Newton che non a Descartes in quanto in questo vortice egli fa intervenire delle forze attrattive e repulsive alla base, secondo lui, della costituzione della materia. Le speculazioni di Kant sui problemi delle scienze della natura in questo periodo precritico (quando ancora la lettura di Hume non aveva scosso in Kant la fiducia nella validità delle scienze fisico-matematiche) furono sviluppate, modificate ed ampliate nei suoi Metaphysische Anfangsgründe der Naturwissenschaft (Primi principi metafici della scienza della natura, 1786) quando egli aveva già scritto il corpo principale dei suoi lavori filosofici (Kritik der reinen Vernunft, Critica della ragion pura, 1781). Kant criticò i concetti di «forza d’inerzia», di «spazio assoluto», di «vuoto assoluto» e di «impenetrabilità della materia». Secondo Kant quindi non vi possono essere atomi e non vi può essere vuoto: egli suppone che la materia sia composta da corpuscoli, che non sono solidi, che risultano indefinitamente divisibili e che si trovano immersi in una sostanza che riempie tutto lo spazio e che ha una densità di gran lunga più piccola di qualunque materia esistente (l’etere). Questa materia è soggetta all’azione di due forze (dinamismo): quella attrattiva (di tipo newtoniano) e quella repulsiva che è molto più intensa dell’altra. Queste due forze producono poi, sempre secondo Kant, diverse altre forze come ad esempio: «la forza calorica» che è alla base della concezione del calore e di tutti i fenomeni che derivano dal fuoco; «la forza luminosa» che è alla base della luce e di tutti i fenomeni dipendenti da essa; «la forza elettrica» che è la causa di tutti i fenomeni elettrici; «la forza magnetica che origina tutti i fenomeni magnetici» ed anche la «forza vitale», chiamata da Blumenback «vita propria», si origina secondo Kant come modificazione delle forze attrattive e repulsive. Per Kant non esistono quindi né fluidi elettrici, né calorici, né di altro tipo, ma forze di vario genere, intese tutte come modificazioni di quelle attrattive e repulsive, che agendo tra le particelle di materia, originano i diversi fenomeni. La «critica generale della conoscenza » di Kant ebbe, nella seconda metà del XVIII secolo, una notevole influenza sulla scienza, influenza che durò per molti anni, almeno fino agli inizi del XX secolo. Così, a cavallo tra la fine del XVIII e gli inizi del XIX secolo, mentre in Francia l’influsso del pensiero illuminista produceva un ambiente scientifico tale da formare degli scienziati che domineranno con le loro scoperte l’Europa intera, in Germania le speculazioni di Kant daranno l’avvio al movimento della Naturphilosophie che, se da una parte rappresenterà un freno all’affermarsi e all’evolversi della scienza, dall’altra porrà i germi per i grandi sviluppi della scienza tedesca della seconda metà del XIX secolo. Il più autorevole pensatore della Naturphilosophie fu certamenteFriedrich Wilhelm Joseph vonSchelling (1775 – 1854) le cui radici di pensiero si possono ritrovare nei lavori di Leibniz (1646 – 1716) di Boscovich e, appunto, di Kant.
Secondo Schelling il meccanicismo fisico non rende ragione dell’esistenza della natura. La concezione meccanicista di materia come un qualcosa di inerte fino a che su di essa non agiscono forze, entità diverse e separate dalla materia è, secondo Schelling, l’ammissione di una discontinuità tra materia e spirito (tra natura e uomo) che non corrisponde alla unità originaria di queste due entità, per esempio, nell’organismo vivente. Schelling, nelle sue Ideen zu einer Philosophie der Natur (Idee per una filosofia della natura, 1797), Von der Weltseele (Sull’anima del mondo, 1798), Erster Entwurf eines Systems der Naturphilosophie (Primo abbozzo di un sistema della Filosofia della Natura, 1799), sosteneva che è lo spirito (le forze) che si organizza in materia e pone quindi le forze, agenti tra punti inestesi, con i loro “conflitti e trasformazioni” alla base dell’esistenza del mondo (dinamismo fisico). Non c’è più materia allora ma c’è una particolare modificazione di una determinata zona dello spazio dovuta appunto ai conflitti ed alle trasformazioni delle forze (spirito) eterne e preesistenti ma anche convertibili le une nelle altre. In definitiva si affermava che tutto lo spazio fosse riempito da forze in permanente conflitto e trasformazione; si credeva che calore, luce, elettricità e magnetismo fossero particolari manifestazioni di queste forze; si vedeva l’origine dei fenomeni sensibili dalla unità di natura e spirito in un «assoluto» metafisico. La natura è quindi unitaria ma dinamicamente poiché è in un mutamento continuo regolato dalle trasformazioni delle forze. I seguaci della Naturphilosophie, che detto di passaggio dominarono negli insegnamenti universitari tedeschi nel primo terzo del XIX secolo, cercarono costantemente un principio che unificasse tutti i fenomeni naturali. Lo stesso Schelling scriveva: I fenomeni magnetici, elettrici, chimici, ed addirittura quelli organici dovrebbero essere interconnessi formando una grande unità […] che comprende tutto il mondo naturale. […] Non c’è dubbio che una sola forza, nelle sue varie forme, si manifesta nella luce, nell’elettricità e così di seguito. [Citato da Kuhn]
Questo rifiuto netto del meccanicismo, e più in generale del metodo scientifico, non nasce casualmente in questo periodo. La paura dell’affermazione di nuove classi sociali portava al rifiuto delle idee che avevano prodotto la Rivoluzione Francese, inoltre l’Illuminismo non era stato introdotto in Europa da Voltaire, Diderot (1713 – 1784) o altri pensatori, ma dagli eserciti di Napoleone a cui spontaneamente si opponevano i nazionalismi dei popoli che allora non potevano far altro che riconoscersi per una ricerca di unità, nei loro regnanti.
Si tenga conto che elementi non immediatamente riconducibili al meccanicismo fisico nascevano senz’altro dalla spiegazione dei processi biologici che i newtoniani insistevano a voler ricondurre ad esso (Goethe, nel suo saggio Zur Farbenlehre o Teoria dei colori del1810, bollò questa pretesa come inaccettabile). Inoltre le scoperte di quegli anni del galvanismo (1789) e della pila di Volta (1800), che il meccanicismo non aveva ancora spiegato esaurientemente, avevano aperto campi di indagine e di polemica in cui si inserirono efficacemente le speculazioni romantiche nella loro offensiva generale contro il meccanicismo.
Torno ora a Mayer, ma il discorso può applicarsi a molti altri scienziati dell’epoca soprattutto tedeschi ma anche inglesi (Faraday), per dire che questo clima, questa atmosfera culturale, questa filosofia, non gli erano certamente estranei. Se si confrontano le cose che ho detto di Schelling con le elaborazioni di Mayer si scopre che vi sono assonanze molto importanti così come si trovano in altri scienziati dell’epoca che addirittura affrontarono ricerche naturali con il preconcetto di conflitti di forze. Credo si possa dire, con Kuhn, che la Naturphilosophie può essere stata un importante precedente filosofico per la scoperta della conservazione dell’energia. Inoltre vari precursori di tale conservazione ebbero conoscenza quantomeno dei suoi concetti base (Liebig studiò due anni con Shelling e Mayer ebbe vari amici aderenti a quel movimento; il padre di Helmholtz fu un Naturphilosoph; …).
NOTE BIOGRAFICHE ED OPERA DI JAMES PRESCOTT JOULE
James Prescott Joule nacque alla vigilia di Natale del 1818 a Salford, paesino vicino a Manchester, in una regione molto ricca dell’Inghilterra, dalla famiglia di un ricco industriale della birra, Benjamin Joule. A proposito del clima che si respirava in quella regione e che interessa cogliere per capire meglio come si formò il carattere di Jouile, commenta il giornalista scientifico Crowther: Manchester era uno dei centri dell’industrialismo selvaggio fondato sull’applicazione alla manifattura della macchina a vapore. E’ possibile che le attività più sottili dell’intelletto umano potevano essere represse dalla brutale lotta per accumulare ricchezza, che accompagnò lo sviluppo della produzione industriale mediante applicazioni della fisica. James era il quarto di 7 figli e pativa, come il resto della famiglia di una non florida salute. Sua madre morì nel 1834 all’età di 48 anni e suo padre fu invalido per gli ultimi nove anni di vita. I suoi primi due fratelli morirono in tenera età; suo fratello maggiore era Benjamin nato un anno prima; la sorella Alice, che nacque dopo di lui, morì a 14 anni; poi vi erano un’altra sorella, Mary, nata nel 1823, ed un fratello, John, nato nel 1824 e morto all’età di 45 anni. Per parte sua James aveva una deformità fisica, generata da un malanno alla colonna vertebrale, che comunque non gli impedì di fare dello sport (cavalcare, remare scalare). Durante gli ultimi 25 anni della sua vita soffrì probabilmente di emofilia per le continue emorragie nasali che lo tormentavano. Dico tutto questo perché tali vicende condizionarono molto il carattere di Joule che fu chiuso e poco comunicativo. Lo condizionarono inoltre nella vita politica (era un conservatore) e nel fanatico attaccamento alla religione.

Un documento della birreria Joule del 1654. Tratto da: http://www.breweryhistory.com/journal/archive/115/bh-115-002.html
James e suo fratello Benjamin non ebbero un’istruzione regolare ma ricevettero lezioni domestiche, prima dalla sorellastra della madre e poi da diversi tutori, fino all’età di 16 anni. A partire dal 1834 fino al 1837 il padre li inviò a studiare dal famoso chimico John Dalton, il creatore della teoria atomica nella chimica che, nonostante avesse 68 anni, era ancora costretto a dare lezioni private per sostenersi. Dalton era il Presidente della Manchester Literary and Philosophical Society e probabilmente era stato scelto, oltre che per la sua fama, anche proprio perché era un chimico. Il padre dei due pensava più a dotare i suoi figli ad una preparazione scientifica immediatamente utilizzabile nell’industria che non a dargli una preparazione scientifica equilibrata. E la chimica avrebbe fornito conoscenze fondamentali ed indispensabili per chi, presumibilmente, avrebbe dovuto in futuro prendere le redini della fabbrica di birra. In tale attività si richiedono buone cognizioni di chimica e fisica dei gas e dei liquidi; occorre conoscere i problemi batteriologici della fermentazione; serve avere nozioni di quell’ingegneria che permetta manovrare e far funzionare pompe in grado di muovere grandi quantità di liquidi e gas di diverse temperature. Dalton sembrava la persona adeguata per fornire le basi a tale preparazione. E il grande chimico era anche una persona cosciente ed onesta perché rimandò le sue lezioni di chimica a momenti successivi, quando i due ragazzi avessero imparato l’aritmetica, l’algebra e la geometria del primo libro di Euclide da un qualche tutore (sarà Tapperden che gli darà due ore di lezione a settimana). Ma questo studio non piaceva ai due giovanetti. Avevano interessi pratici e la matematica è faticosa e richiede capacità astrattive che probabilmente ancora non erano maturate. Fin da piccoli i due erano soliti andare su una collina vicino casa per ammirare il passaggio dei treni della prima ferrovia inglese, la Liverpool-Manchester. Avevano una grande ammirazione per le macchine che la società industriale metteva in mostra. Loro ne avevano in fabbrica dove andavano, anche lì, per curiosare e, a partire dai 15 anni, per iniziare a prendere contatto con il loro futuro lavoro. Probabilmente qui iniziarono le sue curiosità su temperature e pressioni di gas all’interno di riscaldatori e di pompe. Ma altre erano le loro curiosità. Fin da bambini si erano costruiti un apparato (una bottiglia di Leyda) che dava scariche elettriche per fare scherzi ad amici e servitù. Realizzarono anche un aquilone, come quello di Franklin, per catturare i fulmini ed anche loro, come Franklin, rischiarono la folgorazione.

Una pubblicità della birreria Joule. Un gallone di birra a bassa gradazione viene offerta ad uno scellino circa. Tratta da: http://www.breweryhistory.com/journal/archive/115/bh-115-002.html
A questi giovani non piaceva la matematica, erano più interessati alla pura empiria. Tornati da Dalton dopo aver esaurito quanto gli era stato richiesto come conoscenza preliminare, Dalton richiese loro anche un poco di conoscenza di matematica superiore. Qui i due rifiutarono perché la loro posizione economica glielo permetteva (in questa epoca, per acquistare un quadro che gli piaceva, Joule sborsò di tasca sua 50 sterline, l’equivalente del salario annuale di un operaio specializzato). Ma intanto erano passati tre anni e si era al 1837 quando Dalton fu colto da paralisi e non fu più in grado di dare lezioni. Così che poca chimica venne appresa da quella fonte ma certamente il metodo, la confidenza e l’entusiasmo per gli apparecchi da laboratorio e la cura nelle misure, oltre all’abitudine di mantenere un diario di ogni suo lavoro sperimentale (possediamo 6 quaderni di laboratorio che contengono le annotazioni originali di Joule di tutti gli esperimenti che realizzò dal 1839 al 1871). I primi dati annotati sono del 1839 e riguardano esperimenti con elettromagneti e motori elettrici. Da notare che siamo ancora in una epoca in cui si credeva di poter ottenere il moto perpetuo con un motore alimentato da una pila di Volta. Di questo argomento e della sua realizzabilità, Joule aveva letto in un articolo del Prof. M.H. Jacobi dell’Università di Dorpat. Egli iniziò le sue sperimentazioni con questo pregiudizio ma, dopo aver fatto prove in tal senso per almeno due anni, evidentemente senza esito, lo stesso Joule ebbe modo di mostrare che un tale motore presentava un consumo maggiore di un buona macchina a vapore (confronto tra il consumo di zinco nella pila con quello del carbone nella macchina a vapore). Nel 1840 troviamo note su esperimenti di elettricità galvanica con un cavallo. Nel 1842 il diario riporta esperienze di spari con pistola vicino alla superficie dell’acqua di un lago per studiarne la profondità mediante l’eco.
Siamo al punto in cui la vita dei due fratelli segue strade diverse e mentre Benjamin si dedica alla musica, James continua con sempre maggiore interesse i suoi esperimenti nel laboratorio che si era costruito nel 1838 in una delle stanze della casa di famiglia (tale laboratorio sarà trasferito, anni dopo, nella fabbrica di birra). Quello stesso anno, quando non aveva ancora venti anni, realizzò il suo primo lavoro, Description of an electro-magnetic engine, with Experiments, che fu pubblicato sotto forma di lettera sugli Annals of Electricity del fisico William Sturgeon (inventore dell’elettromagnete e del motore elettrico di uso pratico, dotato cioè di commutatore e quindi in grado di fornire corrente continua). Ad esso ne seguirono altri due (l’ultimo del 1839), pubblicati nella stessa rivista e sempre sul medesimo argomento, con sempre maggiori perfezionamenti al suo motore elettromagnetico e con le prime misure del lavoro che fa una macchina elettrica. Da notare che in questi lavori viene affermato che si può realizzare un migliore elettromagnete sostituendo il ferro massiccio che lo costituisce con un assemblaggio di piccole lamine di ferro (un’indicazione per Foucault e le correnti parassite)(3).
La prima memoria di Joule
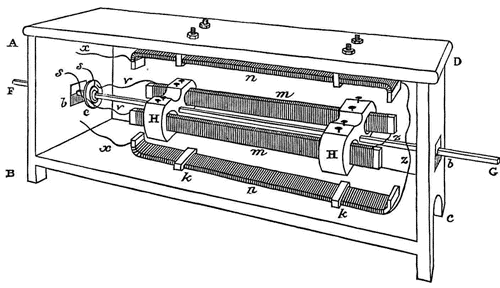
La macchina elettro-magnetica presentata da Joule nella memoria suddetta
C’è qui da fare un’osservazione sulle motivazioni che spingevano Joule a muoversi in una direzione piuttosto che in un’altra. E’ stato osservato che, all’epoca, vi erano varie motivazioni, anche filosofiche (si ricordi la Naturphilosophie), alla base dei lavori di molti scienziati, Faraday, Oersted, Liebig, lo stesso Mayer. Risulta evidente dai lavori di Joule quale era il fine che si proponeva. Egli, intanto, non cercava prove di alcun principio filosofico. Voleva invece dimostrare che i motori elettrici, gli elettromagneti, l’insieme degli apparati che la scienza elettrica aveva realizzato, sarebbero stati in grado di sostituire utilmente e con convenienza economica le macchine a vapore. Per questo iniziò a perfezionare le macchine elettriche affrontandole con lo spirito di un ingegnere industriale. Se il motore elettrico doveva entrare utilmente nell’industria, esso doveva produrre il maggior effetto meccanico possibile con il minor consumo di corrente. Come egli stesso scrive nella sua seconda memoria agli Annals (si noti il cenno al moto perpetuo quando Joule parla di riduzioni all’infinito):
Non posso dubitare del fatto che l’elettromagnetismo finirà col sostituire il vapore nella propulsione di macchine. Se la potenza del primo è in proporzione alla forza attrattiva dei suoi magneti e se quest’attrazione è come il quadrato della forza elettrica, l’economia sarà in rapporto diretto alla quantità di elettricità e il costo di operazione della macchina può essere ridotto all’infinito.
E’ per questo che nei suoi primi lavori egli lavora al perfezionamento dei motori elettrici a partire da ciò che riteneva alla base della loro maggiore redditività, gli elettromagneti. Costruì quindi diverse macchine con diversi arrangiamenti di dimensioni, disposizioni, realizzazione di elettromagneti, avvolgimenti di spire, … al fine di comparare le velocità relative dei motori che otteneva per differenti elettromagneti. Nelle sue prime memorie troviamo tabelle in cui si confronta la corrente elettrica impiegata con la forza elettrica ottenuta ed i pesi sollevati. Si introduce anche la potenza della macchina. Successivamente si confronta l’intensità di corrente con le velocità di rotazione ottenute. E questo per differenti magneti e differenti lunghezze di circuiti induttivi. Alla fine di questi suoi studi che lo impegneranno almeno fino agli inizi del 1840, Joule dovrà riconoscere che al crescere della velocità della macchina, viene indotta una resistenza sempre maggiore nel magnete tanto che resta ancora la convenienza nelle macchine a vapore. Resta qui la fondamentale acquisizione della potenza della corrente e del suo confronto con il lavoro meccanico che essa è in grado di fare, tra l’altro ambedue misurate in unità assolute (basate cioè sulle grandezze fondamentali, lunghezza, massa e tempo). Vedremo tra un poco che in successivi lavori Joule scoprì la relazione tra intensità di corrente in un circuito e calore prodotto. In una sorta di confronto tra le due scoperte troverà l’equivalenza tra lavoro e calore. Ma torniamo alla cronologia.
Nel 1839 Joule iniziò a frequentare la Manchester Literary and Philosophical Society dove conobbe vari scienziati ed iniziò a prendere lezioni di chimica da John Davies uno dei fondatori della Royal Victoria Gallery for the Encouragement and Illustration of Practical Science. Nelle occasioni in cui andava, si recava a trovare Dalton che non aveva mai smesso di incoraggiare tra i giovani lo studio delle scienze. Nel 1840 scrisse, ancora per gli Annals, tre articoli dal titolo On Electro-Magnetic Force.
Sempre del 1840 è il suo primo lavoro di grande rilievo. Si tratta della memoria On the Production of Heat by Voltaic Electricity, pubblicata sui Proceedings of the Royal Society, December 17, 1840.

Il primo lavoro di Joule sul calore prodotto dalla corrente elettrica.
Questo lavoro fu pubblicato sui Proceedings in forma ridotta e fu rifiutato dal Philosophical Magazine perché, sembra, che i giudici del lavoro non potessero credere che un tanto importante risultato fosse ricavato in sole 5 paginette. Esso fu ripreso ed ampliato da Joule in una memoria completa in cui le indagini erano estese al calore sviluppato all’interno di una pila voltaica in funzione in un processo di elettrolisi ed arricchite di una gran quantità di esperienze e misure. Trovò che esiste una relazione tra la quantità di sostanza chimica che consuma la pila, la quantità di calore che riscalda i fili ed il lavoro prodotto dalla macchina azionata dalla corrente. Si tratta della memoria On the heat evolved by metallic conductors of electricity, and in the cells of a battery during electrolysis, pubblicata sul Philosophical Magazine nel 1841.

La memoria di Joule sui Proceedings arricchita di numerose esperienze pubblicata sul Philosophical Magazine nel 1841.
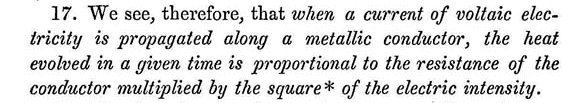
L’enunciato di quanto ricavato dalle molte esperienze.
Si tratta della scoperta di quello che oggi è universalmente noto come effetto Joule: il riscaldamento di un conduttore metallico al passaggio di corrente con relativa legge: il calore che si sviluppa (attenzione: si comincia a parlare di calore che si sviluppa e non più di calore che si trasferisce) in tale fenomeno è proporzionale alla resistenza del conduttore moltiplicata per il quadrato dell’intensità della corrente elettrica che circola nel conduttore in un dato tempo. Ma Joule non si accontentò e proseguì le sue esperienze per mostrare che anche l’elettricità prodotta mediante induzione elettromagnetica in una macchina elettrica dotata di commutazione, praticamente quella che conosciamo come dinamo (che fornisce magneto-elettricità), produce lo stesso fenomeno con la stessa legge.

Il passo di Joule nella memoria di seguito citata in cui si riconosce l’identità di effetti tra la corrente generata da una pila e quella generata da una dinamo
Per realizzare queste complesse esperienze si costruì un generatore magneto-elettrico e misurò il bilancio tra il lavoro fatto dalla corrente ed il calore che veniva sviluppato. Questi risultati li riportò nella sua memoria del 1843 On the Calorific Effects of Magneto-Electricity, and on the Mechanical Value of Heat, pubblicata sul Philosophical Magazine,3rd series, 23, pp. 263-276, 347-355, 435-455. Ed in essa Joule inizia a parlare dell’equivalente meccanico del calore facendo le prime misure.

La memoria di Joule per misurare l’effetto del riscaldamento della corrente prodotta da un generatore ad induzione elettromagnetica.
Quindi le esperienze da cui partì Joule per stabilire l’equivalenza lavoro-calore sono su fenomeni elettrici ed i risultati da lui trovati lasciavano aperte alcune questioni che Joule si era posto: da dove proviene il riscaldamento dei conduttori ? si produce nel conduttore o è trasportato dagli elementi galvanici ai fili ? Se le cose stessero come ora detto si dovrebbe manifestare un raffreddamento simultaneo della pila, un qualcosa di analogo all’effetto Peltier(4) che Joule cita opportunamente. E poiché non si registra alcun raffreddamento, ciò vuol dire che il calore si sviluppa nel conduttore. Questo è ciò che Joule si propone di indagare, come dice esplicitamente all’inizio di questa sua memoria del 1843:
Ho allora deciso di indagare l’incertezza che riguarda il calore magneto-elettrico.
Riprendendo quanto ho scritto qualche riga più su, Joule, per realizzare motori elettrici che sostituissero in economicità le macchine a vapore, aveva scoperto una stretta connessione tra corrente e calore che essa sviluppa. Egli aveva precedentemente trovato che la corrente ha una stretta relazione con il lavoro meccanico. Per una banale proprietà transitiva dovrebbe esservi una stretta relazione tra lavoro meccanico e calore. Questo il filo logico del suo pensiero. Egli, nella prima parte di questa memoria, andò quindi ad indagare ogni possibile modo in cui si produce calore mediante corrente sia con i generatori (pile e dinamo) a vuoto che sotto carico. Iniziò con il mettere in relazione il calore sviluppato in una pila con la quantità di metallo (nel suo caso lo zinco) consumato nella pila medesima. Dimostrò che la quantità di calore corrisponde alla differenza tra il calore sviluppato in una semplice soluzione dello zinco nell’acido e quello prodotto quando lo zinco è consumato nel processo di funzionamento della pila. Calcolò poi il calore che viene sviluppato nei fili mediante una dinamo (il risultato l’ho fornito più su) e si rese conto che si sviluppava meno calore nei fili quando la corrente della dinamo azionava un motore e scoprì la proporzionalità di tale perdita di calore con il lavoro fatto. Nella seconda parte della memoria andò ad indagare qual era il valore meccanico del calore (il became an objet of great interest to inquire whether a constant ratio existed betwen it and the mechanical power gained or lost). Si trattava di dissipare il dubbio, dovuto all’effetto Peltier, rispetto al calore prodotto da un motore elettrico. A tal fine ripeté alcune delle esperienze già fatte aggiungendo le nuove misure che lo interessavano, quelle relative al lavoro meccanico. In particolare prese un tubicino di vetro chiuso ad una estremità e lo rivestì con una foglia di stagno per ridurre la radiazione dall’interno del tubo. Adattò poi degli anelli di legno sul tubo e li avvolse di flanella per migliorare l’isolamento termico. Costruì poi un elettromagnete con un nucleo, composto di lamine di acciaio isolate tra loro, sul quale realizzò un avvolgimento di filo conduttore. Sistemò questo elettromagnete dentro il tubo di vetro che fu successivamente riempito di acqua. Sigillò il tubo facendo uscire dalla chiusura le due estremità dell’avvolgimento di conduttore sul nucleo. Creò un arrangiamento tale che tale tubo potesse ruotare su un asse trasversale tra i poli di un potente magnete (sostituito in una successiva esperienza con un elettromagnete tra i più potenti all’epoca disponibili) mentre i due estremi del conduttore erano collegati, nella parte bassa del sistema rotante, ad un commutatore strisciante (utilizzante del mercurio) che alimentava il circuito con una corrente voltaica la cui intensità si poteva misurare mediante un galvanometro collegato all’avvolgimento dell’elettromagnete girevole (figura seguente).

Disegno dell’apparato progettato da Joule

Realizzazione pratica del progetto. Da: Manchester Museum of Science and Technology.
In tal modo aveva realizzato un motore elettrico che permetteva di misurare il calore che si sviluppava nell’indotto girevole. Faceva girare per un dato tempo (15 minuti) il sistema fornendo il lavoro meccanico con la manovella fino ad una velocità di 600 giri al minuto, quindi apriva rapidamente il tubo di vetro per misurare la temperatura dell’acqua (con un termometro estremamente preciso da lui stesso realizzato) e confrontarla con quella acquistata nelle stesse condizioni ma

Termometro di Joule a dilatazione con mirino microscopico. Da: Manchester Museum of Science and Technology.
senza collegamento con la pila. Trovò che il calore emanato da una nucleo di ferro che gira tra i poli di un magnete è proporzionale al quadrato della forza induttrice e che il calore emanato dall’avvolgimento della macchina elettromagnetica è proporzionale (a parità delle restanti condizioni) al quadrato della corrente. Fece molte esperienze in cui la corrente voltaica circolava nello stesso verso di quella indotta (l’apparato funzionava come dinamo fornendo corrente) ed in verso contrario (l’apparato funzionava consumando lavoro meccanico). Tenne conto della corrente della dinamo che non era continua ma pulsante. Analizzò gli effetti termici prodotti sia dalla corrente voltaica che dalla corrente della dinamo e dedusse che nell’elettricità magnetica vi è un agente capace, con semplici mezzi meccanici, di distruggere o di generare il calore.
Si trattava, a questo punto, di verificare se esisteva una relazione tra il calore ed il lavoro meccanico. Dice Joule:
Avendo provato che il calore è generato da una dinamo e che utilizzando il potere induttivo del magnetismo noi possiamo diminuire o aumentare a piacere il calore dovuto alle reazioni chimiche, diventa argomento di grande interesse indagare se vi è un rapporto costante fra esso ed il lavoro meccanico aumentato o diminuito. A questo fine è solo necessario ripetere alcune delle precedenti esperienze e accertare, al medesimo tempo, la forza meccanica necessaria a far girare l’apparato.
Per fare ciò confrontò i risultati dell’esperienza che aveva proposto nella prima parte della memoria con quella che proponeva ora e che consisteva nel cambiare il meccanismo di rotazione dell’elettromagnete all’interno del tubo di vetro con un sistema meccanico che permettesse di misurare il lavoro fatto con notevole precisione in sostituzione della manovella. Due cordicelle sottili, avvolte intorno ad un cilindro e passanti su due pulegge, erano in grado di far ruotare il medesimo cilindro mediante la caduta di pesi sospesi alle loro estremità. Questo era il sistema che egli utilizzò per sostituire la manovella della precedente esperienza (figura seguente).

Mediante questo dispositivo, che più avanti utilizzò per altre sue famose esperienze, poteva trasformare il lavoro meccanico fatto dalla caduta dei pesi in corrente elettromagnetica mediante il collegamento alla dinamo della precedente esperienza. Questa corrente veniva poi convertita in calore mediante la sua dissipazione in una resistenza immersa nell’acqua contenuta in un calorimetro. In definitiva si aveva conversione di lavoro meccanico in calore. Fece molte esperienze e misure che fornivano questi risultati: mettendo sui piatti 3,5 Kg di peso si otteneva una velocità dell’elettromagnete di circa seicento giri al minuto, quando gli estremi dell’avvolgimento intorno al nucleo erano collegati con una pila (Daniell); ma quando si interrompeva tale connessione, per vincere la resistenza (in questo caso originata solo dall’attrito e dalla resistenza dell’aria), serviva circa la metà di peso. La differenza tra i due pesi era quella che, nella caduta, originava la corrente fornita dalla dinamo. Le esperienze precedenti gli avevano fatto trovare quanto calore si sviluppa nel passaggio della corrente in un conduttore (ed anche quello che si genera in una scintilla). Si calcolò ora le capacità termiche di tutti gli elementi componenti il suo apparato (tubo di vetro, acqua, elettromagnete situato nel tubo) e, mettendo insieme i risultati (ma trascurando, come riconobbe in seguito, il calore dissipato dal potente elettromagnete che abbracciava il tubo rotante), trovò che:
La quantità di calore capace di aumentare la temperatura di un pound [o libbra o 453,59237 grammi, ndr] di acqua di un grado della scala Fahrenheit è uguale a, e può essere convertito in, una forza meccanica capace di sollevare 838 libbre [circa 380 Kg, ndr] ad una altezza perpendicolare di un piede [30, 48 cm, ndr].
[Con le nostre unità, Joule aveva trovato che il lavoro di 838 libbre x piede corrisponde a 4510 joule/Kilocaloria].
Si può quindi convertire, in un senso o in un altro, lavoro meccanico e calore secondo la relazione fornita. E con questi dati Joule non si lasciò sfuggire l’occasione di andare a calcolare la conversione di calore in lavoro di una macchina a vapore tra le migliori, quella del 1834 di Roland Cornish in funzione nelle miniere di rame di Huel Towan, in Cornovaglia. In tale macchina la combustione di una libbra di carbone fornisce 11,437° a una libbra di acqua. Quindi, per quanto abbiamo più su visto, il calore sviluppato dalla combustione di una libbra di carbone è equivalente al lavoro meccanico capace di sollevare circa 9.584 libbre all’altezza di un piede, cioè a circa 10 volte il rendimento della migliore macchina a vapore. Joule faceva poi lo stesso confronto tra il lavoro meccanico dato dal consumo di carbone in una macchina a vapore ed il lavoro meccanico prodotto dal consumo di zinco in una pila voltaica che alimenta una dinamo, trovando che è impensabile, rispetto al consumo, sostituire una macchina a vapore con macchine alimentate da pile voltaiche (alla cosa ho già accennato parlando delle prime fantasie di Joule sulla possibilità di moto perpetuo proprio con motori elettrici). In un post scriptum Joule riconosce al Conte Rumford di aver compreso l’origine del calore sviluppato dall’attrito nella alesatura dei cannoni in nessun caso attribuibile alla variazione di capacità termica del metallo. Ma aggiunge un passo controverso:
Non perderò tempo a ripetere e ad estendere questi esperimenti, essendo soddisfatto di avere accertato che i grandi agenti della natura sono, per virtù del fiat del Creatore, indistruttibili; e che qualunque forza meccanica venga spesa, si ottiene sempre un equivalente esatto del calore.
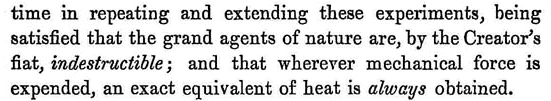
Il passo controverso
Questo brano è stato interpretato, a partire dalla classica biografia di Joule di Osborn Reynolds del 1892, come se Joule avesse scoperto per primo non già l’equivalente meccanico del calore ma il principio di conservazione dell’energia. A tale proposito si può certamente essere d’accordo con Elkana:
È questa la fonte che viene generalmente considerata quando si sostiene che il principio è stato scoperto da Joule (per esempio, E. C. Watson […]). Ciò che Watson e altri non si chiedono è come sia possibile che, se Joule si rese conto di quest’implicazione della sua scoperta, non tornò mai più a scrivere su quest’argomento, né rivendicò il “principio di conservazione dell’energia” come un suo contributo; inoltre nella sua opera non vediamo alcun mutamento interno dopo questa presunta “esposizione generale”.
Il lavoro di Joule non si fermò, anzi. Continuarono sue memorie sperimentali una dopo l’altra e tutte con un rigore nelle misure veramente ammirevole. E’ impossibile in un lavoro con le caratteristiche di quello che state leggendo soffermarsi su tutti i lavori ed i dettagli di grande interesse. Cercherò di cogliere le parti che ritengo di maggiore interesse ai fini che mi sono proposto (essenzialmente la comprensibilità di ciò che scrivo ad un pubblico che spero vasto).
La prima memoria di Joule che stabilisce una importante correzione a quanto avevano fatto sia Carnot che Clapeyron è On the Changes of Temperature produced by the Rarefaction and Condensation of Air, pubblicata in sunto sui Proceedings of Royal Society, 1844 e integralmente l’anno successivo sul Philosophical Magazine. Intanto c’è da distaccare l’interesse che la Royal Society di Londra, diretta da Michael Faraday, riservava ai lavori del giovane Joule e ciò permetterà ai suoi lavori di essere conosciuti più facilmente all’estero. Il lavoro consisteva in un modo diverso di calcolare l’equivalente meccanico del calore. Joule lo concluse affermando che i risultati che aveva trovato sembrano essere in contraddizione con le idee dei due fisici suddetti i quali supponevano che non c’è perdita di calore durante il funzionamento di una macchina a vapore. La teoria che qui si propone, scriveva Joule, esige che il calore, entrando nel condensatore, sia minore di quello comunicato alla caldaia con la combustione del carbone, in esatta proporzione con l’equivalente meccanico del lavoro meccanico realizzato. E la correzione è fondamentale per sbarazzarsi della teoria del calorico indistruttibile e per avviare a buon cammino la scoperta della conservazione dell’energia.
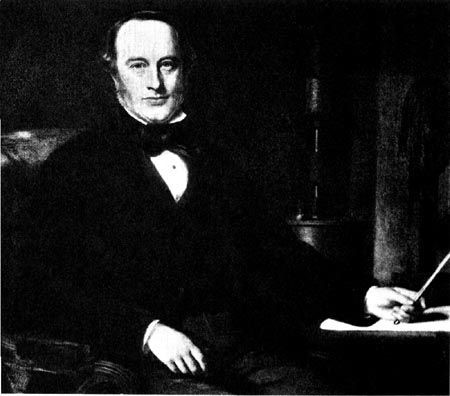
Poiché ancora provava grande curiosità nel confronto fra i rendimenti della macchine a vapore da confrontare con quelli dei motori elettrici, Joule iniziò una collaborazione con il Reverendo William Scoresby, una volta capitano di marina ed esploratore dell’Artico ed ora parroco di Bradford interessato alle scienze (da sottolineare che Joule è uno dei primi fisici a scrivere delle memorie in collaborazione con altri; lo farà anche con Lyon Playfair e Kelvin). Scoresby era famoso per disporre di potentissimi elettromagneti. I due si conobbero ad una riunione della Britsh Association di Manchester nel 1842 e iniziarono a collaborare. Joule voleva far funzionare i suoi motori elettrici con quegli elettromagneti per poter raggiungere il loro massimo rendimento. Ne venne fuori una memoria, Experiments and Observations on the Mechanical Powers of Electro-Magnetism, Steam, and Horses, pubblicata sul Philosophical Magazine nel 1846.

La memoria di Joule con Scoresby. Si noti che parte delle esperienze si fecero nel Vicariato.
Anche qui interessa conoscere cosa ricavò Joule dall’accurato confronto tra i rendimenti delle due macchine. Egli scoprì che la migliore macchina a vapore, ancora la Cornish, forniva solo un decimo della forza viva (è da un poco che Joule si è convertito a questa terminologia) dovuta alla combustione del carbone. C’era ancora da capire qual era la forza viva prodotta da un cavallo (in carne ed ossa). Qui Joule fa uno studio del potere calorifico del mais e del fieno (provocando la combustione di una miscela dei due alimenti in ossigeno) che vengono dati come alimento medio ad un cavallo e del corrispettivo di lavoro medio che è in grado di fare. Le sue conclusioni furono che un quarto del totale della vis viva prodotta dalla combustione dell’alimento nell’organismo animale è in grado di produrre un effetto meccanico utile, risultano necessari i rimanenti tre quarti rimanenti per mantenere il calore animale(5).
Altre memorie furono dedicate al modo di calcolare il calore specifico dei corpi, anche utilizzando correnti elettriche.
Nel giugno 1845 Joule presentò una comunicazione alla riunione della British Association a Cambridge. Un breve resoconto della comunicazione, On the Mechanical Equivalent of Heat, fu pubblicato nei Brit. Assoc. Rep., trans.
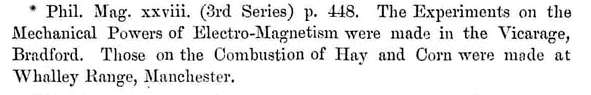
Chemical Sect, p.31. Successivamente, per dare maggiore risalto al suo lavoro, lo annunciò con una lettera, On the existence of an Equivalent Relation between Heat and ordinary Forms of Mechanical Power, al Philosophical Magazine (27, 1845, pag. 205). E’ una breve nota in cui si annuncia un metodo ancora differente

per ricavare l’equivalente meccanico del calore. Altra breve nota, di appena 3 pagine, comparirà sui Comptes Rendus de l’Académie des Sciences di Parigi (Expériences sur l’Identité entre le Calorique et la Force Mécanique, 1847) e, fatto importante, tale memoria era stata richiesta a Joule da Biot, Pouillet e Regnault, come prova del grande interesse francese per questa scoperta, da confrontare con il quasi completo disinteresse inglese che, noblesse oblige, usava pensare che non poteva venir fuori nulla di buono dalla provincia.

L’articolo completo, scritto nel 1849 e con le figure che illustrano la strumentazione, sarà infine pubblicato sulle Philosophical Transactions of the Royal Society di Londra (On the mechanical Equivalent of Heat, 1850) e la presentazione di questo lavoro alla Royal Society fu fatta dal medesimo Faraday e dopo la sua pubblicazione, Joule fu designato membro della Society a 31 anni, prima di quanto non riuscisse a fare Faraday (32 anni). Le figure che riporterò più oltre sono tratte da questa ultima versione delle esperienze di Joule.

La memoria con l’articolo completo sull’equivalente meccanico del calore. Si noti che, nel frattempo Joule è stato nominato corrispondente straniero dell’Accademia delle Scienze di Torino.
Iniziamo con leggere alcuni brani della lettera al Philosophical Magazine. Scrive Joule che:
L’apparato [per misurare l’equivalente meccanico] che avevo mostrato alla British Association consisteva di una ruota a pale di ottone che lavorava orizzontalmente in un recipiente pieno d’acqua. A questa ruota si poteva comunicare del moto mediante pesi, carrucole, ecc., […] La ruota si muoveva con grande resistenza nel recipiente d’acqua, di modo che i pesi (ciascuno dei quali ammontava a quattro libbre) scendevano con una velocità relativamente bassa di circa un piede al secondo. L’altezza delle carrucole rispetto al suolo era di dodici yarde, e, conseguentemente, quando i pesi erano discesi per tutta questa distanza, li si doveva far risalire al fine di rinnovare il moto della ruota. Dopo aver ripetuto per sedici volte questa operazione l’aumento della temperatura dell’acqua veniva accertato mediante un termometro molto sensibile e accurato.
Vediamo ora il famoso apparato di Joule che ancora oggi si trova su ogni testo elementare di fisica. Come si vede dalla figura seguente si ha un calorimetro dentro il quale vi sono delle palette immerse in acqua. Le palette sono mosse da un sistema analogo a quello visto in una esperienza precedente: due cordicelle, passanti attraverso due pulegge, si srotolano intorno ad un cilindro mediante la caduta di sue pesi posti alle loro estremità.
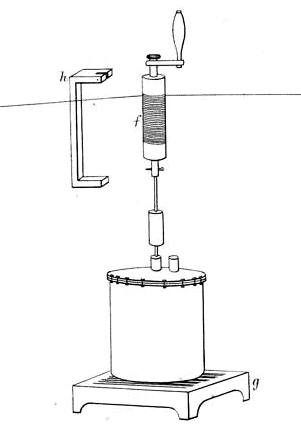
Calorimetro con l’asse solidale con le palette che sono all’interno. Sull’asse vi è il cilindro con le corde avvolte in senso opposto e dal cui svolgimento (per la trazione dei pesi) si origina la rotazione del mulinello costituito da varie palette. Il foro laterale è l’alloggiamento del termometro.
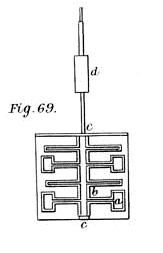
Sezione del calorimetro che permette di vedere le palette solidali con l’albero c, c che hanno una disposizione in pianta come quella mostrata in figura seguente.
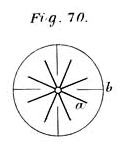
Disposizione vista dall’alto delle palette del calorimetro. Si tratta di un albero rotante (c, c) su cui sono fissate otto (per due) palette (a, a) che ruotano solidalmente in mezzo a quattro ostacoli fissi (b, b), in modo da produrre il massimo attrito con il liquido disposto nel calorimetro. Si deve notare che le palette radiali fisse avevano uno scopo ben preciso: evitare che l’acqua acquistasse energia cinetica di movimento (facesse mulinello trascinata dalle palette rotanti).

Foto del calorimetro (vaso di rame rivestito poi di materiali atti ad impedire la trasmissione del calore per conduzione e per irraggiamento) e del sistema di palette dell’apparato originale usato da Joule. Da: Manchester Museum of Science and Technology.
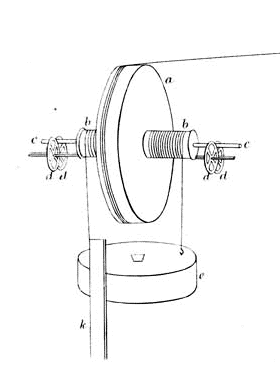
Una delle due pulegge a (un piede di diametro e 2 pollici di spessore) che ruota su un asse (2 pollici di diametro). In primo piano vi è un’asta graduata k che scende fino al suolo (altezza totale h = 150 cm). Subito dietro vi è un grosso peso e (dai 13 ai 5 Kg per diverse esperienze) che scende srotolando le due cordicelle arrotolate sull’asse b, b della puleggia a cui è appeso. La cordicella in alto che va verso destra è connessa al cilindro centrale f.
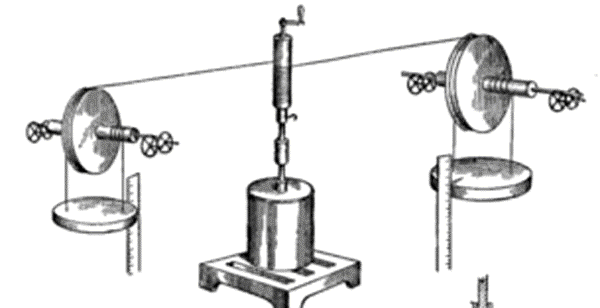
Il montaggio dell’intera esperienza
Joule, prima di procedere alle misure, si accertò di ogni dettaglio, misurò temperatura e pressione del laboratorio (cosa che ripeté a metà esperienza ed alla fine di essa). La caduta dei pesi avveniva con una velocità di circa 6 cm/sec; la durata di ogni misura era di 35 minuti.
Per calcolare con precisione la quantità di calore Q sviluppato dall’attrito delle palette rotanti con l’acqua, Joule si calcolò, con i metodi indicati da Regnault, il calore specifico dell’acqua c, del recipiente di rame e del sistema di palette. Detto con linguaggio oggi corrente, si calcolò l’equivalente in acqua del calorimetro e del sistema di palette. Misurò poi la massa d’acqua alla quale aggiunse gli equivalenti in acqua precedentemente calcolati (massa totale = m). Da qui si ricavò la capacità termica totale C = c.m. Misurò la differenza di temperatura Δ t nel calorimetro tra l’inizio dell’esperienza e dopo la caduta dei pesi (ripetuta 20 volte di seguito). Osservo che questa era la parte più delicata perché le differenze di temperatura erano molto piccole (difficilmente si superava in mezzo grado) e l’errore era molto facile se non si consideravano tutte le possibili dispersioni. Queste misure comunque gli permettevano di calcolare la quantità di calore sviluppato dall’attrito delle palette con l’acqua (Q = C.Δ t).
Restava da calcolare il lavoro meccanico fatto per produrre quel calore. Non si tratta soltanto di moltiplicare la massa per l’altezza da cui cade ma anche di sottrarre a questa quantità quella parte che va a riscaldare per attrito (non l’acqua ma) i vari meccanismi in funzione (attrito tra pulegge e cordicelle; del sistema ruotante sui cardini)() e la forza viva che la massa ha ancora quando giunge al suolo (che data la bassa velocità di caduta, Joule non prende in considerazione). In definitiva Joule calcolò questo lavoro meccanico come prodotto di un’altezza per un peso (alla quale quantità aveva sottratto quella che produceva gli effetti di riscaldamento).
Joule concludeva l’articolo affermando che con i suoi esperimenti aveva dimostrato:
1 – che la quantità di calore prodotta dall’attrito tra due corpi, siano essi solidi o liquidi, è sempre proporzionale alla quantità di lavoro meccanico speso. E
2 – che la quantità di calore capace di aumentare la temperatura di una libbra di acqua […] di 1°Fahrenheit richiede un lavoro meccanico speso equivalente alla caduta di 772 libbre dall’altezza di un piede.
Un’ultima osservazione. Joule si accertava, come ho accennato, che alla fine dell’esperienza le condizioni (temperature, pressione, …) tornassero come erano all’inizio. Ciò è molto importante perché, come diremmo oggi, egli lavorava su un ciclo chiuso. Questa osservazione sarà importante per distinguere l’equivalenza lavoro-calore dalla conservazione dell’energia (ciclo aperto).
Con questa esperienza, ripetuta più volte, Joule determinò, ancora una volta, l’equivalente meccanico del calore che gli risultò (con unità in uso oggi) nel 1845 di 4780 joule/Kcal. Ripetuta l’esperienza due anni dopo dette per risultato 4180 joule/Kcal. Essa fu fatta con diversi liquidi dentro il calorimetro e fornì sempre l’ultimo valore che ho ora dato. Ripetuta ancora nel 1850, con la massima cura possibile (ruote a pale di ottone e ferro che lavoravano con differenti liquidi calorimetrici e due ruote di ferro con sfregamento relativo) per l’equivalente fornì il valore di 4130 joule/Kcal. L’ultima misura che fece Joule nel 1878 gli dette ancora tale valore, vicino a quello che oggi accettiamo (4184 joule/Kcal).
Nel 1847 Joule tenne una conferenza nella sala di lettera della Chiesa di Sant’Anna a Manchester, On matter, Living Force, and Heat, che fu pubblicata sul Courier della città (maggio 1847). Si tratta di una sorta di resoconto quasi divulgativo delle ricerche che aveva fino ad allora fatto.

Leggiamone qualche passo.
La regola generale è che quando la forza viva viene apparentemente distrutta sia per urto che per attrito o altro mezzo simile, viene prodotto un esatto equivalente di calore. Il reciproco di questa proposizione è anche vero, cioè che il calore non può essere diminuito o assorbito senza la produzione di forza viva [energia cinetica, ndr] o il suo equivalente in attrazione spaziale [energia potenziale, ndr]. Così per esempio in una macchina a vapore si troverà che la potenza guadagnata è alle spese del calore del fuoco. Cioè che il calore generato dalla combustione del carbone sarebbe stato maggiore se una parte non ne fosse stata assorbita a produrre e mantenere la forza viva della macchina. È corretto però osservare che ciò non è stato ancora dimostrato sperimentalmente. Tuttavia non c’è dubbio che l’esperimento proverebbe che quanto ho detto è corretto; perché io stesso ho provato che vi è conversione di calore in forza viva nell’espansione dell’aria che è analoga all’espansione del vapore nel cilindro di una macchina a vapore. Ma la prova più convincente della conversione del calore in forza viva è derivata dai miei esperimenti con la macchina elettromagnetica, una macchina composta di magneti e sbarre di ferro messa in moto da una batteria elettrica. Io ho provato che calore viene estratto dalla batteria in esatta proporzione alla forza con cui lavora la macchina. Vedete pertanto che la forza viva può esser convertita in calore e il calore in forza viva o la sua equivalente attrazione spaziale. Tutti e tre quindi – calore, forza viva e attrazione spaziale (a cui potrei aggiungere anche la luce se non esulasse dallo scopo di questa conferenza) – possono esser convertiti mutuamente uno nell’altro. In queste conversioni nulla è mai perso. La stessa quantità di calore sarà sempre cambiata nella stessa quantità di forza viva. Possiamo pertanto esprimere la equivalenza in un linguaggio preciso che si applica sempre e in tutte le circostanze. Così l’attrazione di 817 libbre per lo spazio di un piede [per l’accelerazione di gravità Joule assume 9,75 m/sec2, ndr] è equivalente e convertibile nella forza viva dello stesso corpo quando si muove con la velocità di 8 piedi al secondo e questa forza viva è a sua volta convertibile nella quantità di calore che fa aumentare la temperatura di una libbra d’acqua di un grado Fahrenheit [i valori qui forniti da Joule fanno ricavare per l’equivalente meccanico della caloria 1 joule = 4390 Kcal, ndr].
Abbiamo rivisto molte cose già dette alle quali si può aggiungere una ulteriore considerazione che fa Elkana:
Vorrei sottolineare ancora una volta che Joule parla della generale convertibilità di ogni forma di forza in calore. In nessun luogo egli dice che queste varie forze siano di fatto lo stesso tipo di cosa o che la loro somma sia costante. […] Che le affermazioni di Joule fossero equivalenti ad esempio alla formulazione di Helmholtz fu dimostrato solo nel 1855 da Rankine.
L’anno di questa conferenza, il 1847, è un anno in cui la nozione di equivalenza tra lavoro e calore e di conservazione dell’energia va emergendo da varie parti (non a caso questa scoperta è studiata come caso di scoperta simultanea). Già 3 anni prima, nel 1846, il fisico gallese William R. Grove (1811 – 1896) aveva pubblicato un saggio dal titolo, On The Correlation of Physical Forces: Being the Substance of a Course of Lectures Delivered in the London Institution in the Year 1843, (London Institution, 1846), nel quale si avanzavano ipotesi sulla conservazione dell’energia con esperienze sui gas e sulle celle elettrolitiche. Nel 1843, lo cito per completezza, il fisico ed ingegnere danese Ludwig August Colding (1815 – 1888), scrisse una memoria, Nogle saetninger om kraefterne (Ipotesi sulla natura della forza), letta alla Royal Danish Academy of Sciences and Letters, e pubblicata dallo stesso Colding nel 1856, nella quale dallo studio dell’attrito tra diversi materiali e della loro compressione ricavò che le quantità di calore sviluppate sono, in ogni caso, proporzionali alle forze di movimento. Ma poi si perse nella più pura metafisica assimilando forze ad entità spirituali. Anche Faraday ruotava intorno all’argomento in quegli anni. Nello stesso 1847 viene pubblicata la memoria più importante edefinitva sull’argomento conservazione dell’energia, quella di Helmholtz, Über die Erhaltung der Kraft (Sulla conservazione della forza), sulla quale tornerò diffusamente nel prossimo articolo. Nel 1848 Mayer apre la controversia con Joule scrivendo un articolo per i Comptes Rendus (ho accennato già a tale articolo) e nello stesso anno arriva a Joule un primo importante riconoscimento internazionale, la nomina a membro corrispondente della Accademia Reale delle Scienza di Torino.
Ancora nel 1847 Joule doveva fare una comunicazione alla riunione annuale della British Association for the Advancement of Science che si teneva ad Oxford. Prima che prendesse la parola, il Presidente della riunione lo invitò ad essere breve raccontando solo i risultati delle esperienze, in quanto, in passate riunioni, l’argomento non aveva suscitato interesse. Joule eseguì e, come altre volte, la sua esposizione sarebbe passata inosservata. Alla riunione era però presente, oltre che a Faraday, un giovane fisico di 22 anni dal talento eccezionale, William Thomson (il futuro Lord Kelvin), che scosse l’assemblea con delle obiezioni (già fatte a Joule da Graham e Miller) sull’inattendibilità dei suoi risultati in quanto ricavati da frazioni di grado di temperatura. Le obiezioni molto precise nascevano da alcuni lavori che lo stesso Thomson stava elaborando. L’articolazione della vicenda è ben raccontata da Elkana:
Thomson, pur essendo molto impressionato dalle esperienze di Joule, non era convinto. Il motivo della sua perplessità va ricercato nella teoria di Carnot.
L’interesse primario di Kelvin per la teoria di Carnot e Clapeyron va visto nel suo desiderio di stabilire una scala assoluta della temperatura: ossia un termometro indipendente dalla sostanza termometrica. Secondo la teoria di Carnot un tale progetto era realizzzabile perché in essa “quantità di calore e intervalli di temperatura sono nell’espansione gli unici elementi determinanti per la quantità di effetto meccanico che dev’essere ottenuto attraverso l’azione del calore“.
Proprio qui si vede l’intuizione scientifica di Thomson. Egli si pose un nuovo problema: quello di abolire la contraddizione esistente fra i risultati di Joule e quelli di Carnot. Sapeva che Carnot aveva ottenuto risultati sperimentali validi. Vedeva anche che i risultati ottenuti da Joule erano molto precisi. Com’era possibile che i loro risultati, corretti in entrambi i casi fossero derivati da ipotesi contraddittorie? Thomson trascorse gli anni seguenti a investigare su questo problema. Nel 1851, infine, trovò la risposta. Il suo saggio fondamentale apparve nelle “Transactions” della Royal Soclety di Edimburgo. Era intitolato On the Dynamical Theory of Heat.
Considerando i problemi di Joule e Thomson, è chiaro che era assolutamente essenziale decidere fra la teoria del calorico e la teoria dinamica del calore, ossia fra un principio di conservazione e un principio di convertibilità. Non stupisce pertanto che questo saggio del 1851, in cui Thomson riconcilia con successo i principi di Joule e di Carnot, non sia intitolato On the Conservation of …, bensì On the Dynamical Theory of Heat.
Le obiezioni di Thomson a Joule scossero la distratta platea e servirono, da quel momento, ad interessare il mondo scientifico a quella scoperta. Inoltre servirono a creare una forte amicizia che divenne anche collaborazione scientifica. Fa quel momento i due si scambiarono una fitta corrispondenza.
Anche la vita privata di Joule cambiò nel 1847. Si sposò con Amelia Grimes e fece il viaggio di nozze sulle Alpi. Lì si divertì a misurare la temperatura dell’acqua ai piedi ed in cima ad una cascata, trovandola più elevata in basso. Ebbe due figli anche se il suo matrimonio durò solo 7 anni, per la improvvisa morte della moglie. Tornò allora a vivere con il padre che però morì nel 1858 anno in cui egli stesso riuscì a sopravvivere ad un incidente di treno che gli creò la paura di intraprendere viaggi con tale mezzo.. Nel 1864 morì anche suo fratello minore John.
Nel 1848 Joule presentò alla Manchester Society ed alla riunione di Swansea della British Association un altro lavoro di grande importanza, On the Mechanical Equivalent of Heat, and on the Constitution of Elastic Fluids (Rep. Brit. Assoc. 1848, Sections, p. 21. Letta prima alla British Association at Swansea, Agosto

1848), seguito subito dall’altro, Some Remarks on Heat and the Constitution of Elastic Fluids (Memoirs Manchester Lit. & Phil. Soc. vol. ix. p. 107. Letta Oct. 3,1848. Anche Phil. Mag. ser. 4. vol. xiv. p. 211).

In queste memorie, per la prima volta, Joule espone le sue idee sulla natura del calore e sulla teoria cinetica dei gas. Scrive che finalmente ha accettato la teoria di Herapath(7). Combinando le sue teorie sul calore con le elaborazioni di Herapath, di Daniel Bernouilli (1738), di Euler(8), adottando per lo zero assoluto della temperatura il valore più recente di tutti quelli trovati, e cioè – 491°F (è quella la temperatura in corrispondenza della quale la pressione si riduce a zero) valore ottenuto estrapolando la legge di Amontons,(9) ed usando un valore sperimentale per la costante di proporzionalità relativa all’idrogeno, calcolò che la velocità di una particella di idrogeno, a 60°F e a trenta pollici di pressione atmosferica, è di 6225, 54 piedi al secondo ma se si scende a 30°F questa velocità si riduce a 6055. Non è una cosa da poco perché si tratta dei primi calcoli sulla velocità media delle particelle di un gas ed i valori ottenuti concordano abbastanza con le determinazioni odierne. Joule spiegò che la velocità media delle particelle del vapor d’acqua, azoto, ossigeno e biossido di carbonio sono inversamente proporzionali alla radice quadrata dei loro pesi specifici, di modo che una particella di ossigeno che ha un peso specifico 16 volte maggiore di quello dell’idrogeno, dovrà avere una velocità uguale alla quarta parte di una particella di idrogeno al fine di produrre la medesima pressione. Da qui si deduce che la velocità media di una particella di ossigeno a 32°F e 30 pollici di pressione deve essere di 1514 piedi al secondo.
Ma vediamo come Joule imposta e risolve il problema, leggendo dalla sua seconda memoria sull’argomento.
Supponiamo che un recipiente con le dimensioni e la forma di un piede cubico sia riempito con del gas idrogeno, che, alla temperatura di 60° [Fahrenheit, ndr] e alla pressione di 30 pollici di mercurio, peserà 36,927 grani [10 grani equivalgono a circa 0,65 grammi, ndr]. Supponiamo ancora che tale quantità di gas sia divisa in tre particelle elastiche, infinitamente piccole e tra loro eguali, ciascuna delle quali peserà 12,309 grani; e, inoltre, che ciascuna di queste particelle oscilli tra facce opposte del cubo e mantenga una velocità uniforme salvo all’istante dell’urto; si chiede di trovare la velocità con cui ogni particella deve muoversi per produrre una pressione di 14 831 712 grani su ciascuna delle facce del cubo(10). In primo luogo si sa che, se un corpo in moto con la velocità di 32 1/6 piedi al secondo viene opposto, per un secondo, a una pressione pari al suo peso, il suo moto verrà arrestato, e che, se la pressione viene applicata ancora per un altro secondo, la particella acquista la velocità di 32 1/6 piedi al secondo nella direzione opposta. A questa velocità, su ciascuna faccia del recipiente cubico si avrebbero, ogni due secondi, 32 1/6 urti da parte di ciascuna particella pesante 12,309 grani; e la pressione esercitata sarebbe pertanto pari a 12,309 x 32 1/6 = 395,938 grani. Perciò, poiché è chiaro che la pressione sarà proporzionale al quadrato della velocità della particella, avremo che quest’ultima, al fine di produrre la pressione di 14 831 712 grani su ciascuna faccia del recipiente cubico, dovrà essere:
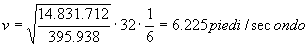
La velocità ottenuta testé sarà capace di produrre la pressione atmosferica, sia che le particelle si urtino tra loro prima di arrivare alle facce del recipiente cubico, sia che colpiscano queste ultime lungo direzioni oblique, e, in terzo luogo, quale che sia il numero di particelle in cui sono suddivisi i 36,927 grani di idrogeno.
Se nel recipiente cubico fosse racchiusa solamente una metà di quell’idrogeno, e cioè 18,4635 grani, e se la velocità delle particelle fosse come prima 6225 piedi al secondo la pressione sarebbe evidentemente solo la metà di quella precedente: il che mostra che la legge di Boyle e Mariotte è una conseguenza naturale dell’ipotesi.
La velocità suddetta è quella dell’idrogeno alla temperatura di 60°; ma sappiamo che la pressione di un fluido elastico a 60° sta a quella che si ha a 32°, come 519 sta a 491. Pertanto la velocità delle particelle a 60° starà a quella che si ha a 32° come √519 sta a √491: il che mostra che la velocità alla temperatura di congelamento dell’acqua è pari a 6055 piedi al secondo.
Nei calcoli sino ad ora eseguiti si suppone che le particelle di idrogeno non abbiano dimensioni sensibili; in caso contrario le velocità corrispondenti alla stessa pressione sarebbero diminuite.
Poiché la pressione di un gas cresce con la temperatura in progressione aritmetica, e poiché la pressione è proporzionale al quadrato della velocità delle particelle, ossia alla loro vis viva, segue che i valori assoluti della temperatura, della pressione e della vis viva sono tra loro proporzionali, e che lo zero della scala delle temperature è a 491° al di sotto del punto di congelamento dell’acqua. Inoltre il calore assoluto del gas, ovvero, in altre parole, la sua capacità, sarà rappresentato dall’ammontare complessivo della vis viva a una data temperatura. Si può allora determinare il calore specifico nel semplice modo seguente:
Si è stabilito che la velocità delle particelle di idrogeno, alla temperatura di 60°, è di 6225 piedi al secondo: una velocità equivalente a una caduta lungo la verticale da un’altezza di 602342 piedi. La velocità a 61° sarà 6225 √520/519 = 6230,93 piedi al secondo, equivalente alla caduta da 603 502 piedi. La differenza tra le due cadute è di 1160 piedi, che è pertanto lo spazio nel quale la pressione di una libbra deve agire su ciascuna libbra di idrogeno per far crescere la sua temperatura di un grado. Ma il nostro equivalente meccanico del calore mostra che per far crescere di un grado la temperatura dell’acqua è necessaria una forza rappresentata da un’altezza di 770 piedi; di conseguenza il calore specifico dell’idrogeno sarà 1160/778 = 1,506, prendendo quello dell’acqua come unità.
Il calore specifico degli altri gas potrà essere facilmente dedotto da quello dell’idrogeno; infatti la vis viva totale e la capacità di volumi uguali dei vari gas saranno tra loro eguali; e la velocità delle particelle sarà inversamente proporzionale alla radice quadrata della gravità specifica. Quindi il calore specifico sarà inversamente proporzionale alla gravità specifica: una legge, alla quale De la Rive e Marcet sono giunti per via sperimentale.
Siamo al 1850 quando ormai il trentunenne Joule aveva raggiunto fama in ogni ambiente scientifico. Ha tutta una vita avanti a sé e farà molti altri lavori anche importanti: studiò la velocità del suono nell’aria, le stelle cadenti, i fulmini, spiegò che il rumore che si accompagna alla magnetizzazione del ferro, o magnetic tick, è dovuto al suo cambiamento di dimensioni (magnetostrizione), costruì eccellenti pompe da vuoto a diffusione con trappole di mercurio che servirono successivamente ad altri per le più diverse ricerche includendo le scariche nei gas, costruì termometri accuratissimi, termometri per misurare la temperatura atmosferica senza risentire del calore radiante, realizzò galvanometri a bussola delle tangenti, realizzò un apparato per determinare la componente orizzontale del campo magnetico terrestre, … Nonostante tutto ciò, il livello delle scoperte e delle elaborazioni già realizzate non saranno più raggiunte.
In qualche modo sembra quasi che Joule avesse esaurito un campo di ricerca con la difficoltà di trovarne altri. Occorre dire che la fisica diventava sempre e sempre più legata a sofisticatissime elaborazioni matematiche e Joule non aveva una preparazione in tal senso. Gli stessi sviluppi della termodinamica che lo avevano visto giganteggiare, saranno di Thomson, Clausius, Rankine, Helmholtz che avevano quella preparazione che lui non aveva. Qualcuno ha avanzato l’ipotesi che proprio il sodalizio che iniziò con Thomson fosse l’origine del rallentamento di Joule. Joule aveva un grande rispetto per le elaborazioni teoriche e quindi molto formalizzate di Thomson e sembra quasi che si sia subordinato a lui. Nei lavori fatti con Thomson scopriamo un Joule che non si pone alla pari con il suo brillante collega ma che diviene quasi un suo assistente di grande rango, ma assistente. Ma vi è forse un’ipotesi più attendibile a questa situazione: la salute di Joule decadeva ed egli, che aveva un carattere chiuso e debole, doveva aver molto sofferto per le disgrazie che si abbattevano sulla salute della sua famiglia.
Vi sono comunque alcuni suoi lavori che meritano ancora un minimo di attenzione.
Nel 1851 Joule scrisse un lavoro d’interesse, On the Air-Engine (Philosophical Transactions, 1852, Part I. p. 05. Read Juue 10,1851). In esso si descriveva il funzionamento di una macchina ad aria calda che poteva funzionare in un ambito

di temperatura molto maggiore di una macchina a vapore. Questa proposta non ebbe alcun esito pratico ma vale la pena osservare che un analogo funzionamento è della macchina che Diesel realizzerà anni dopo(11).
Con gli sviluppi della termodinamica diventava indispensabile conoscere alcune grandezze con maggiore precisione, soprattutto in relazione al comportamento dei gas. Nel 1847 erano state pubblicate sulle Mémoires de l’Académie des Sciences, le Tavole di Henri Victor Regnault (1810 – 1878), Relation des expériences entreprises par ordre du Ministre des Travaux publics et sur la proposition de la Commission centrale des machines à vapeur, etc, in cui vi era la accuratissima

Regnault
determinazione dei calori specifici, dei calori latenti, delle densità, dei coefficienti di dilatazione, … di tutti gli elementi allora noti e di molti composti solidi, liquidi e gassosi. Nello studio della dilatazione dei gas per effetto dell’aumento di temperatura aveva calcolato in 1/273 il coefficiente di dilatazione dell’aria (per ogni grado centigrado di temperatura fornito), migliorando quello di Gay-Lussac fino ad allora accettato 1/266. Questi studi lo portarono a stabilire che la legge di Boyle è vera in prima approssimazione per i gas reali e che non è vero ciò che veniva comunemente accettato e che cioè i gas reali hanno tutti lo stesso coefficiente di dilatazione. Queste precise misure avevano in definitiva mostrato che, anche se ci si poteva ancora fidare in generale della legge di Boyle, la densità dell’aria aumentava più rapidamente, all’aumentare la pressione, di quanto questa legge permetteva di calcolare. Secondo i dati di Regnault l’aria doveva raffreddarsi leggeramente quando si espandeva uscendo da un piccolo foro, senza fare lavoro. Si doveva indagare con esperienze decisive su questo punto e fu Thomson, cosciente della estrema abilità di sperimentatore di Joule, che lo mise su questa strada nel 1852. L’esperienza sembrava semplice: misurare la temperatura dell’aria prima e dopo la sua espansione da un piccolo foro. Joule fece alcune prove qualitative e sembrò che tutto andasse nel senso indicato da Regnault. Si rese però conto che i dati ricavati su piccola scala non erano significativi, occorreva disporre di macchine a grande scala per avere la certezza dell’effetto. Progettò allora una macchina che provocava l’espansione desiderata tramite una macchina a vapore di 3 cavalli. I costi erano tali che da solo Joule non ce la fece (la fabbrica di birra stava per chiudere poiché le condizioni di salute del padre non erano buone) ma usufruì di un finanziamento della Royal Society. Restava l’inconveniente delle dimensioni al quale Joule fece fronte trasferendo tutti i macchinari dapprima alla birreria, e quindi, quando essa fu venduta (1854), alla sua casa dove dovette arrangiarsi con parte del macchinario posto all’aperto, visto che non entrava nel suo laboratorio. A questo punto interviene il racconto del fratello di Joule che ci informa che per alcuni mesi Joule mangiò di rado, e solo qualche panino. Era troppo indaffarato con quella macchina che richiedeva misure estremamente precise che avrebbero sofferto per il solo passaggio di una carrozza. Pertanto lavorò di notte. Questa collaborazione con Thomson sulle proprietà dei gas durò sette anni ed arrivò a stabilire l’effetto di raffreddamento dei gas quando le loro molecole, soggette ad una debole attrazione, si allontanano. Quando le molecole d’aria si separano per effetto dell’espansione, occorre un lavoro meccanico per vincere la piccola forza di attrazione che le tiene legate e questo lavoro meccanico richiesto comporta un assorbimento di calore e quindi un raffreddamento. Si tratta dell’effetto oggi noto come Effetto Joule-Thomson che è alla base della fabbricazione dell’aria liquida (procedimento di Linde) e dell’ottenimento di basse temperature. Mentre portava a termine questo gran lavoro, come effetto collaterale, scoprì e perfezionò il metodo di saldatura elettrica (1855) che oggi è comunemente in uso.

Il lavoro sull’effetto Joule-Thomson produsse varie ed articolate memorie piene di misure e di elaborazioni teoriche sviluppate con la grande abilità matematica di Thomson. La prima di queste memorie, On the Thermal Effects of Fluids in Motion, fu pubblicata nel 1853 sulle Philosophical Transactions of Royal Society (riporto di seguito tutta la prima pagina di tale lavoro perché in essa vi è un sunto di come si è arrivati a scrivere la memoria e cosa essa si propone).

Nel lavoro viene presentato l’apparato con il quale studieranno i fenomeni dell’espansione di un gas, senza lavoro, nel passaggio da un recipiente ad un altro attraverso un piccolo foro.

Macchina per studiare l’Effetto Joule-Thomson. La macchina a vapore della quale ho parlato nel testo funzionava per alimentare il pistone nel cilindro che compare a sinistra in basso.
L’ultima memoria della serie sullo stesso argomento e con il medesimo titolo, la quarta, sarà pubblicata sulla stessa rivista nel 1862.

Non è qui il caso di analizzare la serie di memorie che descrivono i lavori fatti dai due scienziati, ma solo ribadire che esse richiesero 7 anni di duro lavoro. Non è in alcun caso possibile sintetizzare in modo decente tale lavoro.
Terminato questo lavoro di grande impegno con Thomson, Joule iniziò nuovi studi, anch’essi richiedenti massima cura, relativi alla condensazione del vapore sulle superfici metalliche che poi ebbero importanti ricadute sulla costruzione dei condensatori nelle macchine a vapore. Nel 1861 Joule dovette fare un ulteriore trasloco del laboratorio e doveva sempre avere con sé quell’apparecchiatura molto ingombrante della quale ormai disponeva. Il laboratorio non era grande ed anche ora dovette sistemare la macchina a vapore fuori. Inoltre la cura delle misure richiedeva anche ora del lavoro notturno ma in questa nuova sistemazione il lavorare di notte all’aperto provocò l’irritazione dei vicini che ottennero che smettesse. Joule smise e per 10 anni non fece praticamente più nulla.
Nel 1871 pubblicò un lavoro che gli fu suggerito dalle avverse condizioni atmosferiche. Il gran freddo del 1870 aveva provocato varie fratture con conseguenti incidenti o avarie, nel materiale di ferro e di acciaio delle ferrovie. Si era sparsa la voce che fosse il freddo a provocare i danni suddetti e Joule dimostrò che così non era (vi fu anche una polemica perché gli fu obiettato che non si poteva dimostrare, come lui aveva fatto, con piccoli oggetti quanto accadeva a grande scala; fu l’unica occasione di una polemica che vide Joule rispondere in modo piccato).

Nel 1875 quello che era rimasto della famiglia Joule subì un grave tracollo finanziario tanto che il nostro grande fisico si ritrovò povero. Furono gli amici e gli estimatori che riuscirono a fargli ottenere una pensione annua di 200 sterline con la quale visse modestamente ma in modo confortevole per gli ultimi anni della sua vita. Le poche ricerche che fece gli furono finanziate dalla Royal Society in un piccolo laboratorio vicino alla nuova dimora che occupò dal 1877. Dopo una lunga malattia, si spense in quella casa nel 1888. Fu lì che il prof. Haldon Gee ritrovò i libretti di cui ho parlato all’inizio, contenenti una specie di diario di tutte le operazioni che Joule veniva facendo. Due anni prima di morire disse al fratello: “Ho fatto due o tre cosette, ma nulla da farci del chiasso“.

La tomba di Joule
NOTE
(1) Come curiosità di un certo interesse occorre ricordare che il fisico-chimico russo (ma nato in Svizzera), Germain Henri Hess (1802 – 1850), nel 1840, aveva pubblicato un lavoro, Recherches thermochimiques (Bulletin scientifique Académie impériale des sciences, Volume 8, p. 257-272, St. Petersburg, 1840), nel quale aveva ricavato una legge che prefigura la conservazione dell’energia e che oggi è un corollario di essa. La legge di Hess, riferita a reazioni chimiche, afferma che l’effetto termico a pressione costante è indipendente dagli stati intermedi attraverso i quali si evolve il sistema e dipende solo dal suo stato iniziale e finale.
(2) Il termine forza – kraft – era comunemente usato in Germania in luogo della parola energia che sarà introdotta da Rankine negli anni Sessanta dell’Ottocento. L’espressione per energia in uso in Francia era lavoro meccanico ed era stata introdotta da Coriolis e Poncelet intorno al 1825. E’ comunque chiarissimo nei suoi scritti che egli sta parlando di energia. Lo stesso Helmholtz, come vedremo, userà ancora la parola kraft in luogo di energia.
(3) Correnti parassite di Foucault. Questo fenomeno fu scoperto nel 1855 dal fisico francese Jean Bernard Léon Foucault (1819 – 1868) noto per il suo Pendolo per la misura della velocità della luce e per l’invenzione del giroscopio. La fenomenologia delle correnti di Foucault è che esse sono correnti indotte che si formano nei conduttori massicci sottoposti ad un campo magnetico variabile. Se si sottopone a tale campo un blocco di rame, esso si scalda molto di più che se la stessa quantità di rame fosse costituita da lamine sottili isolate tra loro.
Foucault
(4) L’effetto Peltier. A seguito delle scoperte di Volta, vi fu un’intensità di ricerche che ruotavano intorno alle catene aperte o chiuse di conduttori di prima classe. Il fisico tedescoThomas JohannSeebeck (1770 – 1831) scoprì un effetto che porta il suo nome (1821): in una catena aperta di tre conduttori di prima classe ad estremi uguali, la differenza di potenziale agli estremi non è nulla se le due saldature non sono alla stessa temperatura. Riferendoci alla figura, se si ha una catena aperta di rame, zinco, rame e le saldature C e D sono alla stessa temperatura, allora tra A e B non vi è differenza di potenziale. Ma scaldando una delle due saldature, tra A e B si crea differenza di potenziale, entro certi limiti tanto maggiore quanto maggiore è la differenza di temperatura tra C e D (con opportuni arrangiamenti, fatti da Macedonio Melloni, si riesce ad avere una sensibilità di un milionesimo di grado). Si noti comunque che tale effetto è piccolo, tanto che esso è utilizzato come termometro di estrema sensibilità (termocoppia). Con opportuni arrangiamenti, fatti da Macedonio Melloni, si riesce ad avere una sensibilità di un milionesimo di grado.
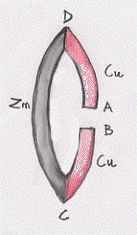
L’effetto, per certi aspetti, inverso dell’effetto Seebeck è l’effetto Peltier. Esso fu scoperto nel 1834 dallo studioso francese Jean Charles Athanase Peltier (1785 – 1845). Quando una corrente elettrica percorre un circuito aperto costituito da due conduttori saldati tra loro, a seconda della direzione della corrente una delle saldature si scalda e l’altra si raffredda. La quantità di calore generata o assorbita per unità di tempo è proporzionale all’intensità di corrente che circola nella saldatura.

Seebeck

Peltier
(5) Conti sulla potenza sviluppata da un cavallo li aveva fatti Watt per definire il suo cavallo-vapore (HP) in modo da poter vendere le macchine comunicando all’acquirente quanti cavalli veri una tale macchina andava a sostituire.
(6) Per determinare con esattezza l’equivalente meccanico del calore, occorre sottrarre al lavoro calcolato come peso per altezza che la massa compie ad ogni discesa, il lavoro fatto contro le resistenze passive esterne al calorimetro. Questo lavoro può essere misurato sperimentalmente, determinando per tentativi il peso minimo necessario per produrre la rotazione delle pulegge e del cilindro sconnesso dal mulinello, con una discesa dei pesi di moto uniforme. Questa è la condizione per avere il valore del lavoro uguale a quello resistente da sottrarre al lavoro complessivo. La relazione completa oggi si scrive così:
JQ = n(Mgh – ½Mv2 – mgh)
dove J è l’equivalente meccanico della caloria, n è il numero di volte che si ripete la caduta delle masse, M sono le masse in caduta, Mgh l’energia potenziale delle masse prima della caduta, mgh il lavoro resistente, ½Mv2 è l’energia cinetica che hanno le masse al momento di toccare il suolo.
(7) Il fisico inglese John Herapath (1790 – 1868), intorno al 1820 elaborò una teoria che fu pubblicata nelle memorie, On the physical properties of gases (Annals of Philosophy 56-60, On the Causes, Laws and Phenomena of Heat, Gases, Gravitation (Annals of Philosophy 9, 273-293, 1821); secondo tale teoria la pressione dei gas è proporzionale alla vis viva delle particelle che li costituiscono.
(8) Euler, nel Tentamen explicationis phaenomenorun aeris del 1729 aveva trovato che le temperature sono proporzionali al quadrato delle velocità e cioè alla vis viva.
(9) Il fisico francese Guillaume Amontons (1663 – 1705) trovò una legge secondo la quale in un gas la pressione aumenta linearmente con la temperatura (P aumenta circa di un 33% nel passare dal punto di gelo a quello di ebollizione) con la conseguenza che una sufficiente diminuzione di temperatura porterebbe allo sparire della pressione ed addirittura a renderla negativa, avendo l’intuizione quindi dello zero assoluto (in due memorie: Le Thermometre Réduit à Une Measure Fixe & Certaine, & les Moyen d’y Rapporter les Observations Faites Avec les Anciens Thermometres, e Remarques sur la Table des Degrés de Chaleur, pubblicate su Histoire et Mémoires de l’Académie Royale des Sciences, 50-56, e 202-212, 1703).
(10) Il conto che fa Joule è quello che ancora oggi si fa per ritrovare, ragionando microscopicamente la legge che macroscopicamente aveva trovato Boyle. Si può a questo proposito vedere il mio Atomi e molecole.
(11) Il motore Diesel è una macchina ad aria calda nella quale l’aria compressa nel cilindro viene ulteriormente riscaldata mediante la combustione del gasolio iniettato; la macchina di Joule prevedeva la compressione dell’aria in un recipiente esterno, quindi l’aria surriscaldata produceva lavoro meccanico all’espandersi nel cilindro dotato di pistone.
BIBLIOGRAFIA
(1) AA. VV. – Scienziati e Tecnologi dalle origini al 1875 – EST Mondadori 1975
(2) Emilio Segrè – Personaggi e scoperte nella fisica classica – EST Mondadori 1983
(3) Yehuda Elkana – La scoperta della conservazione dell’energia – Feltrinelli 1977
(4) Thomas S. Khun – La conservazione dell’energia come esempio di scoperta simultanea – in: Thomas S. Kuhn – La tensione essenziale – Einaudi 1985
(5) Wilhelm Ostwald – Les Grands Hommes – Flammarion, Paris 1912
(6) Enrico Bellone – Le leggi della termodinamica da Boyle a Boltzmann – Loescher 1978
(7) A. Baracca, A. Rossi – Materia ed energia – Feltrinelli 1978
(8) Mario Gliozzi – Storia della fisica – in: N. Abbagnano (diretta da) – Storia delle Scienze, UTET 1965
(9) René Taton (diretta da) – Storia generale delle scienze – Casini 1965
(10) Friedrich Klemm – Storia della tecnica – Feltrinelli 1966
(11) J.G. Crowter – British Scientists of the Nineteenth Century – Hesperides Press, 1935
(12) The Scientific papers of James Prescott Joule. Volume 1 / Published by the Physical society of London Taylor and Francis. London – 1884-1887
(13) The scientific papers of James Prescott Joule. Volume 2, Joint scientific papers / Published by the Physical society of London Taylor and Francis. London – 1884-1887
(14) C. Truesdell – Essay in the History of Mechanics – Springer-Verlag 1968
Categorie:Senza categoria
Rispondi