Roberto Renzetti
I PRIMI ANNI
Ludwig Boltzmann nacque a Vienna nel 1844. Vienna era la capitale dell’Impero austro-ungarico, una città ricca e piena di curiosità intellettuali oltre che produttrice di cultura al massimo livello. Inoltre Vienna faceva a pieno titolo parte della grande cultura tedesca che, a partire dall’unificazione del 1870 della Germania dopo che la Prussia nel 1866 aveva sconfitto l’Impero asburgico e chiuso con la sua egemonia, poté dispiegarsi in modo impressionante. Molti scienziati e tutti di livello elevatissimo nacquero o si formarono in Austria particolarmente a cavallo dell’Ottocento e Novecento. Tra questi appunto il grande fisico teorico Boltzmann.
Suo padre era un impiegato dell’Impero che si occupava della riscossione delle imposte e che, proprio per il suo lavoro, era stato inviato a Linz, dove Ludwig passò parte della sua giovinezza. Sua madre era Katharina Pauernfeind, figlia di un commerciante della media borghesia, di origine tedesca come del resto lo era il nonno di Ludwig. Vi è poco da raccontare della sua giovinezza: studiò a Linz ed ai 15 anni perse il padre. Dopo aver concluso gli studi superiori passò all’Università di Vienna, nell’Istituto creato da Christian Doppler nel 1850, dove nel 1863 si

Doppler
iscrisse a Fisica dove ebbe dei professori di grande livello, tra cui Joseph Loschmidt (1821-1895), tra i primi a dare valori numerici a grandezze molecolari, e Josef Stefan (1835-1893), famoso per i suoi studi sulla radiazione. Quest’ultimo
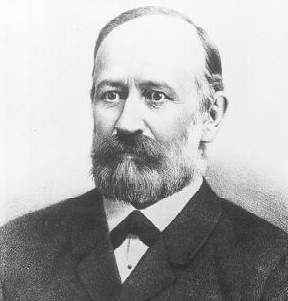
Stefan
esercitò molta influenza su di lui ed i suoi studi facendogli da relatore alla tersi di laurea. Stefan, tra l’altro, avviò Boltzmann ad un argomento avanzatissimo per l’epoca, la teoria cinetica dei gas, ed alla conoscenza dei lavori di Maxwell che all’epoca era poco noto nel centro Europa e per farlo dovette imparare l’inglese, una lingua che gli fu poi molto utile per i suoi rapporti con gli scienziati britannici e statunitensi. Si laureò nel 1866 e nel 1867, dopo aver ottenuto la libera docenza, passò ad essere suo assistente.

Boltzmann a 24 anni
TENTATIVI DI TROVARE IL SIGNIFICATO MECCANICO DEL SECONDO PRINCIPIO
Il primo lavoro di Boltzmann fu la sua tesi, Über die Bewegung der Elektrizität in krummen Flächen (Sul movimento dell’elettricità su superfici curve, Wien. Ber. 52. S. 214-221. 1865.). Subito dopo scrisse il suo primo vero lavoro che si occupava di teoria cinetica, Über die Mechanische Bedeutung des Zweiten Hauptsatzes der Wärmetheorie (Sul significato meccanico del secondo principio della termodinamica, Wiener Berichte, 53, 195–220; 1866). Già dal titolo si può osservare una grande differenza rispetto ai lavori termodinamici di Maxwell. Mentre Maxwell si muoveva mantenendo la termodinamica al margine della sua ricerca che era concentrata alla comprensione microscopica del moto molecolare e affrontava la termodinamica solo per rilevarne le differenze con la fisica determinista, qui l’attenzione tornava al Secondo Principio e la ricerca di Boltzmann resterà sempre su di esso come egli stesso diceva proprio in apertura di questa memoria: Scopo di questo articolo è di fornire una dimostrazione completamente generale, puramente analitica, della seconda legge della termodinamica e di scoprire il teorema di meccanica che le corrisponde. Mentre infatti il Primo Principio era immediatamente riconducibile al principio di conservazione dell’energia, abitualmente considerato come capitolo della meccanica, niente di simile accadeva per il Secondo Principio. Boltzmann cercava quindi una connessione tra Secondo Principio nella formulazione di Clausius e qualche teorema di meccanica. Particolarmente idoneo a questo ruolo sembrava essere il famoso Principio di Minima Azione di Maupertuis (diventato un teorema di meccanica razionale che lo generalizzava) che nel 1867 venne indicato da Peter Guthrie Tait e William Thomson come un’utile guida nella ricerca cinetica per descrivere l’evoluzione di un sistema di punti materiali che si muovesse
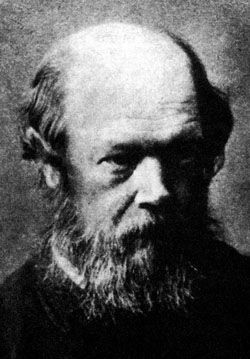
Tait
liberamente. Se si vuole basare la termodinamica su una teoria cinetica, occorre essere capaci di scrivere la seconda legge in termini cinetici in modo che l’irreversibilità discenda direttamente dalla meccanica che però risulta reversibile. Egli tentava di tradurre in termini meccanici il lavoro di Clausius del 1865 (Su alcune differenti Formulazioni delle Equazioni fondamentali della Teoria meccanica del Calore, Annalen der Physik 125; 353-400
Ciò che caratterizza il sistema delle molecole in moto in un gas è la grande irregolarità dei moti che si realizzano al suo interno, con molecole che allo stesso tempo si muovono con le più differenti velocità in tutte le direzioni. Boltzmann iniziava a trattare la questione con il dare un’interpretazione meccanica della temperatura assoluta delle molecole (media nel tempo dell’energia cinetica media delle molecole stesse) attraverso il concetto di equilibrio termico, con l’osservare cioè che a tale equilibrio sia le energie cinetiche che le temperature delle molecole non subiscono mediamente degli scambi. Egli elaborava la discussione mediante un modello di gas costituito da molte molecole tra le quali sceglie un sottosistema costituito da due molecole del quale studia il comportamento assumendo che esso sia in equilibrio con l’intero sistema. Tale condizione di equilibrio richiede che il sottosistema scambi energia cinetica con il resto delle molecole modificando in tal modo il loro stato ma in modo tale che il valor medio dell’energia cinetica scambiata in un intervallo finito di tempo sia certamente nullo (deve accadere ad esempio che il valor medio dell’energia cinetica si mantenga costante). Resta comunque il problema del calcolo degli scambi di energia cinetica e quantità di moto tra sistema e sottosistema per l’impossibilità di applicare le leggi della meccanica degli urti elastici a tale insieme di moltissimi corpi. La difficoltà viene superata assumendo che, dopo un certo tempo (t2 – t1) e relativamente ad una data direzione, la somma delle energie cinetiche dei due atomi del sottosistema, così come il moto del loro centro di gravità, sarà di nuovo lo stesso. Poiché l’energia totale e la quantità di moto del sottosistema cambiano continuamente, per confrontare due differenti stati di esso occorrerebbero dati del sistema praticamente impossibili da conoscere. L’ipotesi di Boltzmann è che nel corso della sua evoluzione il sistema, caratterizzato da collisioni elastiche, dovrà passare attraverso due stati caratterizzati dalla stessa energia e quantità di moto totali. Mediante l’ipotesi dell’equiprobabilità in una data direzione del moto e considerando la media dell’equazione del moto medesimo, Boltzmann generalizza questo risultato agli altri stati. Da sottolineare che in tutto il ragionamento non si dice nulla su quanto è grande l’intervallo di tempo ed inoltre Boltzmann non fornisce alcun argomento a sostegno dell’esistenza degli stati supposti che dovrebbero in un dato istante avere stesse energie e quantità di moto. Tutto è basato sul fatto che tale evento non è impossibile e se tali eventi potrebbero accadere allora accadranno. Siamo in una zona oscura del pensiero di Boltzmann che sarà illuminata dalle successive memorie. C’è comunque da osservare che vi sono qui i primi elementi dell’ipotesi ergodica.
E’ utile sottolineare che Boltzmann, nelle sue elaborazioni,

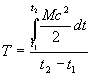
(nella prima espressione, quella che fornisce l’entropia di un corpo, la sommatoria è estesa a tutte le molecole mentre e t1 e t2 sono due istanti di tempo successivi).
Nel 1867 fu pubblicato il lavoro di Maxwell On the Dynamical Theory of Gases, (Sulla teoria dinamica dei gas, Philosophical Transaction della Royal Society, CLVII, 1867, pp. 49-88). Boltzmann la lesse con grande interesse e l’anno successivo (1868), dopo aver abbandonato l’idea di costruire una connessione tra Secondo Principio e Principio di Minima Azione(0), pubblicò il suo secondo lavoro su questioni di termodinamica, Studien über das Gleichgewicht der lebendigen Kraft zwischen bewegten materiellen Punkten, (Studio dell’equilibrio della forza viva fra punti materiali in moto, Wiener Berichte, 58, 517-560). Si trattava della prima di una serie di sue ponderose memorie incentrate sul dare il cercato significato cinetico al Secondo Principio(1). Boltzmann elaborava uno studio che può essere considerato come la generalizzazione dei risultati di Maxwell poiché estese la funzione di distribuzione delle velocità molecolari di Maxwell al caso di gas poliatomici e soggetti ad un campo statico di forze esterne (come il potenziale gravitazionale) e tra le medesime molecole. Restava il problema principale, quello annunciato nel titolo della memoria: la dimostrazione che un gas tende spontaneamente ad uno stato di equilibrio termico, problema alla base dell’irreversibilità dei fenomeni naturali. Tale dimostrazione era ritenuta cruciale anche da Maxwell il quale però si accontentò di aver mostrato che il Secondo Principio ha una validità solo probabilistica inoltre Maxwell non andò oltre nei suoi studi perché era convinto che vi fosse un’unica distribuzione che si mantenesse stabile, quella che aveva trovato. Diverso era l’atteggiamento di Boltzmann che cercava dati quantitativi precisi.
Già in apertura della sua memoria Boltzmann osservava che la matematica di cui si disponeva era in grado di studiare trasformazioni da uno stato all’altro di sistemi completamente definiti fisicamente e questo non era certo il caso della teoria cinetica del calore in cui il gigantesco numero di molecole rendeva impossibile una definizione completa del sistema anche perché gli stessi fenomeni della termodinamica dipendono da parametri generali cioè macroscopici e non certo dalla conoscenza dei singoli componenti, le molecole, del sistema delle quali non siamo in grado di scrivere, componente per componente, l’equazione differenziale del moto che lo rappresenta. Lo stato delle conoscenze attuali non ci permette di scrivere e risolvere ciascuna singola equazione perché conosciamo il comportamento del sistema solo attraverso i valori medi delle grandezze che caratterizzano i componenti che lo costituiscono.
Bolzmann superò questa difficoltà tralasciando le singole equazioni differenziali del moto, che sono in grado di darci informazioni solo in un intervallo infinitesimo della sua evoluzione, ed introducendo le equazioni integrali (metodi variazionali) capaci di fornire informazioni su una estesa traiettoria percorsa da un punto materiale a patto di conoscerne l’inizio e la fine. La funzione di distribuzione che trovò sostituiva all’esponenziale che aveva trovato Maxwell un altro esponenziale dipendente dall’energia delle molecole del sistema. Indicando con E tale energia , l’esponenziale era e -E/kT. E poiché tale esponenziale compariva nella funzione di distribuzione, esso determinava la probabilità relativa di avere un singolo stato molecolare con energia E. Da notare una proprietà di tale esponenziale: al crescere dell’energia esso tende asintoticamente a zero rendendo quindi sempre minore la probabilità di trovare molecole sulle quali agiscono forze esterne. Tali conclusioni non furono però stabilite se non in casi particolari e Boltzmann si aiutò sviluppando una teoria cinetica dell’equilibrio ed introducendo l’ipotesi delle uguali probabilità.
E’ da notare che mentre la funzione di distribuzione per Maxwell rappresenta una densità di probabilità e cioè ci dice quante molecole in un dato volume dV ed in un tempo t hanno velocità comprese tra v e v + dv, essa per Boltzmann rappresenta l’intervallo di tempo in cui la velocità di una molecola qualunque si situa all’interno di quell’intervallo di velocità. Se cioè disponiamo di un sistema di moltissime molecole in un dato istante ed in qualche modo siamo in grado di misurare la frazione di molecole in un dato spazio che abbiano tali velocità otterremmo lo stesso risultato che si avrebbe se aspettassimo un tempo sufficientemente lungo e contassimo quante molecole sono passate per quello spazio con le velocità richieste diviso per la media fatta sul tempo del numero totale di molecole in quel punto. Non è banale accettare l’una o l’altra visione della funzione di distribuzione e la cosa farà molto discutere per molti anni. La visione di Boltzmann fu battezzata come ipotesi ergodica(2) da Paul e Tatyana Ehrenfest nel 1911 in Begriffliche Grundlagen der statistischen Auffassung in der Mechanik, (I fondamenti concettuali dell’approccio statistico alla meccanica, Enzyklopädie der Mathematischen Wissenschaften; Bd. IV, Leipzig, 1911).
ENTROPIA E PROBABILITA’
Nel 1869, all’età di 25 anni, Boltzmann vinse la cattedra di fisica-matematica all’Università di Graz ma restarono per lui un ricordo importante i due anni di lavoro con Stefan per la grande ed importante pratica di laboratorio che fece. Anche se, come accennato, Boltzmann era un fisico teorico, servirono molto alla sua formazione i lavori di laboratorio dove, sotto la guida di Stefan, divenne un abilissimo sperimentatore (si occupò di misure che cercavano di stabilire la relazione tra indice di rifrazione e costante dielettrica di varie sostanze) come Ernst Mach (1838-1916), anch’egli eccellente sperimentatore e non certo suo

Mach
amico, ebbe a ricordare spesso. Altro aspetto importante della sua formazione come assistente fu il vivere in un ambiente dominato da atomisti che lo coinvolse almeno in un primo periodo. Questa comune posizione iniziale lo avvicinò particolarmente a Loschmidt del quale divenne amico e lo restò per tutta la vita

Loschmidt
anche se con posizioni filosofiche che si andarono differenziando. A Graz dove ebbe come allievi Svante Arrhenius e Walther Nernst (colui che formulò il terzo

Arrhenius
principio della termodinamica) restò fino al 1873 quando ottenne una cattedra di fisica all’Università di Vienna dove resterà fino al 1876.

Nerst
Sempre nel 1869 Boltzmann passò un periodo di studio ad Heidelberg dove lavorò con Robert Bunsen. Successivamente, nel 1870 e 1871, passò alcuni mesi a Berlino, sempre per motivi di studio, dove lavorò ed ebbi scambi estremamente

Bunsen
proficui con Hermann von Helmholtz e Gustav Kirchhoff. Nel 1872 conobbe

Kirchhoff
Henriette von Aigentler una giovane che aspirava fare l’insegnante di matematica e fisica e che quindi chiedeva l’ammissione all’Università di Graz. Ma a quel tempo l’Università nell’Impero era chiusa alle donne e Boltzmann consigliò la giovane di fare ricorso sulla sua non ammissione e tale ricorso ebbe successo. Con questa donna Boltzmann si sposò nel 1876 in un matrimonio felice allietato da 5 figli.

Boltzmann con sua moglie a 31 anni
Questi anni furono molto proficui per i lavori di Boltzmann che continuavano sulla strada delle ricerca del significato meccanico del Secondo Principio. Anche le sue memorie continuavano ad essere voluminose e scritte con moltissimi dettagli e particolarmente quella del 1872 che ora discuterò, Weitere Studien über das Wärmegleichgewicht unter Gasmolekülen (Un altro studio sull’equilibrio termico tra molecole di gas, Wien. Ber. 66. S. 275-370, 1872). Tale memoria è di ben 87 pagine e contiene due delle scoperte più importanti di Boltzmann, il teorema H e l’equazione del trasporto, oggi nota come equazione di Boltzmann. In essa egli fornì la prima derivazione dell’aumento di entropia nei processi irreversibili utilizzando leggi meccaniche e probabilistiche e dimostrò che la legge di distribuzione delle velocità di Maxwell determina lo stato di equilibrio di un gas qualunque sia lo stato iniziale del gas esso, al limite, deve sempre approssimarsi alla distribuzione trovata da Maxwell. Boltzmann quindi riuscì a calcolare l’evoluzione di un sistema di particelle a cui competeva inizialmente una qualsivoglia distribuzione di velocità, trovando che questo sistema tende ad assumere la distribuzione di velocità di Maxwell, a seguito degli urti successivi delle particelle tra loro. La distribuzione di Maxwell tende quindi ad assumere il significato di distribuzione più probabile (all’equilibrio) verso cui tendono tutte le altre possibili distribuzioni (lontane comunque dall’equilibrio). Questo fatto è di grande portata poiché comporta l’affermazione che in natura si tende in modo irreversibile verso l’equilibrio e, contemporaneamente, il ritrovare su questa strada, di nuovo, l’irreversibilità insita nel secondo principio. Scriveva Boltzmann:
La teoria meccanica del calore ipotizza che le molecole di un gas non siano in quiete, ma siano invece in movimento vivace. Pertanto, anche se il corpo non modifica il proprio stato, le sue molecole individuali subiscono continue modificazioni dei loro stati di movimento, e le varie molecole assumono molte posizioni diverse le une rispetto alle altre. Il fatto che, ciò nonostante, noi osserviamo nei corpi caldi delle leggi di comportamento del tutto definite, deve essere attribuito alla circostanza per cui gli eventi più casuali danno lo stesso valore medio quando si realizzano nelle medesime proporzioni. Infatti le molecole che costituiscono i corpi sono talmente numerose, ed il loro moto è così veloce, che noi non percepiamo altro se non dei valori medi. Si potrebbe confrontare la regolarità di questi valori medi con la sorprendente costanza dei numeri medi forniti dalle statistiche, numeri che sono tratti da processi ciascuno dei quali è determinato da una interazione completamente non prevedibile con molti altri fattori. Le molecole sono simili a molti individui che siano in stati di movimento i più diversi: il fatto che le proprietà dei gas rimangano invariate dipende unicamente dal fatto che il numero di molecole le quali hanno, in media, uno stato di moto particolare, è una costante. La determinazione dei valori medi è compito della teoria delle probabilità. Pertanto, i problemi di teoria meccanica del calore sono anche problemi di teoria delle probabilità. Sarebbe tuttavia sbagliato credere che, in conseguenza di ciò, la teoria meccanica del calore sia colpita da una qualche incertezza derivante dall’uso dei principi della teoria della probabilità. Non si deve confondere una legge non completamente nota, la cui validità è quindi soggetta a dubbi, con una legge completamente nota del calcolo delle probabilità; quest’ultima, come accade con i risultati di ogni altro calcolo, è una conseguenza necessaria di premesse date, e viene confermata, nei limiti entro i quali queste ultime sono corrette, dall’esperimento, a condizione che siano state fatte osservazioni sufficientemente numerose: e ciò accade sempre nel caso della teoria meccanica del calore, a causa del numero enorme delle molecole che sono implicate.
Per illustrare alcune conclusioni di grande interesse che Boltzmann trova in questa memoria, seguirò un suo lavoro semplificato e successivo, Vorlesungen über Gastheorie (Lectures on Gas Theorie, Lipsia 1896 e 1898), in gran parte ripreso da T. Kuhn nel suo Black-Body Theory and the Quantum Discontinuity 1894-1912.

Egli iniziò considerando un recipiente pieno di un gas costituito da molecole identiche sferiche e perfettamente elastiche. Introdusse poi una funzione f della velocità e del tempo f(u,v,w,t).dudvdwdt, successivamente chiamata per semplicità f.dω (con dω infinitesimo ma contenente un numero molto grande di molecole), rappresentante il numero di molecole per unità di volume che all’istante t hanno componenti della velocità comprese tra u e u + du, v e v + dv, w e w + dw. Tale funzione f(u,v,w,t), descrive la distribuzione di velocità delle molecole nel recipiente in ogni istante. A questo punto Boltzmann, per ragioni di semplicità, introduce due nuove ipotesi che successivamente eliminerà: le molecole non subiscono nessuna forza esterna e le pareti del recipiente che le contiene sono lisce ed elastiche. Egli scriveva:
il gas è sottoposto alle medesime condizioni in ogni punto del recipiente. Da ciò segue che se all’inizio di un certo intervallo temporale il numero di molecole per unità di volume che hanno componenti di velocità comprese tra il limiti [ora dati] è, in media, lo stesso in qualunque luogo occupato dal gas […], e la stessa cosa avverrà in qualunque istante futuro.
Fatte queste premesse, Boltzmann iniziava a studiare un urto tra due molecole(una nel volume delle velocità dω e l’altra nel volume vicino delle velocità dω1) considerate come sfere perfettamente elastiche di diametro σ. Per definire meglio l’urto ipotizzava che la retta che unisce i centri delle due molecole nell’istante della collisione fosse localizzata in un cono infinitesimo di angolo solido dλ e tale urto lo chiamava collisione del tipo specificato. L’obiettivo seguente era quello di determinare il numero dν di urti del tipo specificato che hanno luogo per unità di volume durante un intervallo di tempo dt. Per fare ciò Boltzmann utilizzò una tecnica utilizzata da Clausius per ricavare il cammino libero medio ed oggi di uso comune. Immaginiamo una sfera mobile di diametro 2σ in moto con velocità g uguale alla velocità relativa di due molecole contenute rispettivamente in dω e dω1. Qualunque urto del tipo specificato è equivalente ad un incontro tra la sfera ed un punto fisso, sempre che tale punto fisso giaccia sull’elemento di superficie intercettato dal cono dλ sulla sfera. Man mano che la sfera si muove nel tempo dt, questo elemento di superficie descrive un cilindro di volume σ2.dλ.g.cosθ.dt dove θ è l’angolo tra la direzione del movimento della sfera e l’asse del cono (-π/2 < θ < π/2). Se la sfera rappresenta una molecola che si trova inizialmente in dω, la densità di punti con i quali effettuare un urto del tipo specificato è f1.dω, ed il numero totale di tali collisioni nel tempo dt sarà f1.dω1.σ2.dλ.cosθ.dt, con f1che è un modo più semplice, che userò anche in seguito, di scrivere f(u1,v1,w1,t1). Dato che inoltre le molecole in dω hanno una densità f.dω e che ciascuna di esse può effettuare un urto del tipo specificato, il numero totale di tali collisioni che avvengono in un volume unitario nel tempo dt (il numero medio di collisioni come diremmo oggi e come non dice Boltzmann) sarà:
(1) dν = f.dω.f1.dω1.σ2.dλ.cosθ.dt
Avendo stabilito il numero delle collisioni, Boltzmann utilizzava le leggi della meccanica per determinare le celle delle velocità, dω’ e dω1‘, in cui si trovavano dopo l’urto le molecole che prima si trovavano in dωe dω1. Queste celle così createsi hanno, come egli dimostrava, due proprietà importanti. La prima è che dω’.dω1‘ = dω.dω1 e la seconda è che una collisione tra molecole che si trovano ora in dω’ e dω1‘ riporterà queste molecole nelle celle originali, dωedω1. Boltzmann confrontava questi urti da lui chiamati collisioni del tipo inverso con quelli che si erano originati tra dω e dω1. La caratteristica di questi urti (del tipo specificato) è quella di sottrarre molecole da dω e dω1 riducendo così i valori di f ed f1. Gli urti inversi, invece, restituiscono molecole a dω e dω1 aumentando in tal modo i corrispondenti valori di f ed f1. Ambedue i tipi di urti avvengono nel gas in ogni istante ed il numero delle molecole che entrano in dω e dω1ed escono da questi volumi di velocità possono essere calcolati con l’equazione (1). Mettendo insieme questi risultati con altri che aveva già ricavato, Boltzmann arrivava a determinare la formula che stabilisce il modo con cui varia la sua funzione di distribuzione:
(2)
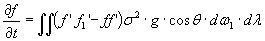
e questo è uno dei primi risultati di notevole importanza che Boltzmann aveva trovato. Si tratta di un caso particolare dell’equazione di Boltzmann che egli applica immediatamente alla dimostrazione che la distribuzione delle velocità di Maxwell è l’unica possibile. Non seguirò tutti i complessi passaggi (anche nella versione semplificata che sto seguendo) che portarono Boltzmann alle sue conclusioni ma darò solo i risultati principali.
Egli iniziava a definire una funzione H(t)(3) mediante l’equazione:
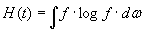
(3)
Passava quindi a dimostrare la seguente uguaglianza:

(4)
Nell’espressione che è sotto segno di integrale, le due quantità che sono tra parentesi o sono ambedue positive o ambedue negative o ambedue nulle in modo che risulta: dH/dt ≤ 0, con l’osservazione che il segno uguale si realizza solo quando f’f1‘ = ff1, condizione che è completamente realizzata quando la funzione di distribuzione era quella di Maxwell in quanto essa rappresenta la stazionarietà del sistema. In definitiva l’equazione (4) dice che la H, definita dalla (3), può solo e sempre diminuire (arrivando ancora una volta alla distribuzione di Maxwell) e rappresenta il teorema H di Boltzmann. A tale teorema Boltzmann assegnava il significato che aveva annunciato: una distribuzione iniziale e completamente arbitraria di un gas subisce varie trasformazioni fino che il suo stato finale era la distribuzione di Maxwell in corrispondenza della quale H era costante. Lo stesso Boltzmann, nell’articolo del 1872, diceva:
E’ così dimostrato in modo rigoroso che, quale che sia la distribuzione iniziale dell’energia cinetica, essa, nel corso di un tempo molto lungo, deve sempre e necessariamente tendere a quella trovata da Maxwell.
e perfezionava quest’affermazione con quanto scriveva nella Lectures on Gas Theorie del 1896/1898:
Abbiamo dimostrato che la grandezza che abbiamo chiamato H può solo diminuire, in modo che la distribuzione delle velocità deve necessariamente avvicinarsi sempre più a quella di Maxwell.
A questo proposito Bellone dice:
La prova, commentava Boltzmann, era di per se stessa fondata su un «artificio matematico», ma riceveva subito un significato qualora il teorema su H fosse applicato nel campo della fisica dei gas. La funzione H era, infatti, proporzionale all’entropia cambiata di segno: a una diminuzione di H corrispondeva quindi un aumento di entropia. Pertanto Boltzmann concludeva di aver «preparato la via per una prova analitica della seconda legge [della termodinamica] secondo modalità completamente diverse da quelle precedentemente esplorate», e di aver dato la prova matematica della tendenza osservabile nei «processi irreversibili, che sono gli unici che si verificano in natura».
Nel 1872 Boltzmann scrisse a sua madre, che si trovava a Vienna, dicendole che aveva letto il suo teorema alla Berliner Physikalischen Gesellschaft (Società Fisica di Berlino) ma che difficilmente vi era stato qualcuno che lo avesse seguito, a parte Helmholtz con cui si sviluppò un’interessante discussione. Non sorprende perché il teorema H è la prima esplicita espressione probabilistica che sarà presto associata all’entropia di un gas ideale.
Molti contemporanei di Boltzmann non solo non capivano ciò che si discuteva ma non erano addirittura in grado di accettare l’abbandono del determinismo. Si trattava di un vero sconvolgimento delle basi concettuali, almeno quelle dominanti, della fisica. A tale proposito commenta Bellone:
La teoria di Boltzmann e il teorema su H approdavano dunque a un esito sorprendente: da un lato, c’erano sistemi di corpuscoli che obbedivano alle leggi della meccanica e che, pertanto, non potevano in alcun modo violare la simmetria rispetto al tempo che era intrinseca a quelle leggi, mentre, dall’altro lato, quegli stessi sistemi esibivano una tendenza privilegiata verso la collocazione su stati “finali” che spezzava la simmetria in quanto introduceva nel mondo molecolare una freccia del tempo.
Com’era possibile un fatto del genere? In apertura dello scritto del 1872 Boltzmann aveva dichiarato che la soluzione matematica dei problemi molecolari richiedeva la valutazione di valori medi su grandissimi numeri di eventi, e che, pertanto, «i problemi della teoria meccanica del calore sono anche problemi di teoria della probabilità. Nel porre questa correlazione fra problemi di meccanica analitica e problemi di natura probabilistica Boltzmann cercava di fondare la teoria dei gas su una miscela di proposizioni i cui criteri di verità appartenevano a due assetti teorici distinti. Quali garanzie esistevano a proposito del tipo di conoscenza che era inferibile da questa miscela? Molti scienziati, in quegli anni, erano inclini a pensare che l’impiego di nozioni probabilistiche non fornisse un sapere rigoroso come quello che caratterizzava le conoscenze acquisibili nell’ ambito della teoria matematica del moto.
La parte finale della memoria serviva a Boltzmann a trovare quale relazione c’era tra la sua H e l’entropia S proprio per tornare al problema dal quale era mosso. La funzione H aveva il significato meccanico che occorreva legare all’entropia che era la funzione caratterizzante il Secondo Principio. Dopo aver calcolato H per l’intero gas in un contenitore e non più per un suo volume unitario, dimostrava un teorema di enorme importanza che legava tra loro proprio H ed S. Quando H nelle sue evoluzioni ∂f/∂t ha raggiunto il suo valore minimo o di equilibrio Hmin, essa può differire dall’entropia del gas (cambiata di segno) solo per una costante additiva arbitraria. E ciò si può scrivere:

(5)
dove Δ è presa lungo un cammino reversibile con il gas che si mantiene in equilibrio. In definitiva, mediante premesse meccaniche e statistiche, Boltzmann aveva derivato il Secondo Principio. E l’espressione che compare nella memoria del 1872 è la (5) senza quel segno meno, espressione che sarà successivamente corretta dallo stesso Boltzmann.
E’ utile dare a questo punto almeno un cenno di una ipotesi matematica che Boltzmann avanza in questa memoria e che avrà a che vedere (ma solo come dato esteriore) con i quanti di energia che introdurrà Planck 28 anni dopo. Ad un certo punto della memoria, Boltzmann diceva che vi era uno strumento matematico che avrebbe fatto meglio capire la questione. Riassume bene questo passo Bellone:
Secondo Boltzmann esisteva una tecnica matematica il cui impiego rendeva «più chiara» l’intera teoria sino ad allora sviluppata a proposito della grandezza f(x,t), dove l’energia x variava con continuità. Nulla vietava infatti di introdurre una congettura speciale, da concepire come un puro e semplice «artificio per aiutarci nel calcolo dei processi fisici»: si doveva supporre che una molecola fosse in grado di assumere solo un certo numero p di energie, ciascuna delle quali era un multiplo intero di una certa quantità energetica ε:
ε, 2ε, 3ε, 4ε, … ,pε.
In questo modo non si dovevano più studiare enti matematici come f(x,t), ma altri enti come f(ε,t), f(2ε,t) , … ,f(pε,t), ciascuno dei quali dipendeva soltanto dalla variabile tempo. La maggior chiarezza consisteva allora in ciò: quando si analizzava il comportamento di f(x,t) entrava in gioco l’equazione differenziale alle derivate parziali ∂f/∂t, mentre ora si passava a un sistema di p equazioni differenziali ordinarie nelle p incognite f(jε,t).
Boltzmann faceva risalire questa tecnica a un saggio che Lagrange aveva pubblicato nel lontano 1759 e ad applicazioni già eseguite da Stefan e da Riemann. Lagrange aveva studiato il classico problema della corda vibrante (e della newtoniana “fibra sonora”) rappresentando una corda come un insieme di m masse puntiformi governate da un sistema di equazioni differenziali, analizzando il caso in cui m diventava infinito e le masse diventavano infinitamente piccole, e suggerendo che in tal modo si apriva la strada per lo studio di un sistema qualunque di corpi tra loro eguali e interagenti, nonché per la determinazione del moto di «un’infinità di punti mobili» dopo una perturbazione qualsiasi del loro stato di equilibrio.
L’utilizzazione boltzmanniana di questa tecnica portava, nel 1872, a ripercorrere, entro i confini di un modello discreto per l’energia, i temi centrali di una fisica molecolare dove l’energia cinetica x era usualmente trattata come una variabile continua. È degno d’interesse notare che la tematica dei quanti non suscitò scalpore. Essa fu citata e discussa da alcuni fisici, dopo essere stata ripresa e ampliata dallo stesso Boltzmann nel 1877, senza però far nascere insanabili contraddizioni a proposito di energie che variavano in modo discontinuo.
L’energia era qui pensata come se potesse essere trattata da variabile discreta e non continua. Conseguenza di ciò era che l’equazione di Boltzmann poteva essere sostituita da un insieme di equazioni differenziali che oggi definiamo stocastiche e non lineari. Su questo problema Boltzmann tornerà con maggiori dettagli nella sua memoria del 1877.

CRITICHE AL LAVORO DI BOLTZMANN
A partire dal 1875 iniziarono critiche molto dure a ciò che aveva ricavato Boltzmann nella sua memoria del 1872. Non erano critiche relative agli strumenti matematici utilizzati ma proprio alle implicazioni che derivavano dal trattare l’irreversibilità con procedimenti meccanici e probabilistici. In linea di massima tali obiezioni furono di due tipi: quella proposta da Loschmidt che vedremo tra un poco e quella avanzata da Zermelo che vedremo più avanti perché fu formulata nel 1896. Ora però occorre soffermarsi un poco su una obiezione d’altro tipo che riguarda piuttosto un modo diverso, tra i vari possibili, di intendere la conoscenza e quindi la fisica. Su questo, un anno dopo il lavoro di Boltzmann, scrisse un articolo Maxwell, A discourse on molecules (Phil. Mag., 46, 1873). Leggiamo gli argomenti di Maxwell:
Sino a che trattiamo di due sole molecole e disponiamo di tutti i dati, possiamo calcolare il risultato di una loro collisione: ma quando abbiamo a che fare con milioni di molecole, ciascuna delle quali subisce milioni di collisioni al secondo, la complessità del problema è tale che, apparentemente, essa stessa ci chiude ogni speranza di giungere ad una soluzione legittima.
I moderni atomisti hanno allora adottato un metodo che è, a mio avviso, completamente nuovo nel settore della fisica matematica, anche se è stato a lungo usato nel settore della statistica. Quando […] si ha a che fare con un rapporto sul censo o su ogni altro documento che contiene i dati numerici della scienza economica e sociale, si comincia con il distribuire l’intera popolazione in gruppi, a seconda dell’età, dell’imposta sul reddito, dell’educazione, della fede religiosa o delle convinzioni criminali. Il numero degli individui è troppo grande per permettere di tracciare, per ciascuno di essi, la sua storia individuale: ed allora, al fine di ridurre l’impresa entro limiti umani, [gli studiosi] concentrano la propria attenzione Su un piccolo numero di gruppi artificiali. Il dato primario a partire dal quale essi lavorano è costituito dal numero variabile di individui entro ciascun gruppo, e non dallo stato variabile di ciascun individuo.
Questo non è, naturalmente, l’unico metodo per studiare la natura umana. Possiamo osservare la condotta di un singolo uomo e confrontarla con quella che il carattere precedentemente dimostrato e le circostanze attuali porterebbero a prevedere sulla base della miglior teoria esistente. Coloro che praticano questo metodo tentano di migliorare la loro conoscenza degli elementi della natura umana in modo analogo a quello seguito da un astronomo che corregge gli elementi di un pianeta confrontando la sua posizione reale con quella dedotta dagli elementi disponibili. Lo studio della natura umana, così come viene eseguito da famigliari e da maestri di scuola, da storici e da uomini di stato, deve pertanto essere ben distinto da quello che viene portato avanti da archivisti e da compilatori di tabelle, nonché da quegli statisti che ripongono ogni fiducia nelle cifre e nei diagrammi. L’un metodo può essere chiamato storico, e l’altro statistico.
Le equazioni della dinamica esprimono completamente le leggi del metodo storico applicato alla materia: ma l’applicazione di quelle equazioni implica una conoscenza perfetta di tutti i dati. Orbene, la più piccola porzione di materia che noi riusciamo a sottomettere all’esperimento consiste di milioni di molecole, nessuna delle quali diventa mai individualmente sensibile per noi. Non ci è possibile, di conseguenza, accertare il moto effettivo di una qualsiasi di tali molecole: ed allora siamo obbligati ad abbandonare il rigoroso metodo storico e ad adottare il metodo statistico di trattare con grandi gruppi di molecole.
I dati del metodo statistico applicati alla scienza molecolare sono le somme di grandi numeri di quantità molecolari. Nello studiare le relazioni fra quantità di questo genere incontriamo un nuovo tipo di regolarità, la regolarità delle medie: da esse possiamo dipendere con notevole sufficienza per tutti i fini pratici, ma esse non possono pretendere in alcun modo di avere quel carattere di assoluta precisione che appartiene alle leggi della dinamica astratta.
E così la scienza molecolare ci insegna che i nostri esperimenti non ci possono dare altro che una informazione statistica, e che da essi non si può dedurre alcuna legge che possa pretendere di avere una precisione assoluta. Ma quando passiamo dalla contemplazione dei nostri esperimenti alla contemplazione delle molecole stesse, allora lasciamo il mondo del caso e del mutamento, ed entriamo in una regione dove ogni cosa è certa e immutabile.
Maxwell diceva che tra le forme di conoscenza che egli aveva individuato ve ne era una migliore e più approfondita, quella storica, mentre quella statistica era una conoscenza dal carattere inferiore. Ma c’è di più. Più oltre Maxwell diceva che la conoscenza statistica è l’ultima per noi possibile perché dopo vi è il limite dove occorre fermarsi:
Siamo così giunti, seguendo un cammino strettamente scientifico, molto vicini al punto in cui la scienza deve fermarsi. Non voglio dire che la scienza sia impedita nello studio del meccanismo interno di una molecola che non si riesce a ridurre in parti: non è più impedita di quanto non le accada nell’analisi di un organismo che non si riesce a costruire mettendo insieme le sue parti. Tuttavia, nel seguire verso il passato la storia della materia, la scienza si ferma nel momento stesso in cui, per un verso, essa diventa consapevole del fatto che la molecola è stata fatta, e, per l’altro verso, essa capisce che la molecola non è stata fatta mediante uno qualsiasi dei processi che chiamiamo naturali.
La scienza non è competente a ragionare attorno alla creazione di materia a partire dal nulla. Abbiamo raggiunto il livello superiore delle nostre facoltà intellettuali nel momento in cui abbiamo ammesso che la materia, in quanto non può essere eterna ed autoesistente, deve essere stata creata.
E il limite alla conoscenza è rappresentato da Dio e dalla creazione che sono entità e fenomeni non naturali e quindi non studiabili. Di nuovo, in Gran Bretagna, registriamo questi atteggiamenti che intrufolano la fede all’interno di una ricerca scientifica che, secondo altri modi di vedere, non ha limiti a priori. Curioso il fatto che una mente del livello di quella di Maxwell individui il limite in quello che si è realizzato fino al suo lavoro non dando altre possibilità a chi proseguirà le ricerche. Stesse cose, e cioè che il Secondo Principio non era stabilito in modo certo come altri fondamenti della fisica, erano praticamente dette dal discorso che Maxwell aveva fatto esemplificando con quell’intelligenza che avrebbe dovuto operare dentro un gas che, non a caso, nel 1879 aveva sostenuto anche Kelvin (che chiamò quell’intelligenza diavoletto)(4). E Kelvin sull’argomento aveva già scritto un articolo per Nature (9 aprile 1874, in Opere, pp. 566-568), nel quale aveva sostenuto un argomento dirimente contro quanto aveva realizzato Boltzmann nel suo lavoro del 1872, argomento poi ripreso abbondantemente da altri critici. Scriveva Kelvin:
Nella dinamica astratta, un rovesciamento istantaneo del movimento di ogni particella in moto di un sistema è causa di un moto all’indietro del sistema stesso, con ciascuna particella lungo la propria vecchia traiettoria così da aver di nuovo per ogni posizione la medesima velocità in valore assoluto già assunta prima – il che equivale a dire, in linguaggio matematico, che ogni soluzione resta una soluzione quando t è sostituito con – t. Nella dinamica fisica, questa reversibilità semplice e perfetta cessa di valere in conseguenza di forze che dipendono da: attrito fra solidi; imperfetta fluidità dei fluidi; imperfetta elasticità dei solidi; differenze di temperatura e conseguente conduzione di calore prodotte da sollecitazioni in solidi e fluidi; imperfetta capacità magnetica, polarizzazione elettrica residua dei dielettrici; generazione di calore da parte di correnti elettriche indotte; dal moto; diffusione di fluidi, soluzione di solidi entro fluidi e altre modificazioni chimiche; assorbimento di calore radiante e luce. La presa in considerazione di queste azioni, in rapporto alla legge universale dell’energia che Joule dimostrò essere valida per esse, mi condusse ventitre anni fa alla teoria della dissipazione dell’energia, di cui diedi comunicazione per la prima volta alla Royal Society di Edimburgo nel 1852, con uno scritto intitolato Una tendenza universale della natura verso la dissipazione dell’energia meccanica.
L’essenza della scoperta di Joule consiste nel sottomettere i fenomeni fisici a leggi dinamiche. Allora, se ad un istante qualsiasi, il moto di ogni particella di materia nell’universo fosse rovesciato con esattezza, il corso stesso della natura verrebbe semplicemente rovesciato per sempre. La bolla di schiuma che sta per scoppiare ai piedi di una cascata si contrarrebbe e tornerebbe entro l’acqua: i moti termici riconcentrerebbero la propria energia e lancerebbero l’intera massa verso l’alto lungo la cascata, in gocce che si riformerebbero all’interno di una colonna chiusa d’acqua risalente. Il calore che è stato generato dall’attrito fra solidi e dissipato per conduzione, e per radiazione con assorbimento, tornerebbe nuovamente al punto di contatto e spingerebbe all’indietro il corpo che era in moto contro quella forza alla quale quest’ultimo aveva dapprima ceduto. I macigni erratici riprenderebbero dalla terra gli elementi necessari per ricostruire se stessi secondo le loro frastagliate forme primitive, e tornerebbero a riunirsi a quei picchi montani da cui originariamente si erano staccati. E se anche l’ipotesi materialistica della vita fosse vera, le creature viventi crescerebbero alla rovescia, con una conoscenza consapevole del futuro ma prive di memoria per il passato, e torneerebbero di nuovo ad esser non nate. Tuttavia i fenomeni reali della vita trascendono infinitamente la scienza umana, e la meditazione sulle conseguenze di un loro immaginario rovesciamento è completamente vana. Ben diverso è però il caso relativo alla meditazione sul rovesciamento dei moti della materia non influenzata dalla vita, in quanto una considerazione del tutto elementare su di essi conduce alla completa spiegazione della teoria della dissipazione dell’energia.
L’argomento di Kelvin era chiaro e demoliva le operazioni che fino al 1872 aveva costruito Boltzmann. La meccanica astratta, la scienza precisa ed indiscutibile, ha determinate leggi che restano le medesime se si inverte il segno del tempo. Ora, con queste stesse leggi non può ricavarsi un effetto contrario e cioè il fatto che, ad esempio, le molecole avevano una direzione privilegiata che non poteva essere percorsa in senso inverso. Piuttosto che speculare su come si comporta la materia, occorreva considerare tutta una serie di fenomeni che non rientrano nella dinamica astratta (attriti, eccetera). Sono proprio questi fenomeni che dissipano energia meccanica e spiegano il paradosso dell’inversione delle velocità.
Questa obiezione solo discorsiva di Kelvin fu ripresa da Loschmidt che sull’argomento pubblicò quattro memorie dal titolo Über den Zustand der Wärmegleigewitches eines Systems von Korpern mit Rücksicht auf die Schwerkraft (Sullo stato dell’equilibrio termico di un sistema di corpi rispetto alla forza di gravità, Wiener Berichte, 73, 74, 75 e 76; 1876/1877).
Secondo Loschmidt l’irreversibilità del Secondo Principio dipendeva dalle particolari condizioni iniziali e non dalle leggi che governano il moto delle molecole. Andare con la meccanica ad analizzare il Secondo Principio non può dar conto dell’irreversibilità. Supponiamo di avere un gas perfetto come esemplificazione di un sistema meccanico e consideriamolo in due fasi successive Tj e Tj‘, fasi identiche tra loro con la sola differenza del verso dei due vettori velocità. Secondo il teorema H di Boltzmann deve risultare che Hj = Hj‘. La prima fase evolverà secondo la direzione …T1, T2, …, Tn, … mentre la seconda fase evolverà secondo l’altra direzione … Tn‘, …, T2‘, T1‘, … Nel primo caso dovrà risultare H1 ≥ H2 ≥ … ≥ Hn, mentre nel secondo caso si dovrà avere Hn‘ ≤ … H2‘ ≤ H1‘. La situazione descrive evidentemente un paradosso perché il sistema meccanico che abbiamo considerato presenta simultaneamente un moto con H crescente ed H decrescente.
In due memorie, Über die Aufstellung und Integration der Gleichungen welche die Molecularbewegung in Gasen Gestimmen (Wiener Berichte, 74, 1876)e Weitere Bemerkungen über einige Probleme des mechanischen Wänmetheorie (Sulla relazione tra un teorema meccanico generale e la seconda legge della termodinamica, Sitzsungsberichte Akad. Wiss., 75, 1877) Boltzmann rispose alle obiezioni di Loschmidt insistendo sul carattere statistico del Secondo Principio intimamente legato alla probabilità. Ed il problema non risiede nel fatto che possano esistere degli stati molto improbabili ma nella misura della loro probabilità. Il Secondo Principio è rappresentato dall’entropia, l’entropia di uno stato misura la sua probabilità e l’entropia aumenta perché i sistemi evolvono verso stati più probabili. Leggiamo la posizione di Boltzmann dalla seconda memoria citata:
Nella sua memoria sullo stato di equilibrio termico di un sistema di corpi rispetto alla gravità, Loschmidt ha stabilito un teorema che solleva dei dubbi sulla possibilità di una prova puramente meccanica della seconda legge. Dal momento che esso mi sembra estremamente ingegnoso e di notevole significato per la comprensione corretta della seconda legge, e visto che nella memoria citata esso è apparso soprattutto in una forma filosofica, tanto che molti fisici troveranno piuttosto difficile la sua comprensione, cercherò di riformularlo in questa sede.
Se noi vogliamo fornire una prova puramente meccanica del fatto che tutti i processi naturali si svolgono in modo che si abbia [un aumento di entropia] (5) dobbiamo assumere che il corpo sia un aggregato di punti materiali. Noi assumiamo che la forza di interazione tra questi punti sia una funzione delle loro posizioni relative. Quando tale funzione sia nota, diremo che conosciamo la legge di azione della forza. Al fine di calcolare il moto reale dei punti, e quindi le variazioni di stato del corpo, è necessario conoscere anche le posizioni e le velocità iniziali di tutti i punti. Diciamo cioè che devono essere date le condizioni iniziali. Se si cerca di provare la seconda legge da un punto di vista meccanico, si cerca sempre di dedurla dalla legge di azione della forza senza fare riferimento alle condizioni iniziali, che sono sconosciute. Si tenta pertanto di provare che – quali che siano le condizioni iniziali – i cambiamenti di stato del corpo avranno sempre luogo in modo che [si abbia un aumento di entropia]. Assumiamo adesso che sia dato un certo corpo come aggregato di punti materiali. Le condizioni iniziali al tempo zero siano tali che il corpo subisca cambiamenti di stato per cui [l’entropia aumenta]. Mostreremo allora che, senza cambiare la legge di forza, si possono trovare altre condizioni iniziali per cui si abbia al contrario [una diminuzione di entropia]. Consideriamo le posizioni e le velocità di tutti i punti dopo che sia trascorso un tempo arbitrario t1. Prendiamo ora, al posto delle condizioni iniziali originali, le seguenti: tutti i punti materiali abbiano al tempo zero le stesse posizioni iniziali che avevano dopo il tempo t1 con le condizioni originali e le stesse velocità ma con direzioni opposte. Per brevità chiameremo questo stato quello opposto a quello precedentemente trovato al tempo t1. E’ chiaro che i punti passeranno attraverso gli stessi stati di prima ma in senso inverso. Lo stato iniziale che essi avevano precedentemente al tempo zero sarà ora raggiunto dopo un tempo t1. Laddove avevamo trovato in precedenza [un aumento di entropia questa adesso decresce]. [L’aumento o la diminuzione] quindi non dipende dalla legge di forza ma solo dalle condizioni iniziali. Il fatto che [l’entropia in effetti aumenti] per tutti i processi che avvenngono nel mondo in cui viviamo (come mostra l’esperienza) non è dovuto alla natura delle forze, ma piuttosto alle condizioni iniziali. Se, al tempo zero lo stato di tutti i punti materiali dell’universo fosse esattamente l’opposto di quello che si ha effettivamente ad un tempo t1 successivo, allora il corso di tutti gli eventi tra i tempi t1 e zero sarebbe rovesciato, e quindi [l’entropia diminuirebbe]. Pertanto ogni tentativo di provare dalla natura dei corpi e dalla legge di forza, senza tener conto delle condizioni iniziali, che [l’entropia aumenta] deve necessariamente rivelarsi futile. Come si vede, questa conclusione è molto seducente e bisogna definirla un interessante sofisma. Al fine di localizzare l’origine della fallacia di questa argomentazione, dobbiamo immaginare un sistema con un numero finito di punti materiali che non interagisce con il resto dell’universo. Immaginiamo un numero grande ma non infinito di sfere assolutamente elastiche, che si muovono in un recipiente chiuso le cui pareti siano completamente rigide e parimenti elastiche. Nessuna forza esterna agisce sulle nostre sfere. Supponiamo che al tempo zero la distribuzione di sfere nel recipiente non sia uniforme; ad esempio supponiamo che la densità delle sfere sia maggiore a destra che a sinistra e che quelle nella parte superiore si muovano più rapidamente di quelle della parte inferiore e cosi via. Il sofisma ora consiste nel dire che, senza fare riferimento alle condizioni iniziali, non può essere provato che le sfere si mescoleranno uniformemente nel corso del tempo. Date le condizioni iniziali che abbiamo originariamente assunto ad esempio le sfere saranno quasi sempre uniformi al tempo t1. Noi possiamo scegliere allora, al posto delle condizioni iniziali originali la distribuzione di stati che è esattamente l’opposta di quella che si avrebbe (in conseguenza delle condizioni iniziali originali) dopo che è trascorso il tempo t1. Le sfere allora si selezionerebbero con l’andar del tempo e al tempo ti acquisterebbero una distribuzione di stati completamente non uniforme, anche se la distribuzione iniziale di stati era quasi uniforme.
Noi dobbiamo fare la seguente. considerazione: una prova che dopo un certo tempo t1 le sfere devono essere necessariamente mescolate uniformemente, qualunque possa essere la distribuzione iniziale di stati, non può essere data. Questa è infatti una conseguenza della teoria della probabilità poiché ogni distribuzione di stati non uniforme, non importa quanto improbabile possa essere, non è mai assolutamente impossibile. E’ chiaro invero che ogni singola distribuzione uniforme, che può realizzarsi dopo un certo tempo da qualche particolare stato iniziale, è altrettanto improbabile di una singola distribuzione non-uniforme; proprio come nel gioco del lotto, un qualunque insieme di cinque numeri ha la stessa probabilità dell’insieme costituito dai numeri 1, 2, 3, 4, 5. E’ solo per il fatto che le distribuzioni uniformi sono molto più numerose di quelle non uniformi che la distribuzione di stati diventerà uniforme con l’andare del tempo. Non si può quindi provare che, quali che possano essere le posizioni e le velocità delle sfere all’inizio, la distribuzione deve diventare uniforme dopo un lungo tempo; si può solo provare, piuttosto, che un numero infinitamente maggiore di stati iniziali condurrà ad uno stato uniforme dopo un certo lasso di tempo che ad uno non uniforme. Il teorema di Loschmidt tratta solo di stati iniziali che di fatto conducono ad una distribuzione non uniforme di stati dopo un certo tempo t1; ma esso non prova che non vi è un numero infinitamente maggiore di condizioni iniziali che conducono ad una distribuzione uniforme dopo lo stesso tempo. Al contrario, segue dallo stesso teorema che, dato che il numero di distribuzioni uniformi è infinitamente maggiore di quello delle distribuzioni non uniformi, il numero di stati che portano a distribuzioni uniformi dopo un certo tempo t1 è molto più grande del numero di quelli che portano a distribuzioni non uniformi, e questi ultimi sono quelli che devono essere scelti, secondo Loschmidt, per ottenere una distribuzione non uniforme al tempo t1.
Si potrebbe anche calcolare, partendo dal numero relativo delle differenti distribuzioni di stati, le loro probabilità, e questo potrebbe condurre ad un metodo interessante per il calcolo dell’equilibrio termico. Allo stesso modo si può trattare la seconda legge. È solo in alcuni casi speciali che si può provare che, quando un sistema passa da una distribuzione di stati non uniforme ad una uniforme, si ha [aumento di entropia], mentre [si ha diminuzione] nel caso opposto. Ma dal momento che vi è un numero infinitamente maggiore di distribuzioni di stati uniformi che di stati non uniformi, quest’ultimo caso è straordinariamente improbabile e può essere considerato impossibile ai fini pratici cosi come può essere considerato impossibile che se uno parte con azoto e ossigeno mescolati in un recipiente, dopo un mese si trovi ossigeno chimicamente puro nella metà inferiore e azoto in quella superiore, anche se dal punto di vista della teoria della probabilità ciò è soltanto molto improbabile ma non impossibile.
In ogni caso il teorema di Loschmidt mi sembra che sia della più grande importanza poiché mostra come siano intimamente connesse la seconda legge e la teoria della probabilità, mentre la prima legge è indipendente da essa. […] Se forse questa riduzione della seconda legge al dominio della probabilità fa si che la sua applicazione all’intero universo appaia dubbiosa, pure le leggi della teoria della probabilità sono confermate da tutti gli esperimenti effettuati in laboratorio.
IL SECONDO PRINCIPIO E LA PROBABILITA’
Queste polemiche ebbero l’effetto di convincere Boltzmann a scrivere un’altra memoria sul significato meccanico del Secondo Principio, Über die Beziehung zwischen dem zweiten Hauptsatze der mechanischen Wärmetheorie und der Wahrscheinlichkeitsrechnung respective den Sätzen über das Wärmegleichgewicht (Sulla relazione tra il Secondo Principio della termodinamica ed il calcolo delle probabilità rispetto al problema dell’equilibrio termico, Wiener Berichte, 76, 373-435), che, a suo parere, avrebbe dovuto sgomberare il campo dalle polemiche. In tale memoria Boltzmann abbandonò l’approccio cinetico classico ed elaborò un nuovo procedimento per descrivere la distribuzione di uno stato. Questa volta egli, mediante il calcolo combinatorio, contò direttamente il numero di differenti cammini attraverso i quali si sarebbe potuta realizzare una distribuzione. La distribuzione che descriveva l’equilibrio del sistema era quindi non solo l’unica distribuzione stazionaria ma anche quella che doveva realizzarsi con maggiore probabilità poiché si raggiungeva attraverso il massimo numero di cammini possibili.
In questa memoria Boltzmann riprendeva molti concetti di quella appena citata ed aggiungeva:
Lo stato iniziale di un sistema sarà, nella maggior parte dei casi, uno stato molto poco probabile ed il sistema tenderà sempre verso degli stati più probabili, fin quando giunge allo stato più probabile, cioè allo stato di equilibrio termodinamico. Se applichiamo questo al secondo principio della termodinamica, potremo identificare la grandezza che si chiama di solito entropia con la probabilità dello stato corrispondente. Consideriamo dunque un sistema di corpi che sia isolato [il cui stato si modifichi solo a causa dell’interazione tra i corpi che lo costituiscono]. In una tale trasformazione, in virtù del secondo principio della termodinamica, l’entropia totale del sistema non può che aumentare. Nella nostra interpretazione attuale, ciò non significa altro che il fatto che la probabilità dello stato d’insieme dei corpi del sistema deve continuamente aumentare: il sistema non può passare che da uno stato ad un altro più probabile.
A questo punto passava discutere dell’applicazione della teoria della probabilità a un sistema termodinamico. Ma questa volta c’era una grossa novità rispetto alle trattazioni precedenti. Boltzmann introduceva nella sua trattazione lo spazio delle fasi che appena un anno prima (1876) era stato introdotto nella meccanica statistica da H. W. Watson(6). Ora non si faceva più il conto probabilistico esteso all’enorme numero di molecole costituenti un gas inteso come unico sistema termodinamico. Si considerava invece il singolo sistema termodinamico macroscopico (ad esempio un gas) come costituito, istante per istante, da un enorme numero di stati dinamici microscopici differenti tra loro per la diversa configurazione o distribuzione (di posizioni e velocità) delle singole molecole costituenti il sistema termodinamico in oggetto. In questo modo, uno stesso stato termodinamico macroscopico, caratterizzato all’equilibrio da determinati valori di pressione, volume e temperatura, può essere originato, microscopicamente, da una enorme quantità di stati dinamici delle singole molecole. Mano a mano che ci si discosta dall’equilibrio il numero di stati dinamici microscopici, che rappresenta lo stesso stato termodinamico macroscopico, tende a diminuire, tende cioè a zero pur senza raggiungere mai questo valore limite(7).
Boltzmann passava quindi a calcolarsi mediante il calcolo combinatorio, il numero di differenti cammini attraverso i quali si sarebbe potuta realizzare una distribuzione. Utilizzava ora il metodo di calcolo che aveva annunciato nella memoria del 1872 quell’artificio che vedeva le energie di ogni molecola multiplo intero di una medesima quantità piccola di energia ε (seguo la traccia sviluppata da T. Kuhn nel suo Black-Body Theory and the Quantum Discontinuity 1894-1912).
Immaginiamo, diceva Boltzmann, un insieme di n molecole. Supponiamo che ogni molecola sia in grado di assumere solo un certo numero p di energie, ciascuna delle quali multiplo intero di una certa quantità energetica ε come nella seguente lista finita: ε, 2ε, 3ε, 4ε, … , pε, dove pε è l’energia totale disponibile. Se wk è il numero delle molecole dell’insieme che posseggono un’energia kε allora l’insieme dei numeri w0, w1, …, wp è sufficiente per definire uno stato (Zustandvertheilung) del gas. Poiché le molecole all’epoca erano distinguibili, uno stesso stato può essere ottenuto in vari modi, ciascuno dei quali Boltzmann chiama complessione diversa. Ci sono, ad esempio, n modi differenti o n complessioni di ottenere lo stato in cui una molecola abbia energia pε e tutte le altre zero. Da un punto di vista più generale se una complessione viene specificata per un insieme di n numeri k1, ognuno dei quali stabilisce l’energia (k1ε) dell’atomo i-esimo, una seconda complessione appartenente allo stesso stato può ottenersi mediante qualunque permutazione di due molecole, i e j, che posseggano energie differenti. Applicando il calcolo combinatorio, il numero di tali permutazioni è:
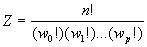
(1)
dove Z è la permutabilità e non la probabilità(8).
Per spiegare meglio ciò che andava a fare, Boltzmann esemplifica con una urna piena di pezzetti di carta, mescolati tra loro, ciascuno con un numero da 0 a p e con ogni numero contenuto lo stesso numero di volte nell’urna. Il numero del primo pezzetto di carta estratto determina il numero k1 di elementi di energia da attribuire al primo atomo, quello del secondo determina l’energia del secondo atomo, e così successivamente fino ad aver estratto n pezzetti di carta e determinato una complessione. A questo punto si rimettono i pezzetti di carta nell’urna rimescolandoli. Ripetendo l’estrazione si determina una seconda complessione, e dopo numerose estrazioni risulta rappresentata approssimativamente lo stesso numero di volte ogni possibile complessione. Per ultimo si scartano tutte le complessioni eccetto quelle per le quali l’energia totale degli n atomi risulti esattamente essere pε. Dentro tale sottosistema tutte le complessioni compatibili con con la condizione di energia totale si realizzano più o meno con la stessa frequenza. Se le complessioni che rimangono le classifichiamo in gruppi che rappresentano, non differenti complessioni, ma differenti stati, allora gli stati con un numero alto di permutazioni conterranno più complessioni degli stati con un numero basso di permutazioni. Lo stato più probabile sarà quello per il quale la Z della (1) sarà maggiore. Occorre allora passare a calcolare questo massimo con le condizioni che seguono:

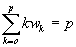
Poiché n è fisso, il problema equivale a rendere minimo il denominatore dell’equazione (1) e quindi, per semplificare i calcoli, a rendere minimo il suo logaritmo. E Boltzmann cerca il minimo di:
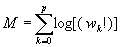
espressione che per valori grandi di wk si può riscrivere mediante la formula di Stirling (per a molto grande vale a! = aa) nel modo seguente:
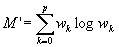
dove M’ differisce da M per una costante dipendente da ε che non influisce nella determinazione del minimo. Mediante il calcolo variazionale si stabilisce subito che per p >> n, la Z sarà massima se le wk sono date da:
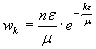
(2)
dove μ è l’energia media di una molecola. E questa relazione ci fornisce la distribuzione di energia più probabile, cosa che cercava Boltzmann. Egli, una volta stabiliti concetti e tecnica con un caso fittizio, passava ad un modello fisicamente realizzabile permettendo che le molecole non avessero più valori discreti di energia ma valori continui. La sua elaborazione richiedeva ancora dei fattoriali e quindi Boltzmann iniziava a dividere il continuo di energia in piccoli intervalli finiti, da 0 ad ε, da ε a 2ε, da 2ε a 3ε, eccetera. Passava quindi a scrivere le wk, che definiscono lo stato del gas, nella forma wk = ε.f(kε), da cui ε.f(kε) è il numero di molecole con energie comprese tra kε e (k + 1)ε. Con questi dati la dimostrazione di Boltzmann procede in modo simile a quello precedente. Non considerando di nuovo una costante che dipende da ε, la funzione da rendere minima è:

e questo problema di minimo è sotto le condizioni:
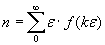

dove ET è l’energia totale del gas. Per valori sufficientemente piccoli di ε si possono approssimare le sommatorie con integrali, di modo che il problema matematico finale è minimizzare l’integrale:
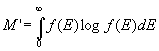
sottoposto alle condizioni:

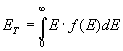
E la f in corrispondenza della quale M’ è minimo si ha in corrispondenza di molecole con energia tra E ed E + dE date da:
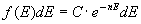
(3)
Poiché E = kε e wk = ε.f(kε) la (3) deriva direttamente dalla (2) per ε piccolo. Sembra quindi che questi ultimi calcoli fatti da Boltzmann potevano essere evitati. Boltzmann diceva subito che la (3) è analoga alla distribuzione di Maxwell in due dimensioni (da queste elaborazioni la statistica classica che conosciamo assumeva il nome di statistica di Maxwell-Boltzmann). Per studiare il caso tridimensionale occorre passare alla situazione fisica reale dividendo non il continuo di energia ma lo spazio tridimensionale delle velocità. Se le componenti ammissibili delle velocità u, v, w sono definite in piccoli intervalli finiti, da aε a (a + 1)ε, da bζ a (b + 1)ζ, da cη a (c + 1)η, dove a, b e c sono interi compresi tra – ∞ e + ∞, allora le wk che caratterizzano uno stato diventano:
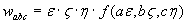
ed il corrispondente numero di permutazioni è:

Boltzmann descriveva a questo punto un nuovo modo di numerare i pezzetti di carta nell’urna, di modo che Z diventava la frequenza relativa di accadimento della corrispondente distribuzione nello spazio delle velocità. Subito dopo tentava come fatto precedentemente di massimizzare Z attraverso la minimizzazione il prodotto del denominatore dell’espressione che fornisce Z. A questo fine scriveva prima in forma di sommatoria il logaritmo dell’espressione da minimizzare e le condizioni relative, si sbarazzava di una costante che dipendeva dai valori di ε, ζ, η ed alla fine sostituiva alle sommatorie gli integrali. Il problema si riduceva quindi a massimizzare l’espressione:

sotto le condizioni:

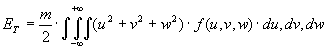
E così, dice Boltzmann, il problema del massimo è risolto.. Le due condizioni non sono altro che conservazione della materia e la conservazione dell’energia. mentre Ω non è altro che la funzione H cambiata di segno. Nella memoria del 1872 (e soprattutto in un ‘altra memoria del 1875) Boltzmann aveva dimostrato che H arriva ad un minimo quando f corrisponde alla distribuzione di Maxwell ed ora quindi non si doveva ripetere la dimostrazione. Avendo ricordato questo Boltzmann aveva dimostrato che il caso dell’equilibrio termico, che corrispondeva ad una H minima, corrispondeva anche allo stato più probabile del gas.
Nella sezione finale della memoria, Boltzmann affrontava il problema di legare l’entropia con la probabilità. Boltzmann iniziava con il dimostrare che:
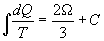
per un gas perfetto monoatomico in equilibrio. Ignorando la costante d’integrazione C, l’entropia del gas deve essere allora a due terzi della misura della permutabilità Ω. Per il secondo principio si sa che l’entropia totale di tutti i corpi interessati ad un cambiamento di stato dato deve aumentare deve aumentare o, per processi reversibili, rimanere costante, e lo stesso deve accadere pertanto per la misura della permutabilità per sistemi in equilibrio. Boltzmann estendeva questa caratteristica di Ω alle transizioni di un gas tra stati di non equilibrio, stati cioè che non ubbidiscono alla distribuzione di Maxwell e per i quali non si erano definite anteriormente entropia e temperatura. A differenza dell’entropia di un gas, scriveva Boltzmann, la grandezza che ho chiamato misura della permutabilità può sempre calcolarsi; e naturalmente il suo valore sarà necessariamente maggiore dopo il cambio di stato rispetto a prima che tale cambio sia avvenuto.
Boltzmann non forniva ulteriori spiegazioni per la relazione che legava tra loro le sue grandezze in gioco, l’entropia S e la probabilità P (9) la famosa:
S = K.logP
Nel suo Vorlesungen über Gastheorie (Lectures on Gas Theorie, Lipsia 1896 e 1898) continuano a non esservi spiegazioni convincenti. Ma qui veniva abbandonato il termine “misura della permutabilità” e veniva dimostrato che -H è proporzionale al logaritmo della probabilità e che ambedue queste grandezze erano proporzionali all’entropia per stati di equilibrio. Più oltre si generalizzava a trasformazioni di non equilibrio con la seguente affermazione: in natura le trasformazioni tendono sempre ad avanzare da stati meno probabili a stati più probabili.
Dopo altri brevi passaggi così si concludeva la memoria di Boltzmann che doveva segnare una svolta importante nella storia della fisica. Boltzmann tornerà ancora su questi problemi ma la parte fondamentale del suo lavoro era fatta.

Negli anni seguenti vi furono importanti aggiustamenti e perfezionamenti ad opera ancora di Maxwell, di Helmholtz, di Boltzmann stesso e di vari altri tra cui Planck e Gibbs. Va ricordato in particolare il contributo di Helmholtz (1821 -1894) che, nel 1877, introdusse nella termodinamica i concetti di ordine e disordine, iniziando a considerare l’entropia come una misura del disordine. In questo modo i processi più probabili sono quelli che fanno passare il sistema termodinamico a stati sempre più disordinati, mentre è solo il moto molecolare ordinato quello che è in grado di essere convertito in altre forme di lavoro meccanico.

L’introduzione dei concetti di ordine e disordine nella termodinamica avvenne in un ciclo di lezioni che Helmholtz tenne nel 1877 a Berlino ed alle quali assistettero Planck e Wien. In esse, raccolte in appunti e pubblicate poi in

Wien
Vorlesungen über theoretische Physik, Vol. 5, Dynamik continuirlick verbreiteter Massen (Lipsia, Barth 1902), Helmholtz sostenne che la meccanica corpuscolare riconosce due tipi di moto. Uno è il moto ordinato che è un moto d’insieme di tutte le particelle. L’altro è il moto disordinato, i movimenti indipendenti che le particelle realizzano dentro lo spazio occupato dal loro aggregato. Per Helmholtz la caratteristica principale della meccanica del continuo è l’assenza del moto disordinato. Questo concetto di moto disordinato ha un interesse limitato in meccanica ma ne assume uno rilevante nella termodinamica. E’ il moto disordinato delle più piccole particelle dei corpi che costituisce il calore; il moto cioè in cui la velocità e lo spostamento di ogni singola particella non ha alcuna relazione con quelle vicine. Dall’ipotesi che le molecole di un gas sono in moto disordinato Helmholtz dedusse poi altre proprietà dei gas.
LA CRITICA DI ZERMELO
Prima di passare all’argomento, è utile dare un cenno all’ultima parte della vita di Boltzmann. Ho già detto del suo matrimonio nel 1876 e dei suoi cinque figli. Nel 1888 perse, con sommo dolore, il figlio maggiore. Nel 1885 fu eletto membro dell’Accademia delle Scienze dell’Impero e nel 1887 divenne rettore dell’Università di Graz. Nel 1890 accettò la cattedra di fisica teorica a Monaco e nel 1895 tornò ad insegnare all’istituto di Fisica di Vienna dove successe al suo vecchio maestro ed amico Stefan. Non si trovò bene a Vienna perché aveva come collega quel Mach con cui ebbe sempre scontri molto importanti. Nel 1899 fece un viaggio viaggio in America, il primo. Nel 1900 passò ad insegnare fisica teorica a Lipsia ma nel 1902 tornò Vienna dove, dal 1903, insegnò anche filosofia della scienza sostituendo Mach a tale insegnamento. Le sue lezioni ebbero un grande successo e

Ehrenfest
furono molto frequentate. Suoi studenti furono Paul Ehrenfest e Lise Meitner.

Meitner
Quest’ultima ci racconta di un Boltzmann che passava da momenti di euforia a momenti di forte depressione. Nel 1906, durante le vacanze estive a Duino, vicino Trieste, si suicidò.

Boltzmann a Saint Louis nel 1904 in visita all’Esposizione Universale. In tale occasione tenne una conferenza sulla matematica applicata alla fisica. In questa occasione fece un giro per varie università USA.
Ma torniamo ai lavori di Boltzmann. Come già accennato, sul finire del secolo una nuova critica molto insidiosa venne ai lavori di Boltzmann da parte di Ernst Zermelo (1871 – 1953), il giovane assistente di Max Planck, con la sua memoria

Zermelo
Über einen Satze der Dynamik und die mechanischen Wärmetheorie (Sul legame esistente tra la dinamica e la termodinamica, Annalen der Physik 57, 1896) e con una successiva, Über die mechanische Erklärung irreversibler Vorgänge (Su una spiegazione meccanicadei processi irreversibili, Annalen der Physik 59, 1896), alla quale rispose Boltzmann con la sua Zu Hrn. Zermelo’s Abbandlung “Über die mechanische Erklärung irreversibler Vorgänge” (A proposito dell’articolo del sig. Zermelo “Su una spiegazione meccanicadei processi irreversibili“, Annalen der Physik 60, 1897).
Zermelo, per muovere la sua obiezione, utilizzò un teorema che aveva trovato Poincaré nel 1890, Sur le problème des trois corps et les equations de la dynamique (Acta Math., 13). Questo teorema, detto Teorema della ricorrenza, studiava la stabilità dei sistemi trattati con la meccanica di Newton ed afferma che se si ha un sistema termodinamico contenuto in un determinato volume, che dispone di una quantità data di energia e che può essere descritto mediante equazioni differenziali ordinarie, tale sistema ritornerà arbitrariamente al suo stato iniziale dopo un tempo lungo a sufficienza. Detto in altro modo, il teorema affermava che un sistema composto da particelle tra le quali si abbiano interazioni con forze dipendenti unicamente dalla posizioni delle particelle nello spazio, può assumere qualunque configurazione. Questo teorema negava quindi l’evoluzione di un sistema termodinamico, come quello descritto, da qualunque stato partisse verso la distribuzione di Maxwell, quella prevista per l’equilibrio; il teorema diceva che il sistema ritornava arbitrariamente verso quello stato iniziale. E, di fatto, negava tutte le ultime elaborazioni di Boltzmann ed il fatto che si potesse applicare la teoria cinetica, costruita su modelli meccanici, alla termodinamica. Ciò che Zermelo concludeva come conseguenza di questo teorema era che, visto che la termodinamica non poteva essere discussa in quanto portato dell’esperienza, vi era la sola strada di abbandonare i modelli meccanici e quindi l’approccio meccanicistico. Egli aggiungeva poi che lo stesso concetto di probabilità non ha nulla che vedere con il tempo e quindi non può essere impiegato per disquisire sulla direzione dei processi irreversibili. E ciò vuol dire che non solo è impossibile spiegare il principio generale dell’irreversibilità, ma è anche impossibile spiegare i singoli processi irreversibili senza introdurre nuove assunzioni fisiche
Boltzmann rispose in modo ironico affermando che, poiché il Teorema di Poincaré è certamente corretto, restava sempre da stabilire la questione del tempo necessario perché avvenga la ricorrenza di cui parla il teorema e quindi se è corretta l’applicazione del teorema a questa applicazione. Per un piccolo volume di gas dell’ordine di alcuni centimetri cubici questo tempo è molti ordini di grandezza superiore all’età dell’Universo e benché H possa aumentare è infinitamente improbabile che ciò avvenga (il tempo invece necessario per un tale sistema di tendere ad una distribuzione di Maxwell è valutabile in centomilionesimi di secondo). Concludere che la teoria cinetica deve essere rifiutata perché è valido il teorema di Poincaré corrisponde ad una persona che prima di lanciare un dado, calcolasse la probabilità di ottenere mille volte di seguito un 1 e, trovando un numero molto piccolo, arrivasse alla conclusione che il dado deve essere truccato. Nuovamente, affermava Boltzmann si confondeva improbabilità con impossibilità. La seconda legge è una legge statistica e non deterministica. Inoltre l’entropia di un sistema misura la sua probabilità ed l’aumento dell’entropia nei processi che avvengono in natura non è altro che la tendenza dei sistemi a tendere verso la distribuzione molecolare più probabile, quello dell’equilibrio termico. E l’irreversibilità era proprio una conseguenza di questa tendenza. In nessun caso, comunque Boltzmann poteva accettare di scegliere tra seconda legge della termodinamica ed interpretazione meccanica di essa e più in generale dei fenomeni naturali. Ed alla fine del suo articolo diceva con tristezza:
il lavoro di Zermelo dimostra che i miei lavori non sono stati ancora capiti; nonostante tutto posso essere contento poiché questa pubblicazione è una prova che in Germania sono soggetti a qualche attenzione.
Su questa polemica dice Bellone:
L’attacco di Zermelo forniva a Boltzmann l’occasione per suffragare la necessità della freccia termodinamica basandola su argomenti relativi a una freccia cosmologica. Quest’ultima era introdotta nel discorso per mezzo di un’assunzione che lo stesso Boltzmann definiva «ovviamente indimostrabile»:
L’universo – o, perlomeno, gran parte di ciò che ci circonda -, visto come sistema meccanico è partito da uno stato molto improbabile e si trova ancora in uno stato poco probabile, Se si prende allora in esame un sistema di corpi più piccolo, così come lo si trova nella realtà, e lo si isola istantaneamente dal resto del mondo, questo sistema verrà inizialmente a trovarsi in uno stato improbabile e, per tutto il tempo in cui resterà isolato, procederà sempre verso stati più probabili.
Nella cornice delineata dalla freccia cosmologica la fisica non analizzava più sistemi completamente arbitrari, ma solo quei sistemi che erano dislocati «nello stato attuale dell’universo» e per i quali, de facto, gli stati “iniziali” precedevano quelli “finali”, L’operazione boltzmanniana era drastica: veniva accettato un principio unificatore attribuendogli una portata esplicativa e negando, di conseguenza, la necessità di suggerirne una spiegazione. L’assunzione della freccia cosmologica, d’altra parte, consentiva una rappresentazione plausibile dello «stato iniziale del mondo».
L’universo era immaginabile, nella sua interezza, come un sistema in equilibrio (e «quindi morto») all’interno del quale erano collocate isole (o «mondi») con dimensioni paragonabili a quelle della nostra galassia. Questi mondi erano fluttuazioni: essi deviano dall’equilibrio termico su periodi di tempo lunghi rispetto alle nostre capacità osservative.
Il problema del tempo, allora, assumeva un aspetto singolare. Per l’universo visto nella sua globalità non esisteva freccia temporale. Il grande sistema era in equilibrio e le due direzioni del tempo erano indistinguibili, nello stesso modo in cui non aveva senso distinguere, nello spazio, 1’«alto» dal «basso». Per un osservatore solidale con un “mondo”, invece, le circostanze erano ben diverse:
Proprio come in un dato luogo sulla superficie della Terra possiamo usare l’espressione «verso il basso» per indicare la direzione verso il centro del pianeta, così, in quanto creature viventi che si trovano in un mondo del genere in uno specifico periodo di tempo, possiamo definire la direzione del tempo come se essa andasse dagli stati meno probabili verso quelli più probabili (di modo che i primi diventeranno il “passato” e, i secondi, il “futuro”), e, in virtù di questa definizione, troveremo che questa piccola regione, isolata dal resto dell’universo, è sempre “inizialmente” in uno stato improbabile.
Con questa descrizione di un universo possibile e privo di freccia temporale, che Boltzmann disegnava anche nel suo trattato sui gas il cui secondo volume si stampava nel 1898, si chiudeva la riflessione ottocentesca sull’ asimmetria legata all’ irreversibilità.
Oltre alle dure critiche ora viste alle quali occorre aggiungere quelle di Loschmidt delle quali ho parlato qualche pagina più su, sul finire del secolo si aggiunsero anche quelle di alcuni fisici britannici che si mostrarono scettici sull’interpretazione che Boltzmann forniva del Secondo Principio nelle discussioni sorte nell’incontro annuale ad Oxford della British Association nel 1894. Nonostante ciò egli era amareggiato perché trovò più conoscenza, interesse e comprensione dei suoi lavori in terra britannica di quanto non ne avesse in Austria e Germania. Qualche anno dopo, nel 1897, si ebbe anche una breve polemica con Planck che in una conferenza del 1891 aveva delineato le difficoltà incontrate nel correlare la meccanica statistica dei moti molecolari con la termodinamica
Planck
macroscopica. La polemica riguardava l’irreversibilità dei fenomeni di radiazione stimolati (era ciò che Planck studiava e che lo avrebbe portato alle sue fondamentali scoperte del 1900). Boltzmann rispose:
E’ certamente possibile e sarebbe gratificante derivare per i fenomeni della radiazione un teorema analogo a quello dell’entropia a partire dalle leggi che riguardano tali fenomeni, allo stesso modo di ciò che è stato fatto per la teoria dei gas. Sarei grato al dott. Planck se il suo lavoro sullo scattering di onde piane prodotte da risonatori molto piccoli diventasse utile per questo fine […]. (L. Boltzmann: Uber irreversible Strahlungsvorgänge II., Berliner Ber).
Secondo Planck, che si mantenne comunque un meccanicista fino a convertirsi in seguito (1900) alle concezioni di Boltzmann, la strada da seguire era quella della termodinamica chimica aperta da Willard Gibbs (1839 – 1903) nel 1876 e che,

Gibbs
insieme ai lavori di Planck, costituirà un approccio alternativo ai lavori di Boltzmann. In ogni caso Planck fece buon uso di quanto Boltzmann gli aveva detto e fu utilizzando i suoi metodi statistici che riuscì, a partire dal problema della radiazione del corpo nero, a formulare la sua invenzione dei quanti.
DIFFERENTI CONCEZIONI SULLA CONOSCENZA DELLA NATURA
E’ utile a questo punto accennare al dibattito accesissimo che si svolgeva nella fisica e non solo su questioni di termodinamica. Non sembri che si esca da quanto discuto, è indispensabile cercare di cogliere in che dibattiti era impegnato Boltzmann per capire uno dei possibili motivi della sua tragica fine. Riprendo qui alcune delle cose che ho discusso altrove e che è possibile leggere lì perché trattate in modo più esteso(10).
Sull’onda del successo del lavoro di Helmholtz, Sulla conservazione della forza, il fisico britannico W.J.M. Rankine (1820-1872) tentò di costruire una fisica basata sulla termodinamica. Nel suo Lineamenti di una scienza dell’energetica (1855), egli sostenne che il metodo più proficuo per conoscere la natura è quello

Rankine
che si affida ad astrazioni che sono in grado di essere formalizzate per condurci alla scoperta di principi generali. La termodinamica, nella quale l’energia gioca il ruolo più importante perché da essa dipendono i cambiamenti, è il migliore strumento che può servire alla conoscenza della natura. In definitiva, per Rankine, la scienza energetica è il sistema teorico più generale per la conoscenza del mondo naturale che ci circonda.
La tesi di Rankine venne ripresa dal fisico tedesco Georg Helm (1851-1923) il quale, nel suo Lezioni sull’energia (1877), sostenne, in accordo in questo con Mayer e lodato per questo da Mach, che tutte le forme di energia sono

Helm
equivalenti, togliendo in questo modo un qualche ruolo privilegiato all’energia meccanica. E poiché tutte le forme di energia sono equivalenti, la materia, che in meccanica è il veicolo di trasmissione dell’energia, perde il suo ruolo centrale (Helm aveva buon gioco a sostenere questa tesi soprattutto a partire dal 1886, dopo le prime esperienze di Hertz di trasmissione dell’energia attraverso onde elettromagnetiche). In questo quadro esplicativo veniva, rifiutata l’idea di atomo e

Hertz
di corpuscolo e quindi di ogni descrizione modellistica e tanto meno meccanicistica come invece usavano fare sia Helmholtz che Boltzmann (e la cosa era in uso anche tra i fisici britannici tra cui Maxwell e Kelvin)(11). Per fare scienza, occorre osservare i fenomeni cercando delle relazioni matematiche tra le diverse osservazioni senza introdurre ipotesi; le stesse osservazioni, comunque, non hanno mai una validità assoluta. Scriveva Helm (L’energetica nel suo sviluppo storico del 1898):
Per la fisica teorica generale non vi sono né atomi né energia, né nulla di simile, ma solo esperienze tratte immediatamente da gruppi di osservazioni. Perciò penso che il maggior pregio dell’energetica consista nella sua facoltà di adattarsi in modo immediato alle esperienze, molto più di quanto non potessero farlo le vecchie teorie.
Dopo questi brevi cenni agli iniziatori, arriviamo al più noto rappresentante dell’energetica, il chimico-fisico tedesco W. Ostwald (1853-1932), premio Nobel per la chimica nel 1909. Egli avanzò delle idee addirittura più radicali di quelle di

Ostwald
Helm: non solo l’energia è la base di tutti i fenomeni naturali, ma essa. è addirittura una sorta di nuova sostanza (ed Helm osserverà: nei tentativi di attribuire all’energia un’esistenza sostanziale, vi è una preoccupante deviazione rispetto alla chiarezza originale delle vedute di Mayer). In una sua opera, L’energia (1908), che ebbe una notevolissima influenza sugli scienziati del tempo, egli formulò così le sue concezioni;
Si intende per energetica lo sviluppo dell’idea secondo la quale tutti i fenomeni della natura debbono essere concepiti e rappresentati come delle operazioni effettuate sulle diverse energie. La possibilità di una simile descrizione della natura, non poté essere immaginata che quando fu scoperta la proprietà generale che possiedono le diverse forme di energia di potersi trasformare le une nelle altre. Robert Mayer fu dunque il primo che poté prendere in considerazione questa possibilità.
Fino a lui tutti gli scienziati aderivano alla concezione meccanicista, cioè all’idea che i fenomeni naturali sono tutti, in ultima analisi, di natura meccanica, il che vuol dire che possono essere ricondotti a dei movimenti della materia. Là dove non si poteva dimostrare l’esistenza di questi movimenti, come nel caso del calore e dell’elettricità, si ammetteva che essi si producessero negli atomi, cioè in particelle così piccole da sfuggire all’osservazione diretta …
L’ipotesi meccanicista ha due inconvenienti molto grandi; in primo luogo essa obbliga ad adottare un gran numero d’altre ipotesi indimostrabili, quindi essa è impotente a farci comprendere il legame che esiste incontestabilmente, dal momento che lo constatiamo giornalmente, tra i fenomeni fisici nel senso stretto del termine ed i fenomeni psicologici…
Ora, sono le teorie meccaniche tali da poter essere applicate in un modo sufficientemente generale ? Ebbene no, non c’è dubbio che esse non lo sono. Bisogna in primo luogo far notare che tra i fenomeni a noi conosciuti non ce ne sono che pochi (la maggioranza dei fenomeni astronomici) che soddisfano alle leggi meccaniche … Noi spieghiamo questo fatto mediante l’attrito. Il problema che allora si pone è di far rientrare i fenomeni d’attrito nelle leggi meccaniche …
Un’altra strada fu seguita da R. Mayer. Essa consisteva nel considerare i fenomeni meccanici come semplici casi particolari delle generali trasformazioni dell’energia, che sottostanno tutte alla legge di conservazione.
Se non si sceglie questa strada, com’è possibile, secondo Ostwald, dar conto dell’elettricità statica ? Dove stanno qui i movimenti ?
Questo problema è nato unicamente dall’ipotesi arbitraria che si abbia a che fare con un fenomeno meccanico, quando esso non lo è affatto. Esso è, con tutta la forza del termine, uno pseudoproblema, per usare un’espressione molto corretta di E. Mach …
Di fronte alla concezione meccanicista si erge quella di Mayer, che noi chiamiamo la concezione energetica poiché essa si fonda essenzialmente sulla nozione di energia … Non è possibile caratterizzare in modo migliore il metodo dell’energetica; essa estrae dai fenomeni le proprietà delle differenti specie di energia, e generalizza queste proprietà per mezzo dell’induzione …
Così si deve considerare Robert Mayer come il primo degli energetisti. Ai suoi occhi, l’energia è un oggetto reale, ed egli la colloca come tale, a lato della materia, dalla quale, per lui, si distingue per la sua imponderabilità …
Un tratto che contribuisce a fare di Mayer un vero energetista, un energetista con spirito moderno, è la sua avversione per le ipotesi.
Con queste parole Ostwald tracciava il nucleo centrale dell’energetica. Ma la polemica contro il meccanicismo non si fermava qui: essa tendeva a diventare dura polemica contro tutto il materialismo. (l’identificazione tra materialismo e meccanicismo è di Hegel e contro questa identificazione si batterà Engels).
Nel 1895, al congresso dei medici e naturalisti che si tenne a Lubecca, Ostwald lesse una comunicazione dal titolo, molto significativo, Il superamento del materialismo scientifico. Tra le altre cose Ostwald disse:
La materia è un’invenzione, del resto abbastanza imperfetta, a cui facciamo ricorso per rappresentarci quanto vi è di permanente in tutto ciò che accade. La realtà effettiva, quella che opera su di noi, è l’energia, [inoltre] l’irreversibilità di fatto dei fenomeni effettivi della natura dimostra che vi sono processi i quali non sono descrivibili mediante equazioni meccaniche, e con ciò il verdetto sul materialismo scientifico è deciso.
Ed Helm, presente a quel congresso, nello scrivere la sua cronaca (1898), coglieva bene i livelli e l’intensità dello scontro, che non erano banalmente legati a questa o a quella teoria, ma ad un modo nuovo o almeno diverso di fare scienza e, più in generale, ad una diversa concezione del mondo. Scriveva Helm:
Nella polemica che si accese a Lubecca non si trattava di atomismo o di spazio occupato da materia continua, non della irreversibilità nella termodinamica, o dei fondamenti energetici della meccanica. Queste sono tutte bazzecole. Si trattava in realtà dei principi della nostra conoscenza della natura.
Anche A. Sommerfeld (1868-1951) era presente a quel congresso e così descriveva (1944) la situazione:
Il campione dell’energetica era Helm, dietro di lui stava Ostwald e dietro entrambi la filosofia di Ernst Mach (che non era presente di persona). A loro si opponeva Boltzmann, assecondato da Felix Klein. La battaglia tra Ostwald e Boltzmann fu molto simile ad un duello tra un toro ed un agile torero. Tuttavia, questa volta il toro sconfisse il torero nonostante la sua agilità.
Gli argomenti di Boltzmann non trovarono resistenza. Noi giovani matematici eravamo tutti dalla parte di Boltzmann; fu subito ovvio per noi che era impossibile che da una sola equazione per l’energia potessero seguire le equazioni del moto anche di un solo punto materiale.
Sommerfeld
Spero si intuisca da quanto qui brevemente riportato a che livello e con che asprezza ci si scontrava.
La tesi di Ostwald e di tutta la corrente fenomenista, che vedeva Boltzmann praticamente solo a tentare una qualche opposizione, era sostanzialmente la seguente. Molti fenomeni fisici e, si noti l’accostamento, psicologici, non sono spiegabili con la meccanica. In particolare, e qui si ritorna all’obiezione che Loschmidt fece a Boltzmann, l’irreversibilità termodinamica non può essere spiegata dalla meccanica che ha delle equazioni che risultano completamente reversibili. Inoltre il complesso dei fenomeni elettromagnetici non è riconducibile ad una interpretazione meccanicista. Ed in definitiva, secondo Ostwald, tutta l’enorme varietà dei nuovi fenomeni sfuggono ad una interpretazione meccanica a meno di supporre strane entità, come gli atomi, delle quali non si ha nessun indizio sperimentale (riguardo al rifiuto degli atomi, Ostwald, nel 1909, nella 4ª edizione dei suoi Fondamenti di chimica generale, ritornò sulle sue posizioni ammettendone l’evidenza sperimentale) o a delle ipotesi che sfuggono a qualunque verifica sperimentale. Il rifiuto della meccanica e dei suoi metodi comportava il rifiuto dei fondamenti della meccanica ed in particolare di quella entità, la materia, che non è altro che una particolare energia che noi percepiamo come materia con i nostri sensi. Tutto ciò che ci circonda non è altro che energia. Noi abbiamo a che fare con differenti forme di energia che si trasformano l’una nell’altra facendo salvi i principi di conservazione e di degradazione (1° e 2° principio della termodinamica). L’energia è alla base di tutto, anche dei fenomeni psicologici ed Ostwald afferma che bisogna passare dalle ipotesi alle prototesi, essendo queste ultime delle ipotesi verificabili sperimentalmente. In particolare:
Ciò che udiamo trae origine dall’azione esercitata sul timpano dalle vibrazioni dell’aria. Ciò che vediamo è soltanto energia raggiante che esercita sulla retina un’attività chimica, la quale viene percepita come luce … Da questo punto di vista la totalità della natura ci si presenta come una serie di energie continuamente mutevoli nel tempo e nello spazio, delle quali abbiamo conoscenza nella misura in cui percuotono il nostro corpo, e specialmente gli organi di senso dotati di una forma adatta a ricevere le energie appropriate.
Ma, con ancora maggiore chiarezza, l’energetica era la panacea che faceva comprendere all’uomo tutto ciò che durante secoli si era affannato a cercare di conoscere:
il materialismo è incapace di rispondere alla questione di sapere come il corpo può arrivare a produrre lo spirito, che differisce totalmente da esso, e lo spiritualismo è impotente a confutare l’obiezione che il mondo, per il solo fatto che non si conforma alla nostra volontà, ma continua, molto spesso a nostre spese, per la sua strada, non dovrebbe essere una creazione del nostro spirito.
L’energetica permette, a mio avviso, di uscire da tutte queste difficoltà in una sola volta ed in un modo del tutto naturale, grazie al fatto che essa ha distrutto l’idea di materia … Non bisogna più preoccuparsi di come lo spirito e la materia possano agire l’una sull’altra; la questione che bisogna risolvere è quella di sapere in quale relazione la nozione di energia, che è molto più ampia di quella di materia, si incontri con la nozione di spirito.
In definitiva, mediante l’introduzione dell’energia nervosa e di quella psichica, Ostwald riconduceva la psicologia all’energetica. Così la coscienza ha delle basi energetiche ed anche la sociologia, intesa come rapporto tra individui, può essere ricondotta all’energetica. Su queste basi Ostwald metteva in discussione le ipotesi non verificabili dei meccanicisti. Una metafisica dell’energia! E quel che più conta è il grande seguito che queste idee avevano. Ma ancora più rilevante era l’estrapolazione che veniva fatta e che rispondeva a questa successione: fallimento del meccanicismo; la materia non esiste; superamento del materialismo nell’interpretazione del mondo.
Ed in questo vi fu una netta e chiara convergenza delle due correnti del fenomenismo: l’empiriocriticismo e l’energetica. L’empiriocriticismo ebbe il suo massimo esponente in E. Mach, che scrisse La Meccanica nel suo sviluppo storico critico nel 1883, libro fondamentale che rimetteva in discussione le intere basi della meccanica. Tale corrente di pensiero forniva all’energetica la critica puntuale, attenta e precisa della meccanica; l’energetica forniva all’empiriocriticismo l’unificazione della scienza sulla base della termodinamica. Ambedue si incontravano sull’antimeccanicismo che, con Hegel, diventava per loro antimaterialismo.
Ci troviamo nel pieno di ipotesi in libertà, formulando le quali nulla è dato per la loro verifica sperimentale e, quantomeno, non si capisce bene perché vengano formulate se non per servire da completamento della tesi di fondo. Così come quando Ostwald prendeva a prestito l’affermazione di Hertz (ben altrimenti motivata !) sul fatto che la teoria di Maxvell è il sistema delle equazioni di Maxwell: in questo non c’era altro che la volontà di screditare l’elaborazione maxwelliana che almeno in una prima fase, era strettamente legata agli strumenti ed ai metodi del meccanicismo (le analogie, i modelli, … ). Del resto si affiancava a questo il giudizio che un altro fenomenista, il fisico francese M.P. Duhem (1861-1916), dava dei lavori di Maxwell affermando che ciò che c’è d’essenziale nelle teorie di Maxwell sono le equazioni di Maxwell.

Duhem
Ma, poiché sono inaccettabili i metodi che hanno portato Maxwell a ricavare le sue equazioni, sarà almeno possibile, si domanda Duhem, mantenerle come punto di partenza per ricavare nuove teorie ? Ciò sarebbe lecito ad un matematico ma non ad un fisico poiché il fisico non può prescindere dall’ insieme delle ipotesi e dei ragionamenti con i quali è giunto alle equazioni in questione. Si negavano quindi i risultati sperimentali ma anche quanto sostenuto da Hertz. Non è vero che due teorie sono equivalenti, se conducono agli stessi risultati; occorre tener conto anche dei ragionamenti, delle ipotesi e dei metodi che hanno condotto a quei risultati. Così Duhem poteva continuare:
Non si possono dunque adottare le equazioni di Maxwell se non si ricavano da una teoria dei fenomeni elettrici e magnetici; e poiché queste equazioni non s’accordano con la teoria classica, che discende dai lavori di Poisson, sarà necessario respingere questa teoria classica, di rompere con la dottrina tradizionale e di creare con delle nozioni nuove, su delle ipotesi nuove, una teoria nuova dell’elettricità e magnetismo.
C’è qualcuno che abbia tentato questa strada ? Certamente, si rispondeva Duhem, e questi è Boltzmann il quale è riuscito a ricavare le equazioni di Maxwell in un modo logico.
Ma Duhem ha ancora dei dubbi, soprattutto perché:
Se per ricavare le equazioni di Maxwell in un modo logico, seguiamo i metodi proposti dal Sig. Boltzmann, ci vediamo costretti a dover abbandonare in parte l’opera di Poisson e dei suoi successori … una delle parti, cioè, più precise e più utili della fisica matematica. D’altra parte, per salvare queste teorie, dobbiamo rinunciare a tutte le conseguenze della teoria di Maxwell e, in particolare, alla più seducente di queste conseguenze, alla teoria elettromagnetica, della luce ?
Anche Poincaré, del resto, aveva notato l’impossibilità di rinunciare alla teoria elettromagnetica della luce. Come risolvere il problema ? Come venir fuori dal dilemma ? Ebbene, secondo Duhem, c’era un’altra teoria che ci avrebbe permesso di superare ogni difficoltà: si trattava della teoria di Helmholtz, esposta nel suo lavoro del 1870, Sulle equazioni del movimento dell’elettricità per corpi conduttori in moto. Questa teoria, sempre secondo Duhem, permetteva di conciliare logicamente l’antica elettrostatica, il vecchio magnetismo e la nuova teoria della propagazione delle azioni elettriche in mezzi dielettrici. Questa teoria
è un ampliamento naturale dei lavori di Poisson, d’Ampère, di Weber e di Neumann … ; senza perdere nessuna delle recenti conquiste della scienza elettrica, essa ristabilisce la continuità della tradizione.
Insomma, per Duhem, occorreva ripristinare la tradizione. Per far questo occorreva ritornare ad Helmholtz che, se da una parte era quello che ha dato il via alla energetica con il suo lavoro del 1847, Sulla conservazione della forza, dall’altra era certamente un atomista che vedeva appunto la corrente elettrica come flusso di corpuscoli. Il fenomenista Duhem ammetteva quindi le particelle che la sua corrente di pensiero respinge in modo deciso ? Certamente che no, anche se la logica, da Duhem più volte reclamata, ne soffre un poco. Nel suo Introduzione alla Meccanica Chimica (1893), Duhem sosteneva:
Perché cercare di sostituire delle costruzioni meccaniche ai corpi ed alle loro modificazioni, invece di considerarli per come i sensi ce li offrono, o piuttosto per come la nostra capacità di astrazione, lavorando sui dati sensibili, ce li fa concepire ? … Perché immaginarsi i cambiamenti di stato come degli spostamenti, delle giustapposizioni di molecole, dei cambiamenti di traiettoria, invece di caratterizzare un cambiamento di stato per il turbamento che provoca rispetto alle proprietà sensibili e misurabili di un corpo … ? … Queste riflessioni conducono a rovesciare il metodo finora seguito in fisica; … la teoria migliore sarà quella che non farà entrare nei suoi ragionamenti altre nozioni che non quelle che hanno un senso fisico, che siano direttamente misurabili … ; quella che non prenderà come principi che delle leggi di origine sperimentale … ; quella che si proporrà come fine non di spiegare i fenomeni ma di classificarli.
Ma c’è di più. Occorre far risaltare quanto già annunciato: la coerenza logica di Duhem. Da una parte si ammettevano le non sperimentabili particelle di Helmholtz, per rendere conto di ciò che della teoria di Maxwell interessava a Duhem, al fine di affermare la tradizione e la sua continuità nella fisica. Dall’altra si affermava la necessità di rovesciare il metodo finora seguito in fisica rinunciando a tutto ciò che come gli atomi non era né misurabile né sperimentabile.
Anche Duhem poi sentiva l’esigenza di trovare una scienza che si fosse posta come unificatrice rispetto alla fisica. E questa scienza era naturalmente la termodinamica, che ci permette di descrivere logicamente il mondo che ci circonda su una base perfettamente sperimentabile. In questo senso dunque Duhem si pone come uno tra i più convinti sostenitori dell’energetica anche se, per il vero, non raggiungeva gli eccessi metafisici e fanatici di Ostwald (situandosi più vicino a Mach che non allo stesso Ostwald). Anche Duhem avrà quindi una grossa parte nella polemica antimeccanicista, sull’altro fronte della quale si batteva, come già ricordato, il fisico austriaco L. Boltzmann.
Questi, subito dopo il congresso di Lubecca, introdusse alcuni brani significativi nel suo Lezioni sulla teoria dei gas (Lipsia, 1896-1898). Scriveva Boltzmann:
Sono convinto che questi attacchi sono basati puramente su un malinteso e che il ruolo della teoria dei gas nella scienza non sia ancora esaurito … Secondo me sarebbe una grande tragedia per la scienza se la teoria dei gas fosse temporaneamente dimenticata a causa di un momentaneo atteggiamento ostile verso di essa.
Del resto Boltzmann aveva sempre inteso che gli atomi non fossero altro che un’ipotesi, aggiungendo la considerazione (1886) che forse, un giorno, l’ipotesi atomica sarà sostituita da qualche altra ipotesi: ma non è molto probabile che ciò accada. Ed inoltre egli era convinto che :
noi ricaviamo l’esistenza delle cose unicamente dalle impressioni che esse incidono sui nostri sensi.
Conseguentemente, per fare scienza:
la via più diretta dovrebbe essere quella di partire dalle nostre sensazioni immediate per dimostrare come, per mezzo di esse, abbiamo ottenuto conoscenza dell’universo. Tuttavia, poiché questa via non sembra condurci al nostro scopo, dobbiamo seguire la via opposta, che è quella della scienza naturale.
Quindi Boltzmann contrapponeva il dato immediato dei nostri sensi al dato mediato della scienza naturale e ciò a causa del fatto che non s’intravede ancora il modo di fare scienza con il solo dato sensoriale immediato. Inoltre, per far scienza occorre una metodologia che sfrutti tutto quanto sia utile all’elaborazione teorica (analogie, modelli, … ), fatta salva la verifica sperimentale. Molto lucidamente scriveva Boltzmann:
Il compito principale della scienza è precisamente quello di costruire delle immagini che servano a rappresentare un insieme di fatti in modo tale che si possa predire da questi l’andamento di altri fatti simili. Naturalmente si intende che la previsione deve essere sempre verificata sperimentalmente. Probabilmente essa sarà verificata solo in parte. Vi è allora una speranza che si possano modificare e perfezionare le immagini in modo tale che esse rendano conto anche dei nuovi fatti.
In questo contesto una teoria meccanica ( e non una spiegazione meccanica) ha senso solo se è in grado di fornirci le leggi più semplici possibili mentre la fenomenologia non è altro che una pura illusione. Aggiungeva Boltzmann:
La fenomenologia ha creduto di poter rappresentare la natura senza, in alcun modo, andare al di la dell’esperienza, ma io penso che questa sia un’illusione. Nessuna equazione rappresenta con accuratezza assoluta un qualsiasi processo, ma lo idealizza sempre sottolineando certi aspetti comuni a più processi e trascurando ciò che è differente, andando in tal modo al di là dell’esperienza. E che ciò sia necessario, se vogliamo avere una qualche idea la quale ci permetta di predire un qualcosa nel futuro, discende dalla natura dello stesso processo intellettuale, che consiste appunto nell’aggiungere un qualcosa all’esperienza e nel creare una rappresentazione mentale che non è esperienza e che può pertanto rappresentare molte esperienze.
La posizione di Boltzmann era dunque in netta opposizione alla fenomenologia del suo tempo: occorre trascendere l’esperienza per poter avere una visione più generale del mondo che ci circondar e più andiamo al di là dell’esperienza e più sono sorprendenti i fatti che riusciamo a scoprire. Ma, avvertiva Boltzmann, l’andare al di là dell’esperienza in modo troppo audace può indurci in qualche errore. La fenomenologia pertanto non dovrebbe vantarsi di non andare al di là dell’esperienza, ma dovrebbe invece, semplicemente, diceva Boltzmann, ammonire a non compiere eccessi in tal senso. Ed in definitiva, ribadiva il nostro,
i migliori risultati si otterranno, senza dubbio, se potremo sempre fare uso di ogni immagine che sia necessaria, senza trascurare di mettere le immagini alla prova ad ogni passo, nei confronti di nuove esperienze.
Inoltre in questo modo non si sopravvaluteranno i fatti, essendo accecati dall’immagine, come spesso si argomenta contro gli atomisti. Ogni teoria, di qualunque tipo essa sia, porta ad una simile forma di cecità qualora sia seguita in modo troppo unilaterale.
Certamente Boltzmann era sostenuto, nel portare avanti le sue tesi, proprio dall’esperienza, da quanto cioè si andava realizzando, con la forza dell’ipotesi, in quegli anni (si pensi a Maxwell, a Lorentz, … ); altrettanto certamente egli era convinto della necessità di non produrre rotture radicali con il passato: l’unità concettuale della fisica andava mantenuta e questo non era certamente garantito dal fenomenismo e tanto meno dall’energetica. Era una posizione di grande onestà intellettuale quella di Boltzmana che si batteva, tra l’altro, per dare un senso alla ricerca scientifica. Nella conferenza di St. Louis del 1904 Boltzmann sostenne una posizione metodologica che, sfortunatamente ed efficientemente, la ricerca fisica del Novecento ed oltre, non farà sua:
Gli scienziati sono ora propensi a mostrare una spiccata predilezione per discutere tesi filosofiche, ed hanno tutte le ragioni per farlo. Una delle prime regole per la ricerca sulla natura è infatti quella secondo la quale non bisogna mai prestare una fiducia cieca nella verità con gli strumenti con i quali si lavora, ma bisogna invece analizzarli in tutte le direzioni … Se un progresso reale è possibile, lo si può attendere solamente da una collaborazione tra scienza e filosofia.
E su questa illusione, che si dovrà scontrare con i bisogni di efficienza che vengono indotti nella fisica dalle necessità produttive, si chiuderà, col suicidio a Duino, la vita di Boltzmann nel 1906.

L’epitaffio sulla tomba di Boltzmann è S = K.logW
Proprio nell’anno della morte di Boltzmann, Duhem, nel suo lavoro La teoria fisica (1906), sosteneva:
Queste due domande:
Esiste una realtà materiale distinta dalle apparenze sensibili ?
Di quale natura è questa realtà ?
non entrano affatto nel campo del metodo sperimentale; quest’ultimo non conosce altro che delle apparenze sensibili e non sa scoprire ciò che le supera. La soluzione di tali domande è trascendente rispetto ai metodi di osservazione di cui fa uso la Fisica, ed è oggetto della Metafisica.
Pertanto, se le teorie fisiche hanno come oggetto la spiegazione delle leggi sperimentali, la Fisica teorica non è una scienza autonoma: essa è subordinata alla Metafisica.
Anche Poincaré dirà la sua a proposito di energia e termodinamica e di come quindi egli si rapportava all’energetica(12). Scriveva Poincaré:
La teoria energetica presenta sulla teoria classica i vantaggi seguenti:
1°) Essa è meno incompleta; cioè, i principi della conservacene dell’energia e di Hamiton ci insegnano più dei principi fondamentali della teoria classica ed escludono certi movimenti non realizzati dalla natura e compatibili con la teoria classica. 2°)Essa ci dispensa dall’ipotesi degli atomi, quasi impossibile da evitare con la teoria classica. Ma solleva a sua volta nuove difficoltà: le definizioni di due specie di energia sono appena più facili di quelle della forza e della massa nel primo sistema.
Inoltre, poiché nella conservazione dell’energia occorre tener conto di tutte le varie forme di energia bisognerà considerare anche l’energia interna molecolare (Q), sotto forma termica, chimica o elettrica. Così, se indichiamo con T l’energia cinetica e con U quella potenziale, possiamo scrivere il principio di conservazione dell’energia nella forma seguente:
T + U + Q = costante.
Tutto andrebbe bene se i tre termini fossero assolutamente distinti, se T fosse proporzionale al quadrato della velocità, U indipendente da queste ultime e dallo stato dei corpi, Q indipendente dalle velocità e dalle posizioni dei corpi e dipendente soltanto dal loro stato interno … Ma non è così. Consideriamo dei corpi elettrizzati; l’energia elettrostatica dovuta alla loro mutua azione, dipenderà evidentemente dalla loro carica, cioè dal loro stato; ma essa dipenderà anche dalla loro posizione. Se questi corpi sono in movimento, agiranno l’uno sull’altro elettrodinamicamente e l’energia elettrodinamica dipenderà non soltanto dal loro stato e dalla loro posizione, ma anche dalle loro velocità. Non abbiamo più dunque alcun mezzo per fare la cernita dei termini che devono far parte di T, di U e di Q, e di separare le tre parti dell’energia.
L’unica cosa che possiamo dire è allora che vi è una certa funzione
f ( T + U + Q )
che rimane costante e nessuno ci autorizza a ritenere che questa particolare funzione, che si chiamerebbe energia, è nella forma
T + V + Q = costante.
In definitiva la corretta enunciazione del principio di conservazione dell’energia è: vi è qualcosa che rimane costante.
Sotto questa forma, esso si trova a sua volta fuori degli attacchi dell’esperienza e si riduce ad una specie di tautologia. E’ chiaro che se il mondo è governato da leggi, vi saranno delle quantità che rimarranno costanti. Come accade per il principio di Newton e per una ragione analoga, il principio della conservazione dell’energia, fondato sull’esperienza, non potrà più essere infirmato da essa. Questa discussione mostra che, passando dal sistema classico al sistema energetico, si è realizzato un progresso; ma essa mostra altresì che questo progresso è insufficiente.
Occorre rifarsi a principi generali, che sono cinque o sei, poiché la loro
applicazione … ai differenti fenomeni fisici basta per insegnarci ciò che ragionevolmente possiamo aspettarci di conoscere di una cosa … Questi principi sono il risultato di esperienze sommamente generalizzate, e dalla loro stessa generalità sembrano acquistare un grado elevato di certezza. In effetti, quanto più generali sono, tanto più frequentemente si ha l’occasione di metterli alla prova, e moltiplicandosi le verifiche, assumendo le forme più diverse e più insperate, finiscono per non lasciar posto a dubbi.
Ma, allo stato presente, questi principi mostrano alcune crepe che occorre chiudere al più presto in qualche modo. Una miriade di fatti sperimentali sembra non accordarsi con essi. Consideriamoli uno ad uno e vediamo dove essi sembrano cadere in difetto.
– Secondo Principio della termodinamica
Osservazioni recenti, più accurate, del moto browniano e la spiegazione datane dal matematico tedesco C. Wiener (1826-1896) nel 1863 e dal chimico britannico W. Ramsay (1852-1916) nel 1876 mostravano che in un mezzo in equilibrio termico (una soluzione colloidale) del calore viene trasformato spontaneamente in lavoro (delle particelle in sospensione nella, soluzione si muovono rapidamente da una parte e dall’altra, con maggiore velocità quanto più sono piccole). Questo fenomeno sembra negare la validità del 2° principio.
– Primo Principio della termodinamica
Da quando P. Curie (1869-1906) e M. Curie (1867-1934) hanno posto del radio in un calorimetro ed hanno osservato che la quantità di calore, prodotta incessantemente, era notevole, il principio di conservazione dell’energia sembra in grave difetto.
Dopo aver individuato le carenze che io qui ho riportato alle quali ne vanno aggiunte molte altre che egli fa e riguardanti un poco tutta la fisica(11), Poincaré formulava un accorato appello:
E’ necessario che non si abbandonino i principi prima di aver fatto uno sforzo leale per salvarli.
Ed aggiungeva:
E’ inutile accumulare ipotesi, poiché non si possono soddisfare in una volta. tutti i principi. Pino ad ora non si è riusciti a salvaguardarne alcuni senza sacrificarne degli altri, ma la speranza di ottenere migliori risultati non è del tutto persa.
Com’è possibile far ciò ? La risposta a questa domanda permetteva a Poincaré di scrivere la seguente proposizione di grande interesse:
Forse … dovremmo costruire tutta una nuova meccanica che non facciamo altro che intravedere, nella quale, aumentando l’inerzia con la velocità, la velocità della luce diventerebbe un limite insuperabile. La meccanica ordinaria, più semplice, rimarrebbe come una prima approssimazione, dato che sarebbe vera per velocità non molto grandi, di modo che ancora torneremmo a trovare l’antica dinamica al di sotto della nuova.
Come risulta evidente, la critica di Poincaré era molto attenta agli sviluppi della fisica, ed il fisico-matematico francese, anche se non faceva il passo definitivo, aveva intuito tutti i problemi che investivano il mondo della fisica. Ben altra classe rispetto agli Ostwald o Duhem.
Roberto Renzetti
PS. Nel prossimo lavoro sarà necessario dare una panoramica delle ricerche e delle memorie di differenti scienziati. Nel trattare i giganti della fisica dell’Ottocento ho trascurato moltissimi scienziati di grandissimo rilievo. Tenterò un recupero.
NOTE
(0) Il Principio di Minima Azione afferma che la quantità di azione (il prodotto della quantità di moto per lo spazio percorso) richiesta perché si realizzi qualsiasi processo naturale sia la più piccola possibile
(1) Le altre memorie di Boltzmann fino al 1872 ed incentrate sulla teoria cinetica dei gas (particolarmente le due scritte in grassetto) sono:
– Lösung eines mechanischen Problems, Wiener Berichte, 58, 1035-1044; 1868b.
– Zur Priorität der Auffindung der Beziehung zwischen dem zweiten Hauptsatze der mechanischen Wärmetheorie und dem Prinzip der kleinsten Wirkung, Annalen der Physik, 143, 211-230; 1871a.
– Über das Wärmegleichgewicht zwischen mehratomigen Gasmolekülen, Wiener Berichte, 63, 397-418; 1871b.
– Einige allgemeine Sätze über Wärmegleichgewicht, Wiener Berichte, 63, 679-711; 1871c.
– Analytischer Beweis des zweiten Hauptsatzes der mechanischen Wärmetheorie aus den Sätzen über das Gleichgewicht der lebendigen Kraft, Wiener Berichte, 63, 712-732; 1871d.
(2) Il teorema ergodico si può enunciare nel modo seguente: tanto più è grande il numero di stati microscopici di un sistema che ci danno uno stesso stato termodinamico macroscopico, quanto più è probabile che, se noi andassimo ad osservare il sistema in un determinato istante, troveremmo quello stato (si osservi che affermare quanto abbiamo ora detto, equivale a dire che gli eventi si svolgono nella direzione verso cui è più probabile si svolgano).
(3) Riporto alcune osservazioni che fa Khun in una sua nota a proposito dell’uso della lettera H per tale funzione. Non era questa la lettera utilizzata da Boltzmann nella sua memoria del 1872 (ed almeno fino al 1877) ma era E. Questa E nasceva dal fatto che si pensava una qualche parentela della funzione che la E rappresentava con la nascente Entropia che ha appunto una E come iniziale. Si capì più avanti che mentre la E diminuiva quando un gas va verso l’equilibrio, l’entropia aumentava. Sembrava inopportuno mettere un segno meno per regolare le cose. Il tutto sembra sia nato a seguito della convenzione del segno che lo stesso Clausius, ad un dato momento, cambiò.
(4) Si veda in proposito il paragrafo Gli ultimi lavori dell’articolo su Maxwell.
(5) La traduzione che sto usando è quella di Baracca, Russo e Ruffo in Scienza ed Industria. Il traduttore pone a questo punto la nota seguente:
Qui e nel seguito del brano usiamo questa dizione (o altre analoghe) tra parentesi quadre in luogo della relazione matematica
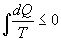
usata da Boltzmann nel testo originale. Ciò solo al fine di consentire una miglior comprensione del testo. Naturalmente dove si parla di diminuzione di entropia si deve intendere che nella relazione scritta sopra il segno ≤ è cambiato in ≥. Il fatto che l’entropia deve sempre aumentare nei processi naturali è un modo di esprimere il secondo principio della termodinamica.
(6) L’importanza dello spazio delle fasi, come ricorda Segrè, poggia su un teorema, scoperto da Liouville, secondo cui il volume dello spazio delle fasi occupato da un certo gruppo di punti rappresentativi non cambia nel tempo. In altri termini si può dire che i punti rappresentativi si muovono nello spazio delle fasi come un fluido incompressibile. Inoltre, poiché l’energia si conserva, i punti rappresentativi sono confinati su ipesuperfici di energia costante. L’ipotesi fondamentale è allora quella che tutti gli elementi di volume dello spazio delle fasi sono equiprobabili.
(7) Vediamo, con calcoli oggi in uso, come è possibile calcolare la distribuzione di Boltzmann utilizzando i metodi del calcolo delle probabilità e lo spazio delle fasi.
Supponiamo di avere un gas di molecole. Sia N il numero totale di molecole ed E la loro energia totale.
Il problema della statistica fisica è di distribuire la quantità assegnata E di energia fra le N molecole. Posto che un certo numero di molecole avrà energia E0, un certo numero E1, un certo numero E2, …, un certo numero En (con E1 + E2 + … + En = E), il problema è di calcolare la funzione di distribuzione, cioè, come E va distribuita fra le N particelle. Si vuole in definitiva determinare tutte le possibili distribuzioni dell’energia fra le N molecole (in modo che l’energia totale sia sempre E) .
Poiché distribuzioni (microscopicamente) diverse non necessariamente corrispondono a stati macroscopici distinguibili, il problema della statistica è determinare qual è lo stato macroscopico che può essere realizzato con il massimo numero di stati microscopici. Chiameremo tale stato macroscopico stato di equilibrio del sistema.
Per facilitare i ragionamenti che svolgeremo, immaginiamo che il volume occupato dal gas sia diviso in tante cellette che chiameremo Z1 , Z2 , … , ZM (queste cellette le supponiamo di ugual volume e in numero finito M). Queste cellette debbono essere pensate tanto piccole da confondersi con un punto. Aggiungiamo poi che in ogni punto del nostro volume potremo avere più di una celletta (spazio delle fasi a più dimensioni) secondo il criterio seguente: in ogni punto del nostro volume si avranno tante cellette quante sono le possibili velocità delle molecole (naturalmente a velocità diverse corrispondono energie diverse) del gas (infatti in ogni punto è possibile che si trovino molecole con differenti velocità)[anche se in un punto vi fosse una sola molecola di energia ½ mv2, in uno spazio tridimensionale sorgerebbero egualmente complicazioni dovendosi tenere in conto che una data energia ½ mv2 può essere ottenuta da molte combinazioni delle componenti vx , vy e vz di v. Si dovrebbe allora avere l’elasticità mentale di pensare il nostro punto (in cui si trova la molecola di energia ½ mv2) occupato o da una molecola con energia ½ mv2 originata da una particolare combinazione di vx , vy e vz , o da una molecola con la stessa energia ma originata da una diversa combinazione di vx , vy e vz, o da … ecc. Quindi, a parità di energia per la molecola, moltissimi valori diversi possono assumere le componenti della sua velocità. E’ chiaro che più è grande l’energia della molecola, in più modi si può ottenere da differenti combinazioni di vx , vy e vz].
La situazione può essere “letta” così: in un particolare stato macroscopico del gas in considerazione (una particolare terna P, V, T) , composto da N molecole identiche ma distinguibili (e quindi numerabili: 1, 2, …, N), n1 molecole si trovano nello stato 1 di energia E1, n2 molecole si trovano nello stato 2 di energia E2, … , nM molecole si trovano nello stato M di energia EM originando così il primo possibile stato del sistema.
Al variare quindi della individualità delle molecole che occupano un determinato stato microscopico otteniamo tutti i possibili stati microscopici che ci danno lo stesso stato macroscopico.
Se si vuole uno stato macroscopico diverso (una diversa terna P, V, T) si debbono cambiare i numeri nj di occupazione [osserviamo a parte che la pressione e la temperatura di un gas sono grandezze statistiche medie (relativamente all’enorme numero di molecole componenti il gas stesso) che noi usiamo per caratterizzare lo stato macroscopico del gas].
Chiamiamo allora con Pi il numero di stati del sistema; e tanto più è grande Pi, cioè tanto più è grande il numero di stati microscopici del sistema che ci danno uno stesso stato termodinamico macroscopico, quanto più è probabile che, se noi andassimo ad osservare il sistema in un determinato istante, troveremmo quello stato (si osservi che affermare quanto abbiamo ora detto, equivale a dire che gli eventi si svolgono nella direziono verso cui è più probabile si svolgano e questo è il teorema ergodico).
Se si ha un sistema (isolato) in esso avvengono solo quelle trasformazioni che lo portano verso lo stato a cui compete la massima probabilità (stato più stabile del sistema) e ciò è sempre vero ogniqualvolta il numero N dei componenti del sistema è grandissimo e nel nostro caso (molecole di un gas) la cosa è sempre verificata.
Cominciamo col dire che il numero di permutazioni di N molecole è N! Così operando, però, si includono anche i casi in cui vengono permutate le molecole di una stessa celletta; poiché queste permutazioni non rappresentano nuove possibilità di realizzazione della distribuzione considerata si deve dividere N! per il numero n1! di permutazioni nella prima cella, per il numero n2! di permutazioni nella seconda cella, e così via, ottenendo allora per il numero di possibilità di realizzazione di una certa distribuzione (probabilità termodinamica):
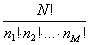
Se si fanno poi variare i numeri n1, n2 , …, nM questa espressione ci dà il numero di possibilità di realizzazione di altre distribuzioni.
Per avere ora la probabilità di una certa distribuzione
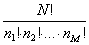
si deve moltiplicare ancora questo numero per la probabilità a priori della distribuzione (data dall’inverso 1/P del numero totale P di distribuzioni possibili); questa probabilità a priori è data dal prodotto:
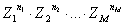
In definitiva la probabilità matematica di una certa distribuzione è data da:

essendo:
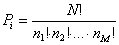
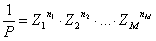

A questo punto è utile introdurre la formula di Stirling che rende più semplici i calcoli da svolgere. Per a molto grande vale la relazione:
a ! = a a
Per cui la relazione che ci dà W diventa:
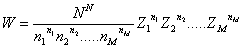
Passando ora ai logaritmi dei due membri si ha:
log W = N log N – n1 log n1 – n2 log n2 – … – nM log nM + n1 log Z1+ n2 log Z2 + . . . + nM log ZM =>
log W = N log N + n1 (log Z1 – log n1) + n2 (log Z2 – log n2 ) + … + nM(log ZM – log nM) =>
log W = N log N +n1 log Z1/n1 +n2 log Z2/n2 + … + nM log ZM/nM .
Poiché sappiamo che lo stato in cui si troverà il gas sarà quello a cui compete la massima probabilità, dobbiamo calcolare il valore massimo di log W.
E’ un problema di massimo assoluto (sotto le condizioni di costanza del numero totale di particelle e dell’energia)
Si ni = N con (N = n1 + n2 + … + nM)
Si ni Ei = E con (E = n1E1+ n2E2 + … + nMEM)
di una funzione a più variabili (ni) che si risolve normalmente con il metodo dei moltiplicatori di Lagrange.
Per il calcolo si tenga conto che n e Z sono grandezze costanti e che, per quanto abbiamo detto prima:
Si dni = 0
Si Ei dni = 0.
Cominciamo con il trasformare l’ultima espressione trovata per log W nel modo seguente:
log W = N log N + Σi ni log Zi/ni.
Tenendo anche conto che
N log N = costante
si può scrivere
log W = costante + Si ni log Zi/ni.
Usando quindi il metodo dei moltiplicatori di Lagrange sotto le condizioni date si ha:
d (log W) = 0
(*) d (log W) – α Si dni – β Si Ei dni = 0
dove i coefficienti – α e – β sono da determinarsi in base alle condizioni di costanza di N ed E.
Differenziando rispetto ad ni l’espressione che ci dà log W troviamo:
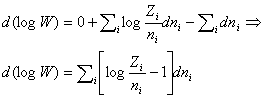
Inserendo quest’ultima espressione nella (*) si ha :

Fino a questo punto era implicito in quanto dicevamo che le operazioni su N, Z ed E erano valide all’interno di ogni intervallo di energia. Ma noi dobbiamo arrivare ad una espressione che abbia valore indipendentemente per ciascuno degli intervalli di energia dati. Ciò vuol dire che nell’espressione che dobbiamo trovare possiamo eliminare la sommatoria e riferirci ad una generica espressione i:

avendo chiamato con C la quantità costante tra parentesi tonda. Con ovvio simbolismo, la precedente espressione si può anche scrivere:
n (Ei) = Z (Ei) . C . e–bEi
dove C e β sono le costanti che si possono determinare con le due condizioni ausiliarie di costanza di N e di E. A questo punto si potrebbe dimostrare che β vale 1/ kT, ma i conti sono complessi e noi ci accontentiamo del risultato. In definitiva, la relazione scritta è l’espressione di Maxwell-Boltzmann, la quale, ricordiamolo, ci fornisce le possibili distribuzioni di una energia (totale) E fra un insieme di N molecole:
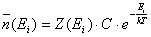
(**)
dove: il primo termine sta per il numero di molecole che possiedono energia Ei (la barra sopra ad n sta per “numero medio”); Z (Ei) = numero di stati (cellette) del sistema a cui compete energia Ei , o meglio, densità degli stati per unità di energia e di volume; C = costante che si può determinare imponendo che la somma di tutte le molecole è costante ed uguale ad N; k = costante di Boltzmann = 1,38 . 10-16 erg/grado; T = temperatura assoluta a cui si trova il sistema.
La relazione scritta ci dice che il numero numero medio di molecole che ha energia Ei , dipende dal numero di stati a cui compete energia Ei e decresce esponenzialmente all’aumentare dell’energia Ei; in altre parole: fra celle di uguali dimensioni quelle con energia maggiore sono meno popolate di quelle con energia minore; in altre parole ancora: in un gas ad una data tempera tura T, una data molecola passerà una parte maggiore del suo tempo in stati di energia inferiore che in sta ti di energia superiore.
(8) Nel suo lavoro semplificato e successivo, Vorlesungen über Gastheorie (Lectures on Gas Theorie, Lipsia 1896 e 1898), Boltzmann discuterà lo stesso argomento a partire dalla ricerca di una spiegazione della sua funzione H:
[…] Facciamo qualche osservazione sul significata della quantità H. Questo significato è doppio. Il primo è matematico, il secondo fisico. Discuteremo il primo solo in un caso semplice, un solo gas in un recipiente di volume unitario. Naturalmente saremo in grado di semplificare le conclusioni usando questa assunzione, sebbene dobbiamo anche rinunciare ad una dimostrazione simultanea della legge di Avogadro.
Facciamo in prima luogo alcune osservazioni preliminari sui principi del calcolo delle probabilità. Da un’urna, in cui sono poste molte sfere nere ed un ugual numero di sfere bianche ma per il resto identiche, facciamo 20 estrazioni puramente a caso. Il caso in cui si estraggano solo palle nere non è per nulla meno probabile del caso in cui alla prima estrazione si ottenga una sfera nera, alla seconda una bianca, alla terza una nera, eccetera. Il fatto che sia più verosimile ottenere 10 sfere nere e 10 sfere bianche in 20 estrazioni di quanto non sia ottenere 20 sfere nere è dovuta al fatta che il primo evento può accadere in un numero molto maggiore di modi del secondo. La probabilità relativa del primo evento a paragone del secondo è il numero 20!/10!10!, il quale indica quante permutazioni si possono fare dei termini nella serie di 10 sfere bianche e 10 nere, trattando le varie sfere bianche come identiche tra loro, e le varie sfere nere come identiche tra loro. Ciascuna di queste permutazioni rappresenta un evento che ha la medesima probabilità dell’evento di tutte sfere nere. Se vi fosse nell’urna un grande numero di sfere identiche per gli altri aspetti, delle quali un certo numero fossero bianche, un ugual numero nere, un ugual numero blu, un ugual numero rosse, e cosi via, allora la probabilità di estrarre a sfere bianche, b sfere nere, c sfere blu, eccetera, è

(*)
volte la probabilità di estrarre sfere di un solo colore.
Proprio come in questo semplice esempio, l’evento che tutte le molecole in un gas abbiano esattamente la stessa velocità nella stessa direzione non è per nulla meno probabile dell’evento che ogni molecola abbia esattamente la velocità e la direzione del moto che essa possiede realmente ad un istante particolare nel gas, Ma se paragoniamo il primo evento con l’evento che valga nel gas la distribuzione delle velocità di Maxwell, troviamo che vi sono innumerio come in precedenza considerammo l’estrazione di una sfera nera o bianca o blu come ugualmente probabile. Al posto di a, il numero di estrazioni di sfere bianche, abbiamo ora il numero n1ω di molecole la cui velocità giace nel primo dei nostri elementi di volume; invece di b, abbiamo il numero n2ω di molecole la cui velocità giace nel secondo elemento di volume ω, e cosi via. Al posto dell’equazione (*) abbiamo

(**)
per la probabilità relativa che la velocità di n1ω molecole giacciano nel primo elemento di volume, e cosi via. Allora n = (n1 + n2 + n3 + … )ω è il numero totale di tutte le molecole nel gas. Per esempio, l’evento che tutte le molecole possiedano velocità uguali e dirette nella stessa direzione corrisponde ad avere tutte le velocità giacenti nella stessa cella. In tal caso avremmo Z = n!/n! = 1; nessun’altra permutazione è possibile. Risulta già molto più probabile che metà delle molecole abbia una particolare velocità e direzione, e l’altra metà abbia un’altra velocità e direzione, rispetto al caso in cui tutte possiedano la medesima velocità e direzione. Allora metà delle velocità sarebbero in una cella e metà in un’altra, cosicché

eccetera […].
[…] Il teorema della sezione precedente, che stabilisce che H decresce a causa delle collisioni, dice semplicemente che a causa delle collisioni la distribuzione delle velocità delle molecole del gas si avvicina sempre più a quella più probabile, non appena lo stato è in condizioni di disordine molecolare, e perciò si introduce il calcolo delle probabilità. […]
In connessione con quanto precede, dovremmo menzionare il punto seguente, già messo in luce tempo fa da Loschmidt: Supponiamo che un gas sia racchiuso da pareti elastiche perfettamente lisce. Inizialmente vi sia uno stato improbabile ma in condizioni di disordine molecolare – per esempio, tutte le molecole abbiano la stessa velocità c. Dopo un certo tempo, si stabilirà in buona approssimazione la distribuzione delle velocità di Maxwell. Immaginiamo ora che all’istante t, la direzione della velocità di ogni molecola sia rovesciata, senza mutarne la grandezza. Il gas passerà ora attraverso la stessa sequenza di stati all’indietro. Abbiamo perciò il caso in cui una distribuzione più probabile evolve a causa delle collisioni verso una meno probabile, ed in cui la quantità H aumenta come risultato delle collisioni. Ciò non contraddice in alcun modo quanto fu dimostrato [che H non può aumentare] l’assunzione fatta in quel caso che lo stato fosse di disordine molecolare non è rispettata qui, poiché dopo l’esatto rovesciamento di tutte le velocità ogni molecola non collide con altre secondo le leggi della probabilità, ma piuttosto essa deve collidere nel modo calcolato precedentemente. […]
Il fatto che H ora aumenti non contraddice neppure le leggi della probabilità; poiché queste predicono solo l’improbabilità, non l’impossibilità, di un aumento di H. Invero, segue al contrario esplicitamente che ogni distribuzione di stati, anche se molto improbabile, possiede una probabilità diversa da zero, anche se molto piccola. In modo simile, quando si ha una distribuzione di Maxwell, il caso in cui una molecola abbia la velocità che essa possiede attualmente a quell’istante, similmente per la seconda, terza ed altre molecole, non è affatto più probabile del caso che tutte le molecole abbiano la stessa velocità.
Sarebbe chiaramente un errore grossolano concludere che qualsiasi moto per il quale H decresce sia equiprobabile con uno in cui le velocità sono rovesciate ed H aumenta. Consideriamo un qualsiasi moto per il quale H decresca dall’istante t0 all’istante t1. Quando si rovescino tutte le velocità all’istante t0, non si potrebbe in alcun modo arrivare ad un moto per il quale H debba aumentare; al contrario, probabilmente H diminuirebbe ancora. E solo quando si rovesciano le velocità all’istante t1 che si ottiene un moto per il quale H deve aumentare durante !’intervallo di tempo t1 – t0 , ed anche allora H probabilmente diminuirebbe ancora dopo di esso, cosicché i moti per i quali H rimane ininterrottamente molto vicino al suo valore minimo sono di gran lunga i più probabili. I moti per i quali essa aumenta fino a valori considerevolmente alti, o si abbassa da un valore grande al suo valore minimo, sono ugualmente improbabili; si sa tuttavia che H possiede molti valori più grandi durante un intervallo di tempo definito, cosicché essa deve diminuire con molta probabilità. […]
(9) Presento un modo per ricavare la connessione tra entropia e probabilità utilizzando calcoli oggi in uso che semplificano un poco quelli di Boltzmann.
Per trovare quel legame cercato da Boltzmann tra la meccanica statistica e la termodinamica occorre osservare che mentre dal punto di vista della prima lo stato stabile di un sistema di data energia è quello cui compete il valore massimo della probabilità di realizzazione P, dal punto di vista della seconda, tale stato è quello a cui compete il valore massimo dell’entropia S. Il fatto che si verifichi ciò induce a pensare che debba esistere una qualche relazione che leghi entropia e probabilità, un qualcosa del tipo:
(1) S = f(P)
Per determinare f(P) consideriamo un sistema composto da due sottosistemi tra loro indipendenti e siano S1 ed S2 le entropie e P1 e P2 le probabilità degli stati stabili di questi sottosistemi. Si può allora scrivere:
S1 = f(P1) S2 = f(P2)
Ricordo ora che l’entropia del sistema totale è la somma tra le entropie dei sottosistemi mentre la probabilità di tale sistema è il prodotto tra le probabilità dei sottosistemi:
S = S1 + S2
P = P1.P2
Mettendo insieme questa relazione e la (1) si ottiene:
f(P1.P2) = f(P1) + f(P2)
che è un’equazione funzionale del tipo:
(2) f(x.y) = f(x) + f(y)
e poiché esiste questa proprietà è possibile determinare la forma di tale funzione. Essendo la (2) valida per qualsiasi x ed y, si può porre y = 1 + ε, con ε infinitesimo del primo ordine. Si avrà allora:
f(x + xε) = f(x) + f(1 + ε)
Da questa espressione è possibile sviluppare entrambi i membri in serie di Taylor. Trascurando tutti i termini di ordine superiore al primo si trova:
f(x) + xεf'(x) = f(x) + f(1) + εf'(1)
Per ε = 0 risulta f(1) = 0, da cui:
xf'(x) = f'(1) = c
con c una costante. Da questa espressione si ricava:

ed integrando si ha:
f(x) = c.logx + cost
Di conseguenza la (1) si può scrivere:
(3) S = c.logP + cost.
Se quindi esiste una relazione funzionale tra entropia e probabilità, tale relazione deve essere necessariamente del tipo della (3).
In pratica si preferisce spesso modificare lievemente la definizione statistica dell’entropia assumendo come tale la relazione:
(4) S = c.logW
dove W rappresenta non la probabilità ma il numero di modi diversi in cui un microstato di un sistema può essere realizzato. Ricordando che W (che si può chiamare peso dello stato) risulta definita a meno di una costante moltiplicativa arbitraria, ne segue che la (4) definisce ancora l’entropia S a meno di una costante additiva.
Per determinare la c che compare nella (4) ricordiamo che nella ripartizione più probabile dell’energia si ha che per ogni sistema di energia E la grandezza ω(E), e quindi la W(E) ad essa proporzionale, soddisfa la seguente equazione:
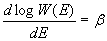
dove β è una costante che determinata altrove assume il valore β = 1/KT . Si ha quindi:

Per la (4) seguirà:
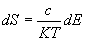
(5)
D’altra parte dalla definizione stessa dell’entropia per via termodinamica:

tenendo conto che la quantità di calore Q non è altro, nel nostro problema, che l’energia E del sistema (per cui dQ = dE) si avrà:
(6)
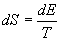
Confrontando la (5) e la (6) si ottiene:
c = K
L’espressione statistica dell’entropia diverrà pertanto:
(7) S = K.logW
dove K è la costante di Boltzmann che assumerà rilievo quando in essa Planck riconoscerà alcune proprietà.
(10) Non si può trattare questo argomento senza introdurre lo stimolante saggio di Ciccoti e Donini trattato in Sviluppo e crisi del meccanicismo: da Boltzmann a Planck e pubblicato in L’ape e l’architetto (1976):
1.
Il problema che qui si tratta può essere considerato parte di un programma, che ha per scopo la comprensione del perché e di come mutano le idee nella scienza. Avendo ben presente l’insufficienza della storia interna, nelle sue varie forme, come meccanismo di spiegazione delle trasformazioni della teoria e della pratica scientifica, ci si propone di caratterizzare, su un caso particolare, gli elementi fondamentali dello scontro culturale, ideale e politico, che sta oggettivamente dietro ogni mutamento radicale del pensiero scientifico e che pertanto può essere ricostruito mediante l’analisi storica. Si vedrà cosi come un ambiente selezionato – la comunità scientifica – raccogliendo gli stimoli che provengono dall’ambiente esterno alla comunità, possa tradurli in una proposta scientifica di conoscenza della natura, coerente alle esigenze dei rapporti di produzione dominanti nella società.
Questo programma non ha molto interesse se preso isolatamente, ma lo acquista se lo si considera come uno dei livelli necessari alla chiarificazione del problema della funzione sociale della scienza. Schematizzando al massimo, si possono individuare altri due livelli fondamentali: quello delle relazioni tra organizzazione e istituzioni della ricerca scientifica e istituzioni sociali di riferimento; quello della politica della scienza come formulazione di un progetto e soluzione del problema della sua gestione (con quali forze sociali, a quali livelli istituzionali, ecc.). Quest’ultimo aspetto ha senso solo se riferito al presente, ma proprio la capacità di fondare l’interpretazione storica del passato può dargli consistenza; viceversa, solo in relazione al presente gli altri due livelli acquistano significato e forniscono il nucleo di condensazione di una teoria della riappropriazione della ricerca scientifica e dei suoi risultati a precise finalità di classe.
2.
Tornando all’aspetto, che qui si considera come principale, vogliamo discutere un caso storico di notevole interesse per la comprensione della dinamica inerente alla crescita della conoscenza scientifica. Esso è fornito da quello che potremmo chiamare il problema della nascita della meccanica quantistica; è del resto quasi banale sottolineare che la questione dei rapporti tra meccanica classica e quantistica presenta ancora alcuni aspetti di attualità, sicché l’integrazione complessiva dei tre livelli, di cui dicevamo sopra, è qui tanto più manifesta.
Più esplicitamente, ci pare che proprio la rilevanza nel presente dei problemi legati alla meccanica quantistica possa dare il significato giusto allo sforzo di definirne storicamente il carattere. Se osserviamo il quadro ufficiale della scienza contemporanea (e in particolare della fisica), vediamo che in esso è stata apparentemente riassorbita tutta la tensione del dibattito accesosi attorno agli atteggiamenti epistemologici peculiari della meccanica quantistica. Nella prima metà del secolo, sia i filosofi che gli stessi scienziati si erano profondamente accapigliati attorno a questioni che andavano dalla causalità alla possibilità di un determinismo rigoroso o all’irriducibile presenza del caso nelle relazioni fisiche; il panorama attuale vede invece una santificazione pressoché totale dei paradigmi scientifici, fondamento indiscusso dell’attuale formulazione della fisica. Di qui deriva un doppio ordine di problemi: da un lato, diventa necessario capire perché le caratteristiche determinate di questa fase storica si proiettino nel dominio di una scienza oggettivata e neutrale, che ha largamente rimosso come marginali i problemi di riflessione sui propri fondamenti epistemologici; d’altro lato, occorre saper finalizzare lo stesso dibattito sulla scienza per ricondurlo all’interno di un progetto complessivo di rovesciamento degli attuali rapporti di classe.
Noi non intendiamo affrontare qui in modo diretto tali questioni; pensiamo però che esse debbano costituire il punto di riferimento dichiarato per capire il senso della discussione sulla nascita della meccanica quantistica, cui ci accingiamo. Non si tratta cioè di cimentarsi con un particolare problema storico, per convalidare l’affermazione di metodo dell’insufficienza di un’analisi condotta solo all’interno della scienza, di cui dicevamo all’inizio, quanto piuttosto di arricchire gli strumenti, con cui orientarsi sui presupposti sociali e ideologici della fisica teorica contemporanea e sul significato quindi delle tendenze che in essa si sviluppano.
Per precisare meglio la rilevanza attuale del problema vogliamo ricordare che, accanto al ruolo di predominio indiscusso esercitato entro la fisica occidentale, la meccanica quantistica si è affermata come struttura portante anche in Unione Sovietica1. Un lungo e accanito dibattito sulla compatibilità dei suoi fondamenti con il materialismo dialettico si è risolto in una riconciliazione piena, che – se già era operante nella prassi, perché molti fisici teorici sovietici anche negli anni Trenta e Quaranta utilizzavano la meccanica quantistica, spesso astenendosi dall’impegnarsi sulle scelte ideologiche – e divenuta ora anche una teorizzazione ufficiale di ortodossia. D’altra parte, anche in occidente e in particolare in Italia, esistono sul problema della scienza posizioni diverse, che pure si richiamano in vario modo al marxismo; la questione centrale, rilanciata con forza dal nuovi livelli di autonomia anticapitalistica espressi nella lotta di classe di questi ultimi anni2, si estende dai progetti di riappropriazione alle ipotesi di scienza alternativa, al rifiuto semplicistico della scienza del capitale. Rispetto a tutto questo diventa essenziale discutere se la scienza si sia sviluppata e si sviluppi in un arricchimento – oggettivamente progressivo – di conoscenze, pur subordinate a fini distorti; oppure se le successive sistemazioni siano connesse in modo essenziale a scelte ideologiche indotte dalle finalità storico-sociali e ne portino quindi in sé tutti i segni di classe.
3.
Vediamo dunque come si pone il problema della nascita della meccanica quantistica. Alla fine dell’Ottocento entro il quadro della fisica spiccano soprattutto due problemi: da un lato, il rapporto tra termodinamica e meccanica statistica: dall’altro, rispetto alla sistemazione ormai compiuta dell’elettromagnetismo con la formulazione della teoria di Maxwell, la questione dell’esistenza dell’etere e, più in generale, del rapporto tra fenomeni ondulatori e meccanica.3
Il problema, di cui ci occuperemo, è legato per certi versi a entrambi gli aspetti; infatti, !’ipotesi di Planck sulla necessità di ammettere che l’energia di certi sistemi non vari in modo continuo, ma assuma solo valori discreti, multipli di un’unità fondamentale (il “quanto,” appunto), scaturisce dallo studio del cosiddetto “corpo nero”: essenzialmente, si tratta di analizzare la radiazione elettromagnetica intrappolata in una cavità e di determinare le proprietà valide in condizioni di equilibrio termodinamico del sistema.
Ora, esiste una vastissima letteratura – a dire il vero di sapore piuttosto apologetico – che considera rivoluzionari i lavori di Planck del 1899-1900 sul problema del corpo nero, essenzialmente perché in essi compaiono quantità discrete di energia4. Si tratta di una considerazione storicamente falsa, perché Boltzmann fin dal 1872 (e poi ancora in un lavoro del 1877) aveva già trattato l’energia come somma di un numero finito di unità multiple di una quantità base ε. Era stato questo per Boltzmann uno strumento di calcolo molto utile, la cui applicabilità era però limitata dalla condizione che fosse possibile mandare ε a zero senza alterare i risultati ottenuti: i risultati, cioè, non dovevano dipendere da quello, che veniva assunto come puro strumento di calcolo. Quest’ultima è appunto la condizione lasciata cadere da Planck.
Se quindi vi è innovazione in Planck – e pensiamo che ciò sia incontestabile – essa non risiede nell’introduzione di un nuovo algoritmo, ma nella concezione del rapporto tra ciò che è la teoria fisica e gli strumenti di calcolo in conseguenza permessi. La “rivoluzione” non risiede nel fatto formale della riduzione dell’energia a quantità discrete, ma nel diverso uso di tale decomposizione. Boltzmann sottolinea infatti che la sua innovazione agisce solo a livello di tecnica matematica, consentendo migliore chiarezza nei calcoli, ma senza porsi come essenziale al risultato. Anzi, egli scrive: “Non ho certo bisogno di sottolineare che per il momento non abbiamo a che fare con un problema fisico reale”5; spiega infatti che sarebbe molto difficile immaginare una situazione tale che le molecole di un gas negli urti potessero scambiarsi solo certe determinate quantità di energia. È chiaro di qui che per Boltzmann il puro carattere strumentale dell’artificio è legato all’impossibilità di darne un’interpretazione fisica in termini meccanico-molecolari.
Ben diversamente, Planck nei suoi lavori del 1899-1900 ignora totalmente il problema dell’interpretazione: ciò che interessa è mettere a punto una formulazione, che risulti particolarmente compatta e semplice. D’altra parte, tanto per sgombrare il campo dagli infiniti equivoci che potrebbero scaturire dai turbamenti filosofici del vecchio Planck, sottolineiamo che potrebbe essere sviante voler misurare la profondità dell’innovazione nell’atteggiamento verso la scienza solo in termini di consapevolezza soggettiva dello scienziato. Ci riferiamo per esempio alla posizione espressa da Planck in occasione della proposta d’ammissione di Einstein alla Preussischen Akademie der Wissenschaften. Qui Planck mostra l’incapacità di risolvere positivamente il. suo intimo contrasto tra istanze ideologiche e concezione (implicitamente ammessa) della natura del progresso della scienza. Tutto ciò risulta molto chiaramente dall’unico dubbio, che egli espresse nei confronti di quella ammissione e che consisteva nel fatto
che le sue [di Einstein] speculazioni l’avevano spinto troppo in là talvolta a esempio per quanto riguarda la sua ipotesi dei fotoni [che Planck ancora negava]; tuttavia non si doveva dare troppa importanza a questo fatto. Infatti, le scienze esatte progredirebbero ben poco, se nessuno osasse correre rischi.6
Ma torniamo al nostro problema e cerchiamo di vedere la questione più in dettaglio.
È noto che Boltzmann conosceva il problema del corpo nero e vi aveva anzi addirittura lavorato, tant’è vero che si deve a lui la dimostrazione che la densità totale di energia della radiazione è proporzionale a T4 (T, temperatura assoluta). Abbiamo appena visto, d’altra parte, che la tecnica che avrebbe consentito di risolvere il problema di determinare la distribuzione spettrale dell’energia del corpo nero era stata appunto introdotta da Boltzmann quando aveva “quantizzato” l’energia per facilitare la soluzione di un gruppo di problemi di meccanica statistica; in particolare, tale tecnica gli era stata necessaria per misurare la probabilità di uno stato. Ma allora – sorge spontanea la domanda – perché Boltzmann non ha affrontato in quei termini se non risolto il problema del corpo nero, anzi, almeno a quanto ci consta, se ne è addirittura disinteressato? Tanto più, si badi, che Boltzmann aveva una grande fiducia nei metodi statistici, mentre Planck, come egli stesso testimonia e come si può ricostruire dai suoi lavori, aveva una spiccata preferenza per una “termodinamica assoluta” piuttosto che statistica e solo dopo alcuni anni di lavoro comprese l’importanza dell’ipotesi statistica.7
4.
Il problema è abbastanza meno ovvio di quanto possa sembrare e diremmo che si può ragionevolmente supporre che vi sia al fondo qualcosa di più che un puro e semplice scontro di opportunità.
Se si considera lo stato della fisica teorica di fine Ottocento e si decide di porre come prioritario il problema del corpo nero – decisione evidentemente tutt’alltro che necessaria – è del tutto verosimile che non si possa trovare una soluzione diversa da quella di Planck, con la conseguente proposta di abbandonare la fisica classica e di costruire una teoria dei quanti. Ma nulla vieta di aggirare l’ostacolo dando una diversa priorità ai problemi da risolvere. Si potrebbe allora decidere, per esempio, di sviluppare e raffinare il formalismo della meccanica statistica classica rendendolo cosi strumento di interpretazione più duttile di fronte alle varie situazioni fisiche. Né sarebbe giusto ritenere questa seconda via, se non impossibile, almeno troppo complicata e cervellotica. Per convincersene, basta pensare allo sviluppo che stanno conoscendo oggi gli studi sulla cosiddetta “teoria ergodica” in meccanica classica e ai molti risultati inattesi, che si sono venuti cosi determinando, tanto – appunto – da giungere a formulare l’idea (per ora non ancora completamente fondata) che l’ipotesi quantistica non sia indipendente, ma possa nascere – in particolari condizioni – dal formalismo statistico classico.
Anche quest’operazione di recupero rende significativa per il presente la discussione sullo stato del problema all’inizio del secolo. Perché, infatti, tutto un filone di studiosi – mossi molto spesso dall’insoddisfazione per il carattere non deterministico o non causale della meccanica quantistica – cercano di sostituire a essa non già una teoria con contenuti predittivi diversi, ma con una diversa sotto struttura di modelli fisici? Rispetto a questa situazione che prova in concreto come la meccanica classica possa essere utilizzata per spiegare certi “fatti”, ritenuti in genere indizio inconfutabile dell’indispensabilità dell’ipotesi quantistica, diventa ancora piu labile ogni interpretazione di sviluppo progressivo e necessario del mutamento delle concezioni scientifiche. A maggior ragione, occorre allora capire che certe potenzialità esplicative di cui pure sono maturi gli strumenti, non sono praticate proprio in quanto muta il criterio di ciò che è significativo o rilevante per la scienza.
Da questo punto di vista, infatti, diventa possibile e semplice rispondere alla domanda sul perché Boltzmann non ha affrontato in tutta la sua estensione il problema del corpo nero: Boltzmann sceglieva evidentemente la seconda delle due vie dette sopra, mentre Planck adottava la prima. Così naturalmente il problema non è stato risolto ma lo si è semplicemente spostato su un altro terreno, quello delle decisioni, e ci si deve chiedere allora per quali ragioni storiche Boltzmann. e Planck abbiano deciso di dare priorità a problemi di ricerca tanto diversi, quale sia il significato dello scontro e, infine, perché abbia perso Boltzmann.
Appare chiaro, dalle considerazioni fatte sopra, che una risposta a queste questioni non si può trovare rimanendo all’interno della problematica scientifica (che, anzi ci offre tutto un ventaglio di potenzialità aperte), ma che occorre confrontare tra loro le diverse finalità sociali, cui i diversi programmi scientifici sono in grado di rispondere.
Per far ciò sarà opportuno riferirsi all’ambiente scientifico tedesco in cui operavano Boltzmann e Planck, e alle tendenze fondamentali ivi presenti.
5.
In Germania, alla fine dell’Ottocento, si contendevano la supremazia tre posizioni principali.
La prima è la meccanica statistica di Maxwell e Boltzmann, la seconda è la cosiddetta scuola energetica, che tenta dI fondare tutta la fisica sul principio di conservazione dell’energia eliminando il fondamento intuitivo della meccanica (Ostwald, Helm, ecc.), la terza è la nascente fisica teorica, di cui Planck può essere considerato un significativo esponente, almeno se si guarda – sul piano della ricostruzione storica – più alla sua produzione che alle sue convinzioni soggettive.
Innanzi tutto, notiamo che questa partizione è realmente vissuta come una battaglia su diversi fronti nella fisica del periodo; Planck stesso, a esempio, vi fa riferimento nelle introduzioni alla prima e alla seconda edizione della sua Termodinamica.8
Il terreno principale dello scontro tra il meccanicismo (con tutte le sue diversificazioni interne) e l’energetica non era una contrapposizione di teorie diverse, ma di modi diversi di intendere la funzione e i compiti della scienza. Citiamo un brano che ci pare molto significativo proprio di uno dei campioni dell’energetica, Helm; riferendosi a un momento particolarmente aspro del dibattito, egli scriveva:
Nella polemica che si accese a Lubecca, nel 1895 non si tratta in realtà di atomismo o di spazio occupato da materia continua, non si tratta del segno di disuguaglianza nella termodinamica o dei fondamenti energetici della meccanica: queste son tutte minuzie; si tratta, in realtà, dei principi della nostra conoscenza della natura. […] Se si concepisce l’energetica con questa ampiezza (con la quale soltanto essa può venire a capo dei compiti che le sono assegnati) allora la decisione è assai semplice: la scolastica o l’energetica: non c’e altra scelta.9
Infatti, lo sforzo dell’energetica, che si salda con tutto un filone. positivista, risponde a un progetto filosofico complessivo, perseguendo il tentativo di ridurre il compito della teoria scientifica alla classificazione dei fenomeni (o, con termine ancora più mistificante, dei “dati dell’esperienza”), per sistemarli secondo le relazioni che li collegano.
Perciò la scuola energetica impone alla scienza unità di principi, in quanto lo spirito è unitario e l’abolizione di ogni struttura esplicativa a fondamento materialista (di qui la polemica con l’atomismo). Perciò per essa è più importante il lato mistico-estetico nella costruzione delle teorie, che non l’efficienza esplicativa10 (anche se il principio di conservazione dell’energia non sembra sufficiente da solo a spiegare i processi irreversibili, non c’è nessuna fretta a complicare la teoria ipotizzando un secondo principio termodinamico indipendente dal primo – di qui la polemica con Planck). Si tratta come si vede di una tendenza conseguentemente conservatrice che, pur di salvare un’idea vecchia della scienza, è disposta a portare quest’ultima alla sclerosi, lasciando senza spiegazione l’enorme messe di fenomeni e di problemi individuati in quegli anni dalla ricerca sperimentale e dalla tecnologia in via di intenso sviluppo.
Molto diverso si presenta invece l’atteggiamento di Boltzmann. La meccanica statistica è un tentativo assai ambizioso di salvare la spiegazione meccanica allargandone il dominio di applicazione mediante l’introduzione di enunciati statistici. Si ottiene così una teoria di riferimento più ricca, che considera dotate di significato fisico anche le spiegazioni ottenute mediante la descrizione del comportamento statistico dei sistemi meccanici.
Più precisamente, un lavoro di ricostruzione storica ci permette di descrivere questo progetto nei termini seguenti: Boltzmann è convinto che i problemi vanno affrontati e risolti, ma è convinto anche che questo risultato vada ottenuto senza compiere rotture radicali con la tradizione. Egli pensa che nuovi strumenti vadano inventati e introdotti in fisica, ma che essi debbano essere tali da non rompere l’unità del quadro concettuale della fisica, cioè che essi debbano essere unitariamente e universalmente dominabili da un’élite, la ristretta comunità scientifica di cui egli stesso è membro. Così la scelta di Boltzmann, che si potrebbe definire un rappresentante dell’ala riformatrice dei conservatori, è di ampio respiro: salvare la spiegazione meccanica e con essa la fondamentale unità nella spiegazione in fisica, ma insieme adeguare la teoria alla necessità crescente di spiegare una miriade di fenomeni ed effetti particolari.
Ben altra ancora la posizione di Planck, quale risulta soprattutto dal suo concreto lavoro scientifico, più che dalla sua consapevole riflessione su di esso. Se riprendiamo le introduzioni alla Termodinamica citate sopra, vediamo emergere con molta chiarezza il suo collocarsi su un fronte contrapposto a entrambi gli altri due atteggiamenti, giacché egli mostra esplicita la sua insofferenza sia per i metodi cinetico-statistici, che per i tentativi di fondare la termodinamica solo sul primo principio.
Planck enuncia anzi in modo assai limpido la sua concezione “possibilista” del lavoro scientifico:
Una terza impostazione della termodinamica si è dimostrata fin qui la più adeguata. Questo metodo […] non si fonda sulla teoria meccanica del calore, ma, evitando ipotesi definite per quanto riguarda la sua natura, parte direttamente da pochi fatti empirici molto generali. […] Quest’ultima impostazione, più induttiva […], corrisponde meglio allo stato presente della scienza. Essa non può essere considerata come definitiva, comunque, ma può dover finire su una teoria meccanica o forse elettromagnetica.
E, va rilevato, questa incompiutezza del punto di vista adottato non impedisce certo a Planck di farne un uso sistematico, anzi. Tanto che egli non avrà alcuno scrupolo a utilizzare, quando gli tornerà utile, il metodo statistico di Boltzmann.
Proprio all’interno di questo “possibilismo” troviamo il nocciolo della portata innovatrice dell’atteggiamento di Planck. Infatti, sia che egli tenti di chiarire ed esplicitare la seconda legge della termodinamica, e in particolare il concetto di irreversibilità, sulla base di una presupposta validità assoluta delle leggi della termodinamica contro l’impostazione degli energetisti, sia che egli si riferisca all’interpretazione statistica di Boltzmann nell’affrontare il problema del corpo nero, andando oltre il limite di applicabilità richiesto da Boltzmann, il suo programma è semplice. Il proposito è quello di aumentare al massimo l’efficienza esplicativa della teoria, a costo di spezzare questa in una miriade di costrutti o teorie parziali tra loro indipendenti o addirittura contraddittorie. Ogni modello matematico, ogni riformulazione linguistica di un problema capace di interpretare teoricamente un gruppo inesplicato di risultati empirici merita considerazione e va assunto come teoria, o almeno un suo abbozzo. Né ciò è contraddetto dalla vasta produzione filosofico-critica sui fondamenti della fisica e dalla convinzione – operante solo sul piano della soddisfazione soggettiva – che l’attività scientifica abbia come scopo la ricerca dell’assoluto. In effetti, questa è per Planck un’istanza estranea alla ricerca attiva, i cui standard egli non mette mai in discussione.
Per chiarire meglio la distinzione qui proposta, confrontiamo le posizioni di Boltzmann e Planck sul problema della semplicità, come criterio metodologico della fisica. Infatti, mentre per Boltzmann la semplicità è un elemento costitutivo della teoria fisica e opera come criterio selettivo delle scelte tra teorie contrapposte, per Planck la semplicità formale fornisce un importante argomento nella scelta tra differenti formule introdotte per spiegare dati sperimentali11.
Non è difficile ora individuare il motivo conduttore delle scelte scientifiche di Planck. Egli proviene da una situazione molto mutata. La scuola in cui ha studiato si sta trasformando in senso favorevole all’allargamento del reclutamento e alla penetrazione dell’istruzione tecnica; la nuova cultura nasce sotto la pressione a lasciar cadere le contrapposizioni teoriche generali (quale a esempio quella tra Boltzmann e gli energetisti) e ad affrontare prioritariamente tutte le questioni. poste dallo sviluppo tecnico e scientifico e non ancora risolte. Ciò anche se si tratta di questioni, dal punto di vista della teoria, molto particolari.
Il contesto storico, che dà senso a questo scontro di ideologie e di concezioni scientifiche, è dato infatti dalla Germania tra Ottocento e Novecento, con il suo potente processo di industrializzazione, in cui svolge un grosso ruolo proprio la diffusione di una formazione culturale sufficientemente duttile da garantire un buon livello di integrazione tra scienza e tecnologia. È significativo che negli ultimi decenni dell’Ottocento l’Inghilterra abbia affrontato anche in questa luce il problema del declino del proprio predominio industriale. Infatti, se la Germania andava superando i livelli inglesi nella produzione dell’acciaio, nell’industria chimica, o nella diffusione. dell’elettrificazione, ciò era largamente legato all’organizzazione del suo sistema di istruzione, gestita dallo stato e a forte componente tecnico-professionale. Così in Inghilterra si esprimeva nel 1884 una commissione reale per l’istruzione tecnica:
Molti chimici tedeschi sono stati e vengono tuttora addestrati nelle università tedesche. I vostri commissari credono che il successo che ha arriso, sul continente, alla fondazione di vasti stabilimenti industriali, officine meccaniche e altri impianti, non si sarebbe realizzato in tutta la sua piena estensione nonostante le molte influenze ritardatrici senza il superiore sistema di istruzione tecnica di tali scuole, senza i mezzi destinati alla ricerca scientifica originale, e senza il generale apprezzamento del valore di tale istruzione, e della ricerca originale, che è diffuso in quei paesi.12
Ciò che la società tedesca chiede alla scienza è dunque la capacità di intervenire in un vasto arco di settori: non interessa quindi una “concezione del mondo,” ma la formazione di aree di ricerca abbastanza autonome da poter essere dominate mediante costrutti anche parziali, purché fecondi di sviluppi. Gli ideali più rigorosamente riduzionistici del meccanicismo soccombono cosi di fronte alla maggiore duttilità e ricchezza di una fisica teorica che – una volta spezzata in linguaggi non più necessariamente unitari – riesce a sistemare in una formulazione matematica ben padroneggiabile il più vasto campo di problemi.13
6.
In conclusione, possiamo dire riassumendo che non sono state le difficoltà interne allo sviluppo della meccanica statistica a imporre una rivoluzione di concetti fondamentali della fisica. È stata invece la nascita di un’esigenza socialmente diffusa di semplificazione e frammentazione dell’attività scientifica a favorire questa rivoluzione, che comportava anche un aumento del potere predittivo della teoria. Si trattava perciò, per l’ambiente scientifico, di compiere una scelta – non soggettiva, ma storica – tra due linee. Queste ultime sono perfettamente individuabili mediante l’analisi storica, anche se non erano perseguite consapevolmente dagli scienziati che le hanno scelte, e si possono cosi riassumere: 1) favorire il processo di socializzazione della scienza, con il rischio di dover rinunciare alla possibilità di dominare la costruzione scientifica nel suo complesso (Planck); 2) tentare di ottenere un compromesso soddisfacente tra la richiesta di una maggiore integrazione sociale della ricerca scientifica, con il conseguente maggior ruolo da giocare, e l’esigenza di garantire alla comunità scientifica un controllo unitario sullo sviluppo dell’attività di ricerca, fondando quest’ultima sulla spiegazione meccanica (Boltzmann); 3) rifiutare in blocco il processo storico in atto, a costo di identificare scienza e filosofia (energetisti).
È chiaro ormai che l’ultima alternativa descritta non aveva alcuna possibilità di affermarsi. E cosi infatti avvenne. Ma è anche chiaro che la via scelta da Boltzmann, assai più impegnativa di quella di Planck, era destinata al fallimento, almeno come posizione isolata. Solo in quanto fosse stata organicamente inserita in una programmazione dell’attività scientifica, essa poteva sperare di rispondere all’istanza sociale, che aveva generato la crisi. Sappiamo d’altra parte che questo non fu il caso.14
Tuttavia, vale la pena di sottolineare alcuni spunti interessanti nella posizione di Boltzmann. Prima di tutto, la lucidità con cui ha compreso che, per superare la crisi – crisi dei compiti istituzionali della ricerca scientifica, prima ancora che crisi esplicativa -, occorreva realizzare una mediazione tra vecchio e nuovo, tra una tradizione scientifica ricca e articolata e le nuove esigenze. Va detto, tuttavia, che Boltzmann vede chiaramente solo i termini culturali del problema. In secondo luogo, va sottolineato il suo rifiuto di accettare acriticamente, come Planck fa, uno stato di necessità. Di qui il tentativo consapevole di mettere tutto un retaggio scientifico al servizio della società, tenendo ferma l’esigenza soggettiva di controllo da parte della comunità scientifica di questo processo. Certo, si tratta di una funzionalizzazione ancora generica, che si riferisce alla società come un tutto e non tiene conto delle contraddizioni di classe in essa presenti, che generano contrapposte finalità. Del resto, questi problemi, che più specificamente si riferiscono al presente, non erano certo maturi all’epoca di Boltzmann e su questi il “caso” che qui abbiamo trattato non può dirci nulla, almeno in modo diretto. Anzi, sono le caratteristiche della scienza nella società capitalistica avanzata a darci le giuste chiavi di lettura per intenderne il processo di formazione, cosi come è il confronto con il presente il reale punto di interesse, perché si innesta nelle responsabilità dei progetti politici. Proprio in questo senso l’analisi storica può non essere né un fatto scolastico di esemplificazione di un metodo, né la cristallizzazione dell’oggettività di ciò che è accaduto, come necessario: per muoverci nel presente, ci interessa perciò discutere a fondo quali forze abbiano dominato e quali finalità abbiano informato certe svolte tuttora operanti.
NOTE
NOTE
1 Si vedano M.E. OMELIANOVSKIJ, V.A. FOCK, L’interpretazione materialistica della meccanica quantistica – Fisica e filosofia in URSS, Feltrinelli, Milano 1972; S. TAGLIAGAMBE, L’interpretazione della meccanica quantistica in URSS alla luce del materialismo dialettico, in L. GEYMONAT, Storia del pensiero filosofico e scientifico, vol. VI, Garzanti, Milano 1973.
2 Si pensi alla ricchezza dei dibattiti sulla funzione della scienza rispetto all’organizzazione capitalistica del lavoro, di cui sono direttamente protagoniste le forze operaie; citiamo ad esempio i contributi apparsi su “Sapere” durante il 1974 e, in particolare, Lavoro e nocività: il sapere operaio (discussione tra sette consigli di fabbrica), in “Sapere“, dicembre 1974.
3 Si veda su questo punto G. BATTIMELLI, Etere e relatività, in “Sapere“, novembre 1974.
4 Si confronti al riguardo la copiosa letteratura citata in E. BELLONE, Aspetti dell’approccio statistico alla meccanica: 1849-1905, Barbera, Firenze 1972, p. 3.
5 S L. BOLTZMANN, Further studies on the thermal equilibrium of gas molecules, Vienna 1872 in S. BRUSH, Kinetic theory, Vol. lI, Pergamon Press 1966, p. 119.
6 Cit. in A. EINSTEIN, La teoria dei quanti di luce, introduzione di A. Hermann, Roma 1972, p. 19.
7 Si veda quanto scrive in proposito Planck stesso in M. PLANCK, Scienza, filosofia e religione, Fabbri, Milano 1973, pp. 17-8. Cfr. anche M.I. K1.EIN, Thermodynamics and Quanta in Planck’s work, in “Physics Today,” 19, 23, 1966.
8 M. PLANCK, Treatise on Thermodynamics, Dover 1945, pp. VIII-X.
9 G. HELM, L’energetica secondo il suo sviluppo storico, Leipzig 1898, citato in E. CASSlRER, Storia della filosofia moderna, voI. IV, Einaudi, Torino 1958, p. 157.
10 Si confrontino a questo riguardo le pagine dedicate a Ostwald ed Helm da E. MEYERSON in Identité et réalité, Paris 1951; in particolare, cfr. pp. 397-401. Si veda anche il giudizio di PLANCK in Scienza, filosofia e religione, citato alla nota 7, pp. 158.
11 Boltzmann, nelle sue Lezioni sui metodi della fisica teorica del 1899, dice: “… nostro compito non può essere quello di trovare una teoria assolutamente corretta, ma piuttosto una rappresentazione che sia la più semplice possibile e caratterizzi il fenomeno nel modo migliore possibile” (citato in E. BRODA, Philosophycal biography of L. Boltzmann, Acta Physica Austriaca, Suppl. X, 26, 1973). E Planck, in uno dei suoi famosi articoli del 1900 sul problema del corpo nero, scrive: “… ho già ricordato poi che nella mia opinione l’utilità di questa equazione era non solo basata sull’evidente stretto accordo […] con i dati sperimentali disponibili, ma principalmente sulla struttura semplice della formula e specialmente sul fatto che essa dà una espressione logaritmica molto semplice.” M. PLANCK, On the theory of the energy distribution law of the normal spectrum, 1900, in Planck’s originaI papers in quantum physics, a cura di H. Kangro, London 1972.
12 Cit. in C. SINGER E AL., Storia della tecnologia, vol. 5, Boringhieri, Torino 1968, p. 799.
13 A conferma ulteriore di quanto qui sostenuto, si può ricordare il processo parallelo di attenzione verso la trasformazione degli atteggiamenti scientifici, che si realizza negli Stati. Uniti, l’altro paese che conosce nel periodo uno sviluppo produttivo impetuoso (citiamo solo il caso di Gibbs e della sua “termodinamica assiomatizzata,” per molti versi vicina alla formalizzazione della fisica teorica che opera in Planck). Rinviamo anche all’articolo di G. BATTlMELLI, citato alla nota 3, per l’esame di come queste stesse caratteristiche del momento storico della Germania si riflettano nella nascita della teoria della relatività.
14 Ci pare significativo, a questo proposito, ricordare che LENIN in Materialismo e empiriocriticismo recupera la positività della teoria di Boltzmann come “in sostanza materialistica.” È anche illuminante la rivalutazione della figura di Boltzmann compiuta dagli scienziati sovietici, che mostra l’interesse, in un regime di pianificazione sociale e scientifica, per questo tentativo di controllo anche soggettivo della scienza. Cfr. anche, a esempio, N.N. BOGOLYUBOV, Y.V. SANOCHKIN, L. Boltzmann, in “Usp. Fiz. Nauk“, 61, 7, 1957.
(11) Riporto di seguito due figure che rappresentano due modelli meccanici realizzati da Boltzmann per spiegare alcuni fenomeni fisici.
Modello meccanico di Boltzmann per illustrare la seconda legge della termodinamica (1884). Questo modello era un’illustrazione di un argomento sviluppato da Helmholtz nel 1884 per dimostrare la limitata convertibilità del calore in lavoro implicata dalla seconda legge della termodinamica (che affermava che in un processo ciclico in cui il calore di un corpo era convertito in lavoro, il calore passava dal corpo caldo a quèllo più freddo). Helmholtz suppose che i moti molecolari di un gas fossero analoghi alle rotazioni di una ruota intorno a un asse fisso, e che l’energia della ruota dipendesse soltanto dalla sua velocità angolare. Se dei dispositivi meccanici fossero stati solidali con la ruota, l’energia del sistema sarebbe stata funzione anche di altre variabili, che potevano essere variate molto poco in confronto alla velocità di rotazione. Helmholtz stabili che l’energia fornita al sistema come calore, rappresentata da un mutamento dell’ energia cinetica della ruota (corrispondente ai moti molecolari di un gas) non poteva essere completamente convertita in lavoro, rappresentato da un lento mutamento negli altri parametri del sistema meccanico (corrispondenti al volume del gas). Benché rinnegasse di aver fornito una qualunque interpretazione meccanica della seconda legge della termodinamica, Helmholtz asserì di aver costruito un’analogia meccanica per la termodinamica basata sulle equazioni di un sistema meccanico.
Nell’illustrare l’argomentazione di Helmholtz attraverso un modello meccanico, Boltzmann studiò le implicazioni dell’analogo meccanico di Helmholtz per la termodinamica. Verso il 1877 Boltzmann aveva formulato un’interpretazione completamente statistica della seconda legge della termodinamica, e nell’elaborare l’interpretazione meccanica della termodinamica di Helmholtz, non rinunciò a considerare questa legge irriducibilmente statistica. Egli volle cercare un analogo meccanico come un mezzo per analizzare gli aspetti problematici dei sistemi termodinamici, quali la distinzione tra calore e lavoro a livello molecolare, e sottolineò la distinzione di Helmholtz tra le coordinate molecolari del sistema (corrispondenti al calore) e i parametri lentamente variabili (corrispondenti al lavoro). (Ludwig Boltzmann, Wissenschaftliche Abhandlungen, Leipzig, 1909, vol. III, p. 143). Tratto da Harman.
Modello meccanico per l’induzione tra circuiti elettrici tratto dalle conferenze di Boltzmann sulla teoria di Maxwell (1891). Boltzmann inventò questo modello meccanico, che fu costruito su sue precise indicazioni, per rappresentare i circuiti accoppiati induttivamente. Il flusso della correnti elettriche e le interazioni tra i circuiti elettrici erano rappresentati dalla rotazione dei dischi dell’ingranaggio, e l’energia della corrente elettrica era considerata dipendente dalla corrispondente velocità di rotazione del disco. Boltzmann stabilì l’identità delle equazioni del suo sistema meccanico e quelle per l’induzione tra circuiti. Egli non era soddisfatto della rappresentazione analitica della teoria di Maxwell formulata attraverso le equazioni della dinamica di Lagrange né di un modello schematico come quello postulato da Maxwell nel 1861 nel suo saggio Physical lines of force. Boltzmann cercò di descrivere un modello meccanico funzionante, spiegandone dettagliatamente la struttura e il moto. Egli sostenne che le analogie meccaniche possedevano un alto valore euristico nel chiarire il significato della teoria dell’ elettricità di Maxwell. Maxwell stesso aveva progettato un modello meccanico per illustrare l’induzione delle correnti tra due circuiti elettrici; il suo modello, descritto nella biografia di Campbell e Garnett, fu costruito al Cavendish Laboratory di Cambridge durante la sua permanenza come professore di fisica negli anni Settanta. (Ludwig Boltzmann, Vorlesungen über Maxwells Theorie der Elektricität und des Lichtes, 2 voll., Leipzig, 1891-1893, vol. I, tav. II, fig. 15). Tratto da Harman.
(12) In questo duro scontro tra posizioni radicalmente diverse, si inserisce la posizione epistemologica di Poincaré, che ridiscusse i fondamenti di tutti i capitoli più rilevanti della fisica, a partire naturalmente dalla meccanica. Ne La scienza e l’ipotesi Poincaré iniziava con l’osservazione che occorre ben distinguere, nella meccanica, ciò che è esperienza e ciò che è ragionamento matematico, ciò che è convenzione e ciò che è ipotesi. Quindi, dopo aver sottolineato che:
non vi è spazio assoluto e noi concepiamo solo moti relativi … ; non vi è tempo assoluto … [e due durate sono uguali solo] per convenzione; … non abbiamo [l’intuizione diretta] della simultaneità di due avvenimenti producentisi in due teatri diversi; … la nostra geometria euclidea non è che una specie di convenzione di linguaggio [e quindi] possiamo enunciare i fatti meccanici, riferendoli ad uno spazio non euclideo,
con la conseguenza che i concetti suddetti non sono condizioni che s’impongono alla meccanica, Poincaré passava a discutere i principi della meccanica.
Riguardo al primo principio, quello d’inerzia, esso non s’impone a noi a priori inoltre è impossibile verificarlo sperimentalmente poiché è impossibile, in tutto l’Universo, disporre di corpi sottratti all’azione di ogni forza. Poincaré proponeva quindi di sostituire il principio d’inerzia con una legge d’inerzia generalizzata avente il seguente enunciato:
l’accelerazione di un corpo dipende dalla posizione del corpo stesso, dai corpi vicini e dalla loro velocità.
Questa nuova legge è certamente quella con cui si è avuto a che fare in tutti i casi in cui si è dovuto fare una misura e quindi essa è stata verificata sperimentalmente in alcuni casi particolari. Inoltre essa
può essere estesa senza timore ai casi più generali, poiché sappiamo che in tali casi generali l’esperienza non può più né confermarla, né contraddirla.
Riguardo poi al secondo principio, Poincaré diceva che così come esso è definito, basato cioè sul concetto di forza come causa di accelerazioni di date masse, è privo di significato perché non sappiamo né cos’è la massa né cos’è la forza. Quindi, quando si dice che la forza è la causa di un movimento si fa della metafisica. Perché la definizione di forza abbia senso occorre potere e sapere misurare quest’ultima, e per far ciò non c’è altro modo che passare al confronto diretto di due forze che ci permetta, ad esempio, di stabilire quando esse sono uguali. Per realizzare questo proposito, secondo Poincaré, disponiamo di tre regole: l’uguaglianza di due forze che si fanno equilibrio; l’uguaglianza dell’azione e della reazione (terzo principio); l’ammissione che certe forze, come il peso, sono costanti nella grandezza e nella direzione. Il fatto poi che il principio di azione e reazione debba intervenire nella definizione dell’uguaglianza di due forze fa si che
tale principio non deve essere più considerato come una legge sperimentale ma come una definizione.
Poste così le cose, si poteva affermare, con Kirchhoff, che la forza è uguale alla massa per l’accelerazione ma, la legge di Newton cessa a sua volta di essere considerata una legge sperimentale; è una semplice definizione.
Ed anche come definizione è ancora insufficiente perché non sappiamo cos’è la massa. Per completarla occorre di nuovo far ricorso alla definizione di azione e reazione:
Due corpi A e B agiscono l’uno sull’altro; l’accelerazione di A moltiplicata per la massa di A è uguale all’azione di B su A; nello stesso modo, il prodotto dell’accelerazione di B per la sua massa è uguale alla reazione di A su B. Poiché, per definizione, l’azione è uguale alla reazione, le masse di A e di B sono in ragione inversa delle accelerazioni di questi due corpi. Ecco definito il rapporto delle due masse: spetta all’esperienza verificare che esso è costante.
Ma anche qui si tratta solo di un’approssimazione, poiché bisognerebbe tener conto delle attrazioni che tutti i corpi dell’universo esercitano su A e su B. E l’approssimazione è lecita solo se noi ammettiamo l’ipotesi delle forze centrali.
Ma abbiamo il diritto di ammettere l’ipotesi di forze centrali ?
Se dovessimo abbandonare questa ipotesi ci troveremmo di fronte al crollo dell’intera meccanica; non sapremmo più come misurare le masse ed il principio di azione e reazione dovrebbe essere enunciato così:
Il movimento del centro di gravità di un sistema sottratto ad ogni azione esteriore sarà rettilineo ed uniforme …Ma [poiché] non esiste sistema che sia sottratto ad ogni azione esteriore, la legge del movimento del centro di gravità non è rigorosamente vera, se non applicandola all’universo tutto intero.
Ma in che modo potremmo noi misurare le masse seguendo i movimenti del centro di gravità dell’universo ? La cosa è manifestamente assurda ed allora siamo costretti a riconoscere la nostra impotenza ricorrendo alla seguente definizione:
le masse sono dei coefficienti che è comodo introdurre nei calcoli.
Insomma, l’esperienza è certamente potuta servire di base ai principi della meccanica ma, poiché questi principi non sono altro che approssimazioni (e già lo sappiamo), esperienze più precise non potranno aggiungere mai niente a quanto sappiamo e quindi l’esperienza non potrà mai contraddire questi principi.
Più oltre Poincaré definisce quello che da lui è chiamato il principio del movimento relativo:
Il movimento di un sistema qualunque deve ubbidire alle stesse leggi, che si riferiscono a degli assi fissi, o a degli assi mobili trascinati da un movimento rettilineo ed uniforme.
Ed osserva che
Così enunciato il principio del movimento relativo rassomiglia singolarmente a ciò che ho chiamato il principio dell’inerzia generalizzato; ma non è la stessa cosa, poiché, qui si tratta delle differenze di coordinate, e non delle coordinata stesse. Il nuovo principio c’insegna dunque qualcosa di più.
Ma poiché, per questo principio si può fare la stessa discussione fatta per il principio d’inerzia generalizzato, ne consegue che anche esso non può essere né dato a priori, né ricavato come risultato immediato dell’esperienza.
Riguardo poi al principio di minima azione vi è una obiezione ancora più grave. Quando si pensa che, a seguito di questo principio, una molecola per spostarsi da un punto ad un altro seguirà la linea più breve, sembra quasi che questa molecola, come un essere animato e libero, dopo essersi fatta tutti i suoi conti sui possibili cammini, scelga quello più breve. Ciò ripugnava letteralmente Poincaré (quasi che il principio di minima azione fosse dato a priori e non a posteriori!).
In ultima analisi, i principi della meccanica, da una parte sono verità fondate su una esperienza grossolana, dall’altra sono postulati applicabili all’intero universo da considerarsi come veri. Ebbene, se possiamo considerare i principi della meccanica come postulati è per una semplice convenzione, la quale non è arbitraria ma, come alcune esperienze ci hanno mostrato, comoda.
Occorre quindi rifarsi a questi principi generali, che sono cinque o sei, poiché la loro
applicazione … ai differenti fenomeni fisici basta per insegnarci ciò che ragionevolmente possiamo aspettarci di conoscere di una cosa … Questi principi sono il risultato di esperienze sommamente generalizzate, e dalla loro stessa generalità sembrano acquistare un grado elevato di certezza. In effetti, quanto più generali sono, tanto più frequentemente si ha l’occasione di metterli alla prova, e moltiplicandosi le verifiche, assumendo le forme più diverse e più insperate, finiscono per non lasciar posto a dubbi.
Vi sono infatti molti principi che hanno più o meno gravi problemi e questi principi, oltre a quelli già dati nel testo e relativi alla termodinamica, erano per Poincaré:
– Principio di relatività
L’esperienza di Michelson-Morley sembra metterlo in discussione. Lorentz è stato costretto ad accumulare ipotesi per cercare di sistemare le cose: tempo locale, contrazione delle lunghezze, …
– Principio di azione e reazione
In difficoltà per quanto già discusso ed in particolare perché, nell’ipotesi di Lorentz, nell’emissione di radiazione da parte di cariche elettriche accelerate esso non sembra rispettato.
– Principio di conservazione della massa
Recenti studi di Abraham, confermati da esperienze di Kaufmann, hanno mostrato la natura puramente elettrodinamica della massa. Ebbene, questa massa deve allora aumentare con la velocità: la massa non si conserverebbe più. Ma anche supponendo una massa meccanica essa, come Lorentz ha mostrato, sarebbe soggetta a contrazioni.
– Principio d’inerzia
Se non ha più validità il principio di conservazione della massa, anche il principio d’inerzia cessa d’essere valido. Infatti, in questo caso, qual è il centro di gravità che continua a muoversi di moto rettilineo uniforme ? A parte si può osservare che nel caso la massa non si conservi, che ne è della legge di gravitazione universale di Newton ?
– Principio di minima azione
E’ l’unico che sembra rimanere intatto (anche se così come è formulato ripugnava Poincaré).
Dopo questa rassegna abbastanza scoraggiante – e dalla quale si può subito capire che Poincaré aveva colto tutti gli elementi alla base dei radicali cambiamenti che presto avrebbero interessato la fisica – egli formulava un accorato appello:
E’ necessario che non si abbandonino i principi prima di aver fatto uno sforzo leale per salvarli.
Ed aggiungeva:
E’ inutile accumulare ipotesi, poiché non si possono soddisfare in una volta. tutti i principi. Pino ad ora non si è riusciti a salvaguardarne alcuni senza sacrificarne degli altri, ma la speranza di ottenere migliori risultati non è del tutto persa.
Com’è possibile far ciò ? La risposta a questa domanda permetteva a Poincaré di scrivere la seguente proposizione di grande interesse:
Forse … dovremmo costruire tutta una nuova meccanica che non facciamo altro che intravedere, nella quale, aumentando l’inerzia con la velocità, la velocità della luce diventerebbe un limite insuperabile. La meccanica ordinaria, più semplice, rimarrebbe come una prima approssimazione, dato che sarebbe vera per velocità non molto grandi, di modo che ancora torneremmo a trovare l’antica dinamica al di sotto della nuova.
BIBLIOGRAFIA
(1) AA. VV. – Scienziati e Tecnologi dalle origini al 1875 – EST Mondadori 1975
(2) Emilio Segrè – Personaggi e scoperte nella fisica classica – EST Mondadori 1983
(3) Ernst Peter Fisher – Aristotele, Einstein e gli altri – Raffaello Cortina 1997
(4) Articoli di Enrico Bellone su: Paolo Rossi (diretta da) – Storia della scienza – UTET 1988
(5) Enrico Bellone – I nomi del tempo – Bollati Boringhieri, 1989
(6) Enrico Bellone – Le leggi della termodinamica da Boyle a Boltzmann – Loescher 1978
(7) A. Baracca, S. Ruffo, A. Russo – Scienza e industria 1848 – 1915 – Laterza 1979
(8) Mario Gliozzi – Storia della fisica – in: N. Abbagnano (diretta da) – Storia delle Scienze, UTET 1965
(9) René Taton (diretta da) – Storia generale delle scienze – Casini 1965
(10) Peter H. Herman – Energia, forza, materia – il Mulino 1984
(11) Ciccotti, Cini, De Maria, Jona-Lasinio – L’ape e l’architetto – Feltrinelli 1976
(12) Ludwig Boltzmann – Modelli matematici, fisica e filosofia – Bollati Boringhieri 1999
(13) Ludwig Boltzmann – Lectures on Gas Theory – Dover 1995
(14) Ludwig Boltzmann – Escritos de mecánica y termodinamica – Alianza Editorial, Madrid 1986
(15) Max Planck – Treatise on Thermodynamics – Dover 1945
(16) Max Planck – The Theory of Heat Radiation – Dover 1991
(17) E.A. Guggenheim – Boltzmann’s Distribution Law – North-Holland Publishing Company, Amsterdam 1955
(18) Max Born – Atomic Physics – Blackie & Son, London 1962
(19) PROBABILITY AND STATISTICS IN BOLTZMANN’S EARLY
PAPERS ON KINETIC THEORY
(20) Thomas S. Kuhn – Black-Body Theory and the Quantum Discontinuity 1894-1912 – Oxford University Press 1978
(21) E. Bellone – Il mondo di carta – EST Mondadori 1976
(22) Piero Caldirola – Lezioni di fisica teorica – Viscontea, Milano, dopo 1950
(23) H. Poincaré – L’espace et le temps – SCIENTIA, Vol.13, 1912.
(24) H. Poincaré – Sur la dynamique de l’electron – RENDICONTI DEL CIRCOLO MATEMATICO DI PALERMO, 21, 1906.
(25) H. Poincaré –La scienza e l’ipotesi – LA NUOVA ITALIA, 1950.
(26) H. Poincaré – Ciencia y metodo – ESPASA CALPE, 1944.
(27) H. Poincaré – El valor de la ciencia – ESPASA CALPE, 1946.
(28) H. Poincaré – Ultimos pensamientos – ESPASA CALPE, 1946.
(29) C. Scribner – H. Poincaré and the Principle of Relativity – AMERICAN JOURNAL OP PHYSICS, 32, pagg.672-678, 1964.
(30) S. Goldberg – H. Poincaré and Einstein’s Theory of Relativity – AMERICAN JOURNAL OP PHYSICS, 35; pagg.934-944; 1967
Categorie:Attualità, Senza categoria
Rispondi