1 – Dipolo elettrico – Momento di dipolo
Cominciamo con il definire una grandezza che ci sarà molto utile per quanto dovremo trattare; il momento di dipolo elettrico.
Per far questo occorre prima definire il dipolo elettrico.
Supponiamo di avere una carica elettrica + q ed una carica – q uguale in valore assoluto ma di segno opposto.
Disponiamo queste cariche ad una distanza fissa d:

Questo oggetto che abbiamo descritto e disegnato è un dipolo elettrico (nel seguito elimineremo l’aggettivo elettrico, in quanto avremo a che fare solo con dipoli elettrici).
La grandezza momento di dipolo (M) è data dal prodotto della carica q (presa in valore assoluto) per la distanza (d) tra le due cariche:
M = q.d
II momento di dipolo M è un vettore (M) che ha la direzione ed il verso che va dalla carica negativa alla carica positiva:

Per indicare simbolicamente un momento di dipolo con il suo verso si usa il simbolo: .

intendendo con esso che la carica negativa è dalla parte della freccia, mentre quella positiva dalla parte opposta.
2 – Dipolo indotto.
Supponiamo di avere un atomo, ad esempio, con un elettrone. Abbiamo quindi un atomo di idrogeno. Noi sappiamo che quest’atomo è neutro, ha, cioè, un numero di cariche positive uguale al numero di cariche negative. Sappiamo poi, da quanto abbiamo studiato precedentemente, che quest’atomo si può rappresentare con un nucleo centrale, positivo, circondato da una nuvola di carica negativa:
Atomo di idrogeno non eccitato
In media, dunque, il centro delle cariche positive e quello delle cariche negative coincide. L’atomo ha allora la carica non distribuita preferentemente da una parte piuttosto che da un’altra.
Ricordiamo ora qualche concetto di elettrostatica.
Supponiamo di avere una piccola sfera conduttrice carica, ad esempio, positivamente (le cose sono identiche se scegliamo la carica negativa), la quale è sospesa su di un sostegno isolante:
Immaginiamo poi di avere un’altra sfera, non carica, e sospesa su di un sostegno isolante:
Questa sfera non carica è in realtà un oggetto in cui cariche positive (nuclei degli atomi che la costituiscono) e cariche negative (elettroni degli atomi che la costituiscono) sono disposti in modo tale da dare come risultato una carica nulla (c’è una neutralizzazione, l’un l’altra, di tutte le cariche):
La sfera precedente con disegnate le cariche (a caso), in modo tale da dare una carica nulla.
Disponiamo i due oggetti ad una certa distanza e cominciamo ad avvicinarli:

Quando le due sfere saranno abbastanza vicine troveremo una situazione del genere:
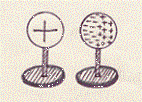
troveremo cioè (fenomeno dell’induzione elettrostatica) che la sfera carica positivamente avrà attratto verso di sé molte cariche negative (elettroni) che si trovano sull’altra sfera generando in questo modo un eccesso di carica negativa da una parte (a sinistra della figura) e, di conseguenza, un eccesso di carica positiva dall’altra parte (a destra della figura) della sfera non carica (in pratica gli atomi che si trovano a sinistra della figura si saranno ionizzati negativamente, avendo acquistato degli elettroni; mentre gli atomi che si trovano dalla parte opposta si saranno ionizzati positivamente, avendo perso elettroni).
Ritorniamo al nostro atomo: abbiamo già detto che, coincidendo il centro delle cariche positive con quello delle cariche negative, l’atomo non ha particolari proprietà:
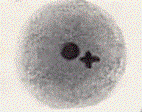
Avviciniamo a quest’atomo una carica, ad esempio, positiva (uno ione positivo). Questa carica da una parte tenderà a respingere l’altra carica positiva (cioè il nucleo) e dall’altra tenderà ad attrarre la carica negativa (cioè la nuvola di

carica che rappresenta l’elettrone). Si avrà in definitiva la situazione seguente: l’atomo sarà discentrato, non avrà più una simmetria di carica (il centro della carica positiva non coincide più con il centro della carica negativa).
Consideriamo questo atomo discentrato. Esso avrà la sua carica positiva situata, preferentemente, dalla parte opposta della sua carica negativa. Questo atomo potrà essere rappresentato come un dipolo
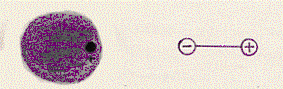
Un dipolo così ottenuto è chiamato dipolo indotto essendo generato dal fenomeno dell’induzione elettrostatica. (Il campo elettrico, che possiamo indicare con E, della carica + che avviciniamo all’atomo neutro, induce su quest’ultimo un determinato dipolo che noi chiamiamo dipolo indotto).
Il discorso che abbiamo fatto, legandolo per semplicità all’atomo di idrogeno, è naturalmente valido per tutti gli atomi. Infatti tutti gli atomi hanno una distribuzione di carica con un centro di simmetria comune e sono quindi sprovvisti di momento di dipolo. E’ possibile comunque, come abbiamo visto per l’idrogeno, indurre su di essi un dipolo: il dipolo indotto.
3 – Polarizzabilità
Secondo quanto abbiamo visto precedentemente a proposito del dipolo indotto, una carica, ad esempio uno ione, positiva avvicinata ad un atomo lo deforma facendolo diventare un dipolo. La deformazione dell’atomo dipende dall’intensità del campo elettrico E della carica (ione) inducente.
Maggiore sarà E, maggiore sarà la deformazione dell’atomo. D’altra parte maggiore deformazione significa che, quando andiamo a rappresentare l’atomo come un dipolo, dovremo considerare una distanza maggiore tra le due cariche:
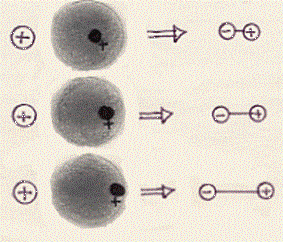
Avvicinando ad un atomo neutro uno ione positivo si origina un dipolo indotto. Maggiore è la deformazione dell’atomo, maggiore sarà la distanza tra le due cariche che rappresentano simbolicamente il dipolo indotto.
Ricordando quanto abbiamo.detto a proposito del momento di dipolo (M = q.d), all’aumentare della distanza tra le due cariche avremo come conseguenza un aumento del momento di dipolo stesso.
In definitiva maggiore è il campo elettrico E, in prossimità di un atomo, maggiore è il momento di dipolo indotto M. Si avrà quindi una proporzionalità diretta tra campo elettrico E e momento di dipolo M:
M = a E
dove a è un coefficiente di proporzionalità che ha le dimensioni di un volume. Alla costante a:
a = M/E
si dà il nome di polarizzabilità elettrica o elettronica (nel caso di un atomo si parla di polarizzabilità elettronica, mentre nel caso di una molecola si parla di polarizzabilità atomica).
In pratica a è un fattore che rende conto di come un determinato atomo (o molecola) si lascia deformare da un campo elettrico esterno (definizione chiara ma non rigorosamente esatta). Un atomo che si lascia deformare di più (che ha di conseguenza un momento di dipolo più grande, a parità di campo elettrico) ha una polarizzabilità più grande.
Si osservi che ogni atomo ed ogni molecola ha una sua determinata polarizzabilità elettronica a. Gli atomi che hanno più elettroni tendono in genere ad avere una polarizzabilità più grande di quella degli atomi con pochi elettroni. Quest’ultimo fatto si spiega ricordando che più gli elettroni si trovano distanti dal nucleo, meno risentono della sua attrazione; è quindi più facile deformare un atomo con molti elettroni, con degli elettroni cioè che si trovano distanti dal nucleo.
4 – Orientamento dei dipoli sotto l’azione di un campo elettrico
Supponiamo di avere dei dipoli elettrici (dipoli, e non dipoli indotti) in assenza di campo elettrico. Questi dipoli saranno orientati a caso:
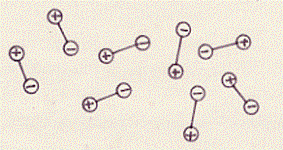
Disponiamo ora questi dipoli all’interno di un campo elettrico costante (E), generato da due piastre conduttrici, affacciate e caricate di segno opposto:
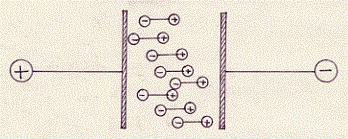
Possiamo vedere dalla figura che i dipoli, sotto l’azione di un campo elettrico, si orientano, in quanto la loro estremità positiva viene attratta dal polo negativo e viceversa.
Vediamo qual è la grandezza che ci dà l’indicazione della tendenza del dipolo elettrico ad orientarsi sotto l’azione del campo elettrico. Consideriamo un solo dipolo. Consideriamolo in tre diversi momenti: 1°) quando il campo elettrico esterno non c’è; 2°) quando il campo elettrico comincia ad agire; 3°) quando il campo elettrico ha già agito.
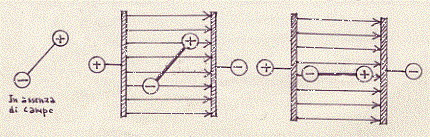
Evidentemente, quando il campo comincia ad agire, la carica elettrica positiva del dipolo sarà attratta dalla piastra negativa che crea il campo e viceversa. In definitiva si avrà una coppia di forze:
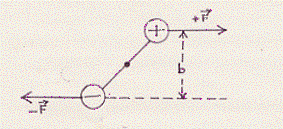
la quale tenderà a far ruotare il dipolo sul suo baricentro (che, se le cariche hanno uguali masse, si troverà al centro del segmento d che separa le due cariche).
Ricordando ora che il momento di una coppia di forze (Mc) è definito come prodotto della forza F (vedi figura precedente) per il braccio b (vedi ancora figura precedente) della forza F:
Mc = b.F
si vede facilmente che: più grande è la distanza d tra le cariche del dipolo, più grande è il braccio b della forza; più grande è la distanza d, più grande è il momento di dipolo M (M = q.d); più grande è il braccio b della forza, più grande è il momento della coppia M (Mc = b.F); ed in definitiva più grande è il momento di dipolo (M), più grande è il momento della coppia (Mc).
Si può allora concludere, come del resto avevamo premesso, che il momento di dipolo dà una indicazione della tendenza di un dipolo ad orientarsi sotto l’azione di un campo elettrico: maggiore è il momento di dipolo, più rapidamente e facilmente un dipolo si orienterà sotto l’azione di un campo elettrico esterno.
5 – Molecole polari (e non polari)
Vi sono delle molecole che, come l’atomo di idrogeno che abbiamo visto prima, hanno la loro carica elettrica disposta simmetricamente; in modo tale, cioè, che il centro di gravità delle cariche positive coincide con il centro di gravità delle cariche negative. Una molecola siffatta è una molecola che non ha polarità distinte, è una molecola non polare.
Caratteristica delle molecole non polari è quindi di non avere, come abbiamo già visto per l’atomo di idrogeno, un momento di dipolo proprio.
Queste molecole comunque, ancora come l’atomo di idrogeno, possono acquistare un momento di dipolo (momento di dipolo indotto) se sono sottoposte all’azione di un campo elettrico esterno (il fenomeno è anche qui quello della polarizzazione: gli elettroni possono essere spostati dalle loro posizioni dal campo esterno; si origina così una deformazione della distribuzione elettronica; questa deformazione fa si che si generi il dipolo indotto).
Oltre a queste molecole, che naturalmente sono non polari, ve ne sono delle altre in cui il centro di gravità delle cariche positive non coincide con quello delle cariche negative. In queste molecole vi sono allora due centri di carica e di conseguenza la distribuzione di carica risulta asimmetrica. La polarità del legame fra due (o più atomi) non dipende dal fatto che un atomo ha più elettroni dell’altro (perché a ciò fa equilibrio la circostanza che a più elettroni corrisponde una maggiore carica positiva nel nucleo) ma dalla posizione di tutti gli elettroni nell’intera molecola, i quali rimangono più a lungo nell’orbita dell’uno piuttosto che dell’altro atomo.
Il fatto che una molecola sia polare significa che essa possiede un momento di dipolo, essendo essa stessa un dipolo permanente (Il primo ad ipotizzare l’esistenza di dipoli associati con le molecole fu P.Debye nel 1912. Anche Reinganum nel 1912 ipotizzò che le molecole neutre trasportano cariche positive e negative). Vediamo qualche esempio dei due tipi di molecole che abbiamo descritto. Se abbiamo delle molecole biatomiche (composte da due atomi) siamo in grado di prevedere la loro polarità andando a considerare gli atomi costituenti. Se infatti i due atomi che costituiscono la molecola sono uguali la molecola deve essere non polare, viceversa se i due atomi che costituiscono la molecola sono diversi la molecola sarà polare.
Esempi di molecole biatomiche non polari, che non hanno cioè mo- mento di dipolo proprio, sono: la molecola di idrogeno (H2 ), la molecola di ossigeno (O2 ) e la molecola di doro (Cl2 ); esempi, invece,di molecole biatomiche polari, che hanno cioè momento di dipolo proprio sono: la molecola di acido fluoridrico (HF), la molecola di acido cloridrico (HCl) e la molecola di cloruro di sodio (NaCl).
Nel caso di molecole poliatomiche (composte da più di due atomi), il criterio per stabilire la polarità è molto più difficile. Infatti, pur essendo polare il legame tra gli atomi a due a due, la molecola in complesso può risultare non polare.
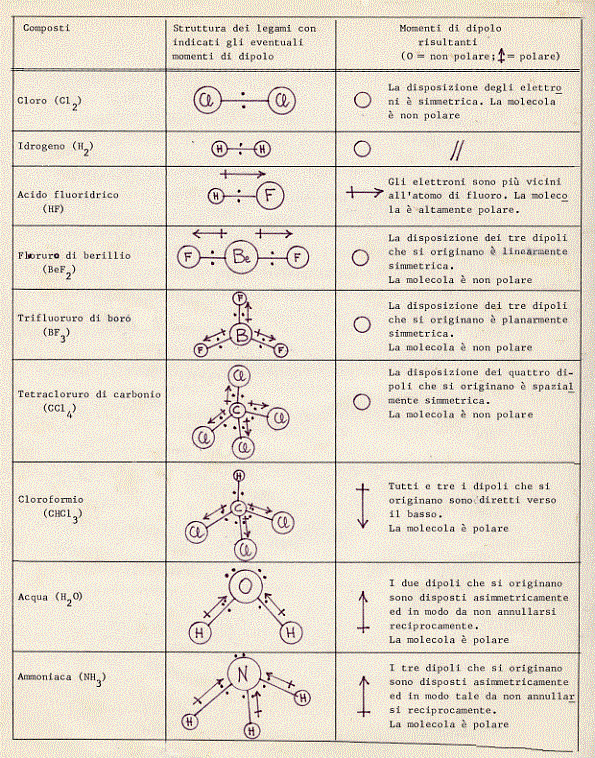
Esempi di molecole poliatomiche non polari sono: la molecola di anidride carbonica (CO2 ), la molecola di tetracloruro di carbonio (CCl4 ) , la molecola di trifluoruro di boro (BF3 ) e la molecola di fluoruro di Berillio (BeF2 ); esempi, invece, di molecole poliatomiche polari sono: la molecola di cloroformio (CHCl3 ) , la molecola di acqua (H2O) e la molecola di ammoniaca (NH3 ).
Nella figura seguente sono riportati i disegni schematici di alcune molecole con i relativi momenti di dipolo:
6 – Dipolo istantaneo
Ritorniamo al nostro atomo di idrogeno e ridisegnamolo secondo il modello atomico di Bohr:
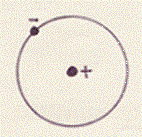
Se bloccassimo la rotazione dell’elettrone ad un certo istante, ci troveremmo con una carica positiva (il nucleo) ad una certa distanza da una carica negativa, l’elettrone.
Ricordando allora la definizione di dipolo, essendovi ad un certo istante una carica positiva ad una certa distanza da una carica negativa, l’atomo di idrogeno, in quell’istante, è un dipolo.
In definitiva nell’atomo di idrogeno, ma anche in tutti gli altri atomi e molecole non polari, vi è istante per istante un dipolo che chiamiamo appunto dipolo istantaneo (il concetto di dipolo istantaneo fu introdotto per la prima volta da London nel 1930, vedi oltre).
Osserviamo però che quanto abbiamo detto non è in contraddizione con la rappresentazione a nuvola di carica. Infatti il valor medio dei momenti di dipolo in tutti gli atomi risulta sempre uguale a zero:
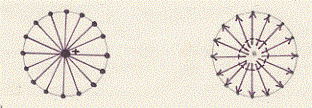
I dipoli istantanei sono simmetricamente sistemati in modo tale da dare in un dato intervallo di tempo risultante nulla.
7 – Quadruplo, ottupolo, etc….
Supponiamo di avere una molecola in cui le cariche elettriche siano distribuite come in figura:
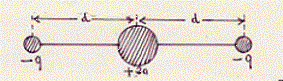
Poiché il centro di gravità delle cariche positive coincide con quello delle cariche negative la molecola non ha momento di dipolo (Md = 0) . Si è però osservato sperimentalmente che, pur essendo Md = 0, il sistema genera un campo elettrico esterno diverso da zero che al crescere della distanza decresce molto più rapidamente di quello di dipolo.
Un sistema con Md = 0 e costituito come sopra prende il nome di quadrupolo ed il momento che si origina prende il nome di momento di quadrupolo (Mq ).
Abbiamo già visto che il momento di dipolo originato da due cariche + q e – q ad una distanza d è dato da Md = q.d. In questo caso Md = 0 mentre Mq ≠ 0. Si può dimostrare che il momento di quadrupolo Mq originato da cariche disposte, per esempio, come in figura è dato da:
Mq = q.d2
Oltre ai dipoli ed ai quadrupoli, qualche volta, occorre considerare gli ottupoli che sono associati a sistemi con Md = 0 e Mq =0. (Sugli ottupoli e sui momenti di ottupolo non diremo altro).
Per spiegare la scelta dei nomi (quadrupolo ed ottupolo) ci serviremo di disegni. Un quadrupolo è un sistema che può essere rappresentato con le cariche disposte ai vertici di un parallelogramma, mentre un ottupolo è un sistema che può essere rappresentato con le cariche ai vertici di un paralilepipedo:
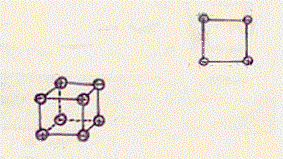
Per ambedue i sistemi si può vedere che il centro delle cariche positive coincide con quello delle cariche negative, da cui Md = 0.
8 – I potenziali di una carica, di un dipolo, di un quadrupolo e di un ottupolo.
Sappiamo già che una carica elettrica q isolata genera nello spazio circostante un campo elettrico. Se in questo campo disponiamo un’altra carica q ad una distanza r dalla prima carica.questa sarà attratta o respinta con una forza data dalla legge di Coulomb. Facciamo una semplice operazione: moltiplichiamo ambo i membri della legge di Coulomb per la distanza r tra le cariche:
F.r = K.(q1q2/r2).r => F.r = K.(q1q2/r)
Ricordando che il prodotto di una forza per una lunghezza origina un lavoro (L = F.s) che ha le dimensioni di una energia, possiamo chiamare, il secondo membro dell’ultima relazione scritta, energia potenziale del sistema formato dalle due cariche q1 e q2 . Abbiamo quindi:
L = K.(q1q2/r)
Dividiamo ora ambo i mèmbri della relazione scritta per q1 :
L /q1 = K (q2/r)
Alla quantità V = L/q1 = K (q1/r) che si ottiene operando in questo modo si dà il nome di potenziale elettrico ed è la grandezza che caratterizza il campo creato da una certa carica q.
Si vede subito allora che il potenziale V = K (q2/r) di una carica q1 è proporzionale ad 1/r.
Allo stesso modo si può dimostrate che: il potenziale (Vd ) originato da un dipolo, ad una distanza r da esso, è proporzionale ad 1/r2; il potenziale (Vq ) originato da un quadrupolo, ad una distanza r da esso, è proporzionale ad 1/r3; il potenziale (Vo ) originato da un ottupolo, ad una distanza r da esso, è proporzionale ad 1/r4.
***
Ricapitoliamo brevemente quanto abbiamo detto.
Tutti gli atomi esistenti in natura non hanno momenti di dipolo permanenti associati, essendovi coincidenza fra il centro delle cariche positive e di quelle negative (vedi “dipolo indotto” in 2).
Tutti gli atomi possono però acquisire un momento di dipolo indotto quando sono sottoposti all’azione di un campo elettrico esterno; infatti, in questo caso, il centro delle cariche positive non coincide più con quel lo delle cariche negative (vedi 2 e “polarizabilità” in 3). Inoltre ad ogni atomo si può associare, istante per istante, un momento di dipolo istantaneo (vedi “dipolo istantaneo”in 6).
Per quanto riguarda le molecole esse si possono distinguere in polari e non polari.
Le molecole polari sono quelle a cui è associato un momento di dipolo permanente, a causa della asimmetrica distribuzione di carica nella molecola (vedi “molecole polari e non” in 5).
Le molecole non polari sono che non hanno un momento di dipolo permanente, poiché il centro delle cariche positive coincide con quello delle cariche negative (vedi vedi “molecole polari e non” in 5).
Queste molecole non polari possono comunque, sotto l’azione di un campo elettrico acquistare un momento di dipolo indotto (vedi 5); ed inoltre sono dotate, istante per istante, di un momento di dipolo istantaneo (vedi vedi “molecole polari e non” in 5).
Pur essendo nulli i momenti di dipolo di alcune molecole, queste possono essere dotate di momenti di quadrupolo o di ottupolo (vedi “quadrupolo, ottupolo, …” in 7).
9 – Le forze di Van der Waals iniziano a trovare una spiegazione. Le prime ipotesi di Keesom (molecole come sistemi elettrici rigidi). Le forze d’orientamento di Keesom.
Abbiamo già detto che nel 1912 prima Debye e poi Reinganum ipotizzarono l’esistenza di cariche elettriche trasportate dalle molecole (ricordiamo che l’anno prima Rutherford aveva proposto il suo modello atomico). Più precisamente Debye (nel febbraio del 1912) ideò una serie di esperienze (sul comportamento delle molecole in processi elettrolitici e sulla loro costante dielettrica e , misura del potere isolante di una sostanza) in cui mostrò che, in determinate condizioni, alcune molecole presentano dei dipoli elettrici associati (si comportano cioè come dipoli); mentre Reinganum (nel giugno del 1912) trattò delle forze che si esercitano tra dipoli servendosi di metodi statistici ed applicò questi risultati agli ioni ed alle molecole, trovando che queste forze, che risultano essere (come vedremo meglio in seguito) attrattive, variano come 1/r7 (se r è la distanza tra gli ioni o le molecole).
In quel periodo si lavorava molto anche a Leida in Olanda. Sotto la guida di Kamerlingh-Onnes, una grossa équipe di scienziati studiava problemi di fisica delle basse temperature(1). L’elio, che aveva resistito per molti anni, proprio a Leida, nel 1908, era stato liquefatto. Questo era un notevole risultato che portò importantissimi contributi all’interpretazione dell’attrazione molecolare oltre ad aprire un praticamente infinito campo di ricerca.
Tra gli scienziati di Leida lavorava anche W.H.Keesom al quale si deve appunto, tra il settembre ed il novembre 1912, il primo tentativo teorico di spiegazione delle forze molecolari.
Keesom considerò le molecole come sistemi rigidi (sfere rigide) dotati di carica elettrica in modo da costituire dipoli permanenti costanti (in pratica considerò tutte le molecole come polari). Secondo Keesom tutti gli atomi e le molecole sono sistemi elettrici ed allora le forze molecolari devono avere origine elettrica. Se ogni molecola è formata da un insieme di cariche positive e negative, ad essa dovrà essere associato un campo elettrico la cui intensità dipenderà dalla distribuzione delle cariche elettriche nella molecola stessa.
Supponiamo di avere un fissato dipolo e di avvicinare ad esso un altro dipolo. Evidentemente l’energia di interazione (e quindi la forza di attrazione o repulsione) tra i due dipoli dipenderà dal loro reciproco orientamento (oltre ché dai valori dei rispettivi momenti di dipolo e dalla distanza a cui si trovano i dipoli). Costruiamoci allora qualche esempio di orientazione reciproca tra dipoli (supponendoli nello stesso piano) e vediamo qual è l’energia corrispondente di interazione (di attrazione o repulsione).
I due dipoli abbiano momenti di dipolo rispettivamente mA ed mB , sia no qA e qB gli angoli rispettivi che questi dipoli formano con la retta congiungente i due centri dei dipoli stessi che si trovano ad una distanza r:
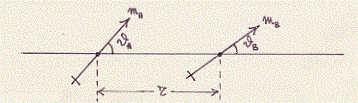
A seconda della rispettiva orientazione dei dipoli, a seconda cioè degli angoli qA e qB avremo situazioni di attrazione o repulsione con diverse energie:
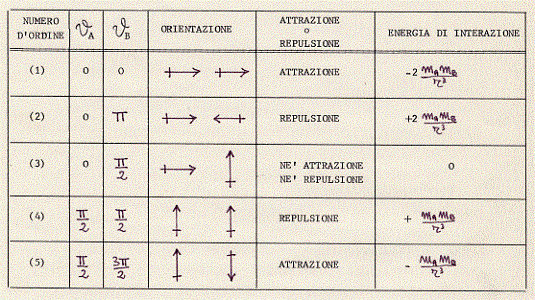
Riferiamoci, ad esempio, al caso (4). I dipoli risultano paralleli con le cariche positive da una parte e quelle negative dall’altra. Le cariche positive si respingono allo stesso modo di quelle negative: il risultato è una energia repulsiva [vedi figura (a) seguente].
Riferiamoci ora al caso (5). I dipoli risultano.paralleli con cariche di segno opposto da una parte e ancora di segno opposto dall’altra. Le cariche di segno opposto si attraggono da una parte e dall’altra: il risultato è una energia attrattiva [vedi figura (b) seguente].
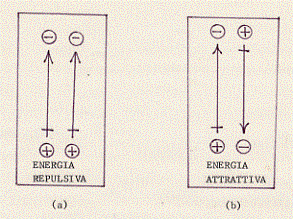
Gli esempi che abbiamo fatto non esauriscono però tutti i casi possibili. In generale il secondo dipolo può assumere tutte le orientazioni rispetto al primo fissato dipolo. E proprio perché tutte le orientazioni sono possibili, in media, l’energia potenziale del secondo dipolo rispetto al primo è nulla. Infatti, tenendo conto di tutte le orientazioni possibili, le cariche nella molecola con il loro movimento creano, in media, una superficie di una sfera con densità di carica costante (allo scopo vedi la figura dei dipoli istantanei che in media creavano una situazione di risultante nulla e riferiscila al caso di dipoli permanenti). Ora, una sfera con densità di carica costante sulla sua superficie si comporta come se tutta la sua carica fosse concentrata nel suo centro. Se tutte le cariche si trovano al centro, le cariche positive neutralizzeranno le negative in modo da originare una molecola che si comporta, appunto in media, come un sistema non carico e quindi non in grado di generare campo elettrico.
In media non vi dovrebbe essere, dunque, attrazione. Comunque non c’è nessuna orientazione privilegiata, e quindi nessuna attrazione, solo quando la temperatura è infinitamente grande. In pratica, cioè a temperature finite ed ordinarie, tra le molecole si avrà una situazione di attrazione, cioè le molecole tenderanno ad orientarsi in modo tale che l’interazione tra i dipoli origini una attrazione. Avremo così attrazione tra le molecole, ma questa attrazione diminuirà con l’aumentare della temperatura fino a che, a temperatura infinitamente grande, non esisterà più.
Questo modello, introdotto da Keesom, per spiegare le forze di attrazione molecolare implica che se non ci sono orientazioni privilegiate dei dipoli tra le molecole, non vi può essere nessuna forza di attrazione tra le molecole stesse.
E questa conclusione ricavata da Keesom era in contrasto con molti fatti sperimentali i quali dimostravano: 1) che esistono forze di attrazione molecolare anche in assenza di dipoli permanenti (anche, cioè, quando le molecole sono non polari c’è attrazione tra di esse) e 2) che le forze di Van der Waals persistono anche ad alte temperature. Intanto nel 1913 ancora Debye faceva esperienze sulle molecole (esperienze riprese nel 1914 da J. Timmers e nel 1919 da M. Iona) ed in particolare studiava gli indici di rifrazione di diversi gas.
Nel 1916, sulla base dei risultati acquisiti in quegli anni, Keesom ampliò e perfezionò la sua precedente teoria riuscendo, almeno in parte, a rimuovere la prima obiezione che abbiamo sollevato poco fa.
Facendo esplicito riferimento ai lavori di Debye sulle molecole (relativi all’indice di rifrazione ed alla costante dielettrica di alcuni gas) i quali facevano rilevare il fatto che le molecole biatomiche dei gas elementari (N2, O2, H2, etc…) non possedevano momento di dipolo, Keesom avanzò l’ipotesi che alcune molecole, pur non essendo dotate di momento di dipolo, debbono essere dotate di momento di quadrupolo.(2)
Queste molecole erano dunque considerate da Keesom come rigide sfere con momenti di quadrupolo associati. Secondo lo scienziato olandese:
a) le molecole, quando collidono, si comportano come sfere rigide;
b) le forze attrattive o repulsive (escluse quelle di collisione) che le molecole esercitano l’un l’altra possono essere derivate dalla legge di Coulomb;
c) la molecola nel complesso risulta neutra;
d) alcune molecole hanno un momento di dipolo associato, altre un momento di quadrupolo;
e) le attrazioni tra le molecole possono essere originate: 1) da interazioni dipolo-dipolo, 2) da interazioni dipolo-quadrupolo, 3) da interazioni quadrupolo-quadrupolo.
f) L’energia media di interazione tra due dipoli (cioè tra due atomi o due molecole) a distanza r è proporzionale ad 1/r6 e, di conseguenza la forza che si esercita tra questi dipoli è proporzionale ad 1/r7.
La teoria di Keesom dava valori ragionevoli per i momenti di quadrupolo delle molecole e questi valori erano in accordo con quelli standard ricavati all’epoca; la teoria risultava però insufficiente poiché non spiegava l’esistenza di forze di Van der Waals a temperatura per le quali l’effetto di orientamento, alla base delle ipotesi di Keesom, era trascurabile.
Questa difficoltà fu superata, nel 1920, da P.Debye, il quale osservò che in realtà le molecole non sono strutture rigide ma sistemi con una distribuzione di carica deformabile.
Con l’ipotesi di Debye relativa alla deformabilità della struttura di carica delle molecole, si raggiunse una prima soddisfacente e completa interpretazione delle forze di Van der Waals.
10 – Le forze di Van der Waals. Le forze di induzione di Keesom.
Secondo Debye (1920) esistono forze di attrazione fra molecole di ogni tipo e questo fatto è una proprietà generale della materia. Se immaginiamo le molecole essere dei sistemi rigidi dotati di carica elettrica vi sarà sempre una forza che agisce tra due d» questi sistemi (tra due molecole); questa forza sarà più o meno grande, attrattiva o repulsiva, a seconda dell’orientazione reciproca dei sistemi (delle molecole). Poiché in un gas, tutte le orientazioni delle molecole sono possibili, Debye si preoccupò di ricavare la media di queste orientazioni in modo tale da calcolare il termine attrattivo ( a/V2) che compare nell’equazione di stato di Van der Waals. Per calcolare questa media occorre servirsi di concetti statistici ed osservare che le orientazioni dei dipoli dipendono dalla temperatura. Quando queste temperature sono alte, tutte le orientazioni dovrebbero essere possibili e quindi non dovrebbe esservi attrazione tra le molecole. Ma l’ipotesi, relativa alla coesione tra le molecole, fatta da Van der Waals per ricavare la sua equazione rimane anche ad alte temperature; e questa era 1’incongruenza che aveva posto un limite di validità alla teoria di Keesom.
Secondo Debye, però, questo limite cade e tutto cambia in modo radicale se abbandoniamo il modello di sfere rigide per le molecole e lo sostituiamo con un modello di strutture non completamente rigide e quindi deformabili (questo fatto era stato suggerito a Debye dalle esperienze da lui effettuate nel 1913 e relative all’indice di rifrazione di diversi gas).
Supponiamo allora che le molecole siano deformabili: esse saranno allora polarizzabili.
I casi allora sono due: o la molecola è polare ed allora ha il suo dipolo permanente associato (sia se essa è rigida sia se è deforma bile) o la molecola è non polare avendo un quadrupolo associato (se è rigida) e risultando polarizzabile (se è deformabile). Occorre qui notare che il momento di dipolo indotto dovuto alla polarizzabilità può aversi in aggiunta ad un eventuale dipolo o quadrupolo permanente.
Se la molecola è deformabile, posta in un campo elettrico generato da un’altra molecola (ad esempio da una molecola polare a cui è associato un dipolo permanente) si polarizzerà acquistando un momento di dipolo m proporzionale al campo elettrico che lo ha generato: il risultato di ciò è una attrazione tra le due molecole. Ponendo quindi una molecola nel campo elettrico generato da un’altra molecola (ad una distanza r), la prima acquisterà un momento di dipolo indotto mediante il meccanismo della polarizzazione e fra le due molecole si originerà una forza di attrazione (proporzionale ad 1/r7 da cui segue che l’energia U è proporzionale ad 1/r6 ). Questa forza di attrazione non può svanire ad alte temperature infatti non siamo più nel caso di dipoli permanenti associati a molecole, come sfere rigide, in cui, ad alte temperature, tutte le orientazioni erano egualmente probabili.
Ora siamo nel caso in cui, qualunque sia l’orientazione del di- polo che crea il campo, la molecola che si polarizza segue corrispondentemente, con la sua deformazione, il dipolo che crea il campo. Visualizziamo con un esempio quanto abbiamo detto. Fissiamo le idee su una molecola polare (un dipolo) che crea il campo. Se poniamo.nel campo creato da questo dipolo una molecola non polare (nella quale in centro delle cariche positive coincide con quello delle cariche negative e che per semplicità possiamo rappresentare come una struttura sferica, con una nuvola di carica negativa ed il nucleo di carica positivo). Allora,comunque vari l’orientazione del dipolo inducente (a causa per esempio,dell’aumento di temperatura) in tempi successivi, allo stesso modo varierà (sempre in tempi successivi) il dipolo indotto sulla molecola polarizzabile (si dice allora che i due dipoli, quello permanente e quello indotto sono in fase) :
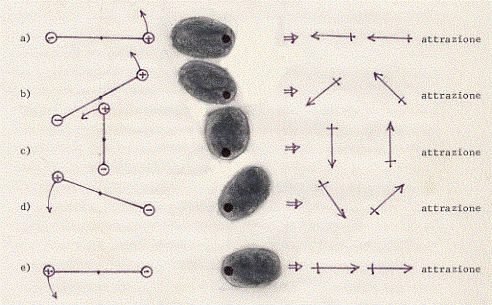
La figura rappresenta una situazione in cui ad un dipolo permanente che crea un campo elettrico viene avvicinata una molecola polarizzabile. La situazione di cui alle lettere a), b), c), d), e) è relativa a tempi successivi in cui il dipolo inducente ruota in verso antiorario. Come si può vedere c’è una rotazione analoga del dipolo indotto in modo tale che tra i due dipoli risulta sempre una attrazione.
Il risultato dell’avvicinamento di un dipolo permanente ad una molecola polarizzabile (dipolo indotto) è quindi sempre una attrazione.
Illustriamo meglio, con un esempio, il perché queste forze risultano attrattive.
Supponiamo di avere due dipoli permanenti, associati a due molecole polarizzabili, disposti come in figura (a) e gli stessi due dipoli disposti in altro modo come in figura (b):
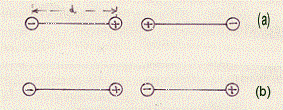
Vediamo il caso di figura (a).
La posizione assunta dai dipoli origina un effetto repulsivo. Il campo elettrico, generato dai dipoli, agisce in modo tale da ridurre la distanza (d) tra la carica positiva e quella negativa in ogni dipolo. Diminuiscono allora i momenti di dipolo dei due dipoli. In definitiva, subito dopo che comincia ad agire la forza repulsiva, diminuisce il valore dei momenti di dipolo dei due dipoli poiché, essendo il momento di dipolo m = q.d, se diminuisce d, a parità di q, il momento m deve diminuire:
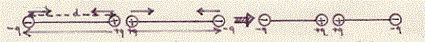
Di conseguenza la forza repulsiva diminuisce e questo fatto si può interpretare nel senso che, come effetto secondario, si origina una forza attrattiva.
Vediamo il caso di figura (b).
La posizione che hanno i dipoli origina un effetto attrattivo. L’insieme dei due dipoli darà luogo ad un campo elettrico, l’intensità del quale deformerà i dipoli stessi (spostando la distribuzione originaria di carica) in modo tale da originare un aumento dell’attrazione tra di essi (facendo aumentare i momenti di dipolo dei due dipoli). Quello che succede è il contrario di ciò che accadeva prima: subito dopo che comincia ad agire la forza attrattiva, il campo elettrico generato dai due dipoli agisce in modo tale da aumentare la distanza (d) tra la carica positiva e negativa in ogni dipolo. Aumentando d devono aumentare i momenti di dipolo m dei due dipoli e di conseguenza all’attrazione originaria se ne aggiunge un’altra.
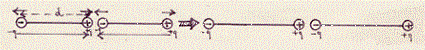
Anche qui si ha allora un effetto secondario che fornisce una forza attrattiva che si va ad aggiungere a quella iniziale.
In ambedue i casi l’effetto primario di attrazione o repulsione si annulla quando si fa la media su tutte le possibili orientazioni dei dipoli; ciò che rimane comunque è l’effetto secondario che origina sempre una forza attrattiva.
A questo punto dobbiamo osservare che l’interpretazione delle forze molecolari basata sulla polarizzabilità delle molecole è ancora insufficiente. La domanda che sorge spontanea è infatti: se abbiamo molecole non polari, che cosa (o chi) origina il campo inducente?
A quell’epoca tutti i gas (monoatomici) rari (come argon, neon ed elio) erano stati liquefatti. Gli atomi che costituiscono questi gas sono tutti a simmetria perfettamente sferica [il centro di gravità delle cariche negative (gli elettroni) coincide con quello delle cariche positive (il nucleo)]. Non c’è nessun dipolo permanente che possa indurre un dipolo sulla polarizzabilità di un atomo ed allora non c’è nessuna forza che può agire tra questi atomi per farli vieppiù aderire fino ad originare un liquido.
Questo fatto metteva in crisi la teoria di Debye.
Si cercò allora di sistemare la teoria (sia da parte di Keesom nel marzo del 1921, sia da parte di Debye nel maggio dello stesso anno) introducendo anche qui i quadrupoli: erano i quadrupoli associati alle molecole non polari ad originare il campo inducente.
Questa spiegazione ebbe scarso successo perché, proprio nel caso dei gas rari, si ha a che fare con atomi e non con molecole; e gli atomi non hanno quadrupoli associati (né tanto meno dipoli).
* * *
A questo punto la situazione può essere così riassunta: l’effetto di orientamento di Keesom è capace di spiegare le forze di Van der Waals considerando associati alle molecole dei gas, considerate come sistemi rigidi, dipoli o quadrupoli. Questa spiegazione è valida solo per basse temperature.
Le forze di induzione di Debye, considerando le molecole polarizzabili, introduce un effetto di attrazione addizionale per i gas in considerazione. Questa attrazione addizionale persiste anche ad alte temperature. Nessuno dei due effetti (quello di orientamento di Keesom e quello di induzione di Debye) è però in grado di spiegare le forze di attrazione tra gli atomi dei gas rari.
Questa difficoltà venne rimossa nel 1930 dal fisico tedesco Fritz London.
NOTE
(1) Si osservi che siamo alla vigilia della Prima Guerra Mondiale e, come si sa, in tempo di guerra la scienza fa dei grossi balzi avanti, perché si cercano, con profusione di denaro, sue applicazioni belliche. Inoltre, all’epoca, era profondamente sentito il problema della conservazione dei cibi da parte delle grosse industrie e dei grandi finanzieri che li importavano dal vasto impero coloniale olandese. E proprio nel senso di queste ultime cose che abbiamo detto, era già nota l’estrema importanza delle basse temperature.
(2) Il quadrupolo è infatti un sistema in cui la distribuzione di carica ha una più grande simmetria di quella del dipolo; questa simmetria non è però sferica, per cui i quadrupoli producono un campo elettrico esterno. I momenti di quadrupolo, al contrario di quelli di dipolo, non possono essere misurati direttamente; è la conoscenza della struttura delle molecole che fa intendere che molte molecole debbano possedere un momento di quadrupolo.
Categorie:Atomi e Molecole
Rispondi