Ciò che si può ricavare da quanto detto è che se si ha un sistema (isolato) in esso avvengono solo quelle trasformazioni che lo portano verso lo stato a cui compete la massima probabilità (stato più stabile del sistema) e ciò è sempre vero ogniqualvolta il numero N dei componenti del sistema è grandissimo e nel nostro caso (molecole di un gas) la cosa è sempre verificata.
Prima di andare avanti, cerchiamo di ricavare dagli esempi fatti qualche informazione relativa al numero delle distribuzioni di un certo numero di oggetti in un certo numero di posti. Dati Z posti ed N oggetti, in quanti modi diversi gli N oggetti si possono distribuire nei Z posti?
Nel primo esempio avevamo a disposizione N = 3 molecole e Z = 2 celle e avevamo trovato che si poteva ottenere un totale di P = 8 distribuzioni.
Nel secondo esempio avevamo a disposizione N = 3 molecole e Z = 3 celle e avevamo trovato che si poteva ottenere un totale di P = 27 distribuzioni.
Nel terzo esempio avevamo a disposizione N = 3 molecole e Z = 4 celle e avevamo trovato che si poteva ottenere un totale di P = 64 distribuzioni.
Cominciamo col dire che il numero di permutazioni di N molecole è N! (un numero seguito da un punto esclamativo che vuol semplicemente dire il prodotto di tutti i numeri interi che precedono quel numero fino al numero stesso).
Vediamo un esempio. Se N = 3 (a, b, c), N! sarà uguale a 6 ed infatti si hanno le seguenti permutazioni:
abc
acb
bac
bca
cab
cba
che sono proprio in numero di 6, cioè 3! = 1 . 2 . 3 = 6.
Così facendo, però, si includono anche i casi in cui vengono permutate le molecole di una stessa celletta; poiché queste permutazioni non rappresentano nuove possibilità di realizzazione della distribuzione considerata si deve dividere N! per il numero n1! di permutazioni nella prima cella, per il numero n2! di permutazioni nella seconda cella, e così via, ottenendo allora per il numero di possibilità di realizzazione di una certa distribuzione (probabilità termodinamica):
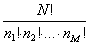
Se si fanno poi variare i numeri n1, n2 , …, nM questa espressione ci dà il numero di possibilità di realizzazione di altre distribuzioni.
Vediamo un esempio di quanto detto.
Rifacendoci all’esempio 2, precedentemente visto, ricordiamo che si avevano N = 3 molecole da distribuire in Z =3 stati possibili.
Abbiamo visto nell’esempio che si avevano varie distribuzioni microscopiche (27) a cui corrispondevano un certo numero di stati macroscopici (10).
Ora abbiamo già visto che 3 molecole si possono permutare in 3! = 6 modi diversi.
Nel caso della distribuzione P1 si ha allora (N = 3 molecole in totale; n1 = 3 molecole in Z1; n2 = 0 molecole in Z2; n3 = 0 molecole in Z3):
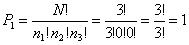
il che corrisponde alla unica possibilità di realizzazione di questo stato microscopico.
Altrettanto si può dire per P2 e P3:
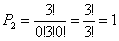
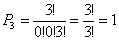
Nel caso della distribuzione P4 si ha allora (N = 3; n1 = 2; n2 = 1; n3 = 0):
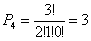
il che corrisponde alle tre possibilità di realizzazione di questo stato microscopico.
Altrettanto si può dire per P5, P6, P7, P8, P9:
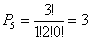
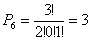
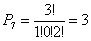
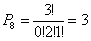
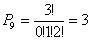
Nel caso della distribuzione P10 si ha (N=3; n1 = 1; n2 = 1; n3 = 1):
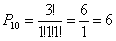
il che corrisponde alle 6 possibilità di realizzazione di questo stato microscopico.
Tenendo ora conto che il volume totale del nostro gas è stato diviso in tre celle (Z1, Z2, Z3) che, implicitamente, abbiamo supposto di ugual volume segue che ogni cella avrà un volume 1/3, cioè: Z1 =1/3, Z2 = 1/3, Z3 =1/3.
Per avere ora la probabilità di una certa distribuzione
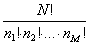
si deve moltiplicare ancora questo numero per la probabilità a priori della distribuzione (quella che nei nostri esempi era data dall’inverso 1/P del nume ro totale P di distribuzioni possibili); questa probabilità a priori è data dal prodotto:
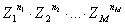
Riferendoci sempre al secondo degli esempi fatti (N =3; Z = 3) si aveva che il numero totale delle distribuzioni era P=27; quindi la probabilità a priori per ciascuna distribuzione doveva essere 1/P = 1/27.
Facendo i conti con qualche possibile distribuzione delle 27 complessive, tenendo conto che Z1 = Z2 = Z3 = 1/3, si trova:
– nel caso in cui n1 = 3, n2 = 0, n3 =0:
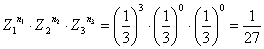
– nel caso in cui n1 = 2, n2 = 1, n3 = 0:
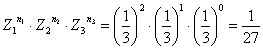
– nel caso in cui n1 = 1, n2 = 1, n3 = 1 :
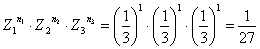
e, continuando così, si trova che ogni possibile distribuzione ha una probabilità a priori uguale proprio a 1/27.
In definitiva la probabilità matematica di una certa distribuzione è data da:
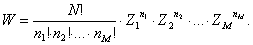
Ancora riferendoci al secondo esempio vediamo qual è la probabilità di avere una molecola per ogni cella. Si ha (N = 3, Z = 3, Zi = 1/3, n1 = n2 = n3 = 1):
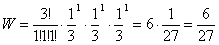
che è proprio il numero P10/P che avevamo trovato.
In definitiva, per legare questo simbolismo a quello usato negli esempi, si ha:
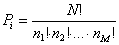
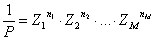
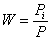
A questo punto è utile introdurre la formula di Stirling che rende più semplici i calcoli da svolgere.
Per a molto grande vale la relazione:
a ! = a a
Per cui la relazione che ci dà W diventa:
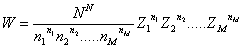
Passando ora ai logaritmi dei due membri si ha:
log W = N log N – n1 log n1 – n2 log n2 – … – nM log nM + n1 log Z1+ n2 log Z2 + . . . + nM log ZM =>
log W = N log N + n1 (log Z1 – log n1) + n2 (log Z2 – log n2 ) + … + nM(log ZM – log nM) =>
log W = N log N +n1 log Z1/n1 +n2 log Z2/n2 + … + nM log ZM/nM .
Poiché sappiamo che lo stato in cui si troverà il gas sarà quello a cui compete la massima probabilità, dobbiamo calcolare il valore massimo di log W.
E’ un problema di massimo assoluto (sotto le condizioni di costanza del numero totale di particelle e dell’energia)
Si ni = N con (N = n1 + n2 + … + nM)
Si ni Ei = E con (E = n1E1+ n2E2 + … + nMEM)
di una funzione a più variabili (ni) che si risolve normalmente con il metodo dei moltiplicatori di Lagrange.
Per il calcolo si tenga conto che n e Z sono grandezze costanti e che, per quanto abbiamo detto prima:
Si dni = 0
Si Ei dni = 0.
Cominciamo con il trasformare l’ultima espressione trovata per log W nel modo seguente:
log W = N log N + p>i ni log Zi/ni.
Tenendo anche conto che
N log N = costante
si può scrivere
log W = costante + Si ni log Zi/ni.
Usando quindi il metodo dei moltiplicatori di Lagrange sotto le condizioni date si ha:
d (log W) = 0
(*) d (log W) – α Si dni – β Si Ei dni = 0
dove i coefficienti – α e – β sono da determinarsi in base alle condizioni di costanza di N ed E.
E differenziando rispetto ad ni l’espressione che ci dà log W troviamo:
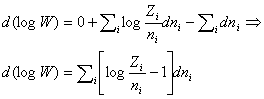
Inserendo quest’ultima espressione nella (*) si ha :
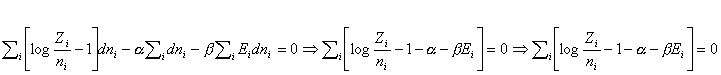
Fino a questo punto era implicito in quanto dicevamo che le operazioni su N, Z ed E erano valide all’interno di ogni intervallo di energia. Ma noi dobbiamo arrivare ad una espressione che abbia valore indipendentemente per ciascuno degli intervalli di energia dati. Ciò vuol dire che nell’espressione che dobbiamo trovare possiamo eliminare la sommatoria e riferirci ad una generica espressione i:
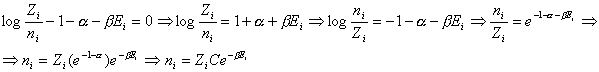
avendo chiamato con C la quantità costante tra parentesi tonda. Con ovvio simbolismo, la precedente espressione si può anche scrivere:
n (Ei) = Z (Ei) . C . e–bEi
dove C e β sono le costanti che si possono determinare con le due condizioni ausiliarie di costanza di N e di E. A questo punto si potrebbe dimostrare che β vale 1/ kT, ma i conti sono complessi e noi ci accontentiamo del risultato. In definitiva, la relazione scritta è l’espressione di Maxwell-Boltzmann, la quale, ricordiamolo, ci fornisce le possibili distribuzioni di una energia (totale) E fra un insieme di N molecole:
(**)
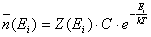
dove: il primo termine sta per il numero di molecole che possiedono energia Ei (la barra sopra ad n sta per “numero medio”); Z (Ei) = numero di stati (cellette) del sistema a cui compete energia Ei , o meglio, densità degli stati per unità di energia e di volume; C = costante che si può determinare imponendo che la somma di tutte le molecole è costante ed uguale ad N; k = costante di Boltzmann = 1,38 . 10-16 erg/grado; T = temperatura assoluta a cui si trova il sistema.
La relazione scritta ci dice che il numero numero medio di molecole che ha energia Ei , dipende dal numero di stati a cui compete energia Ei e decresce esponenzialmente all’aumentare dell’energia Ei; in altre parole: fra celle di uguali dimensioni quelle con energia maggiore sono meno popolate di quelle con energia minore; in altre parole ancora: in un gas ad una data tempera tura T, una data molecola passerà una parte maggiore del suo tempo in stati di energia inferiore che in sta ti di energia superiore.
Per eliminare il parametro C occorrono dei conti che, al nostro livello, non è possibile fare. Imponendo comunque la condizione secondo cui la somma di tutte le molecole è costante ed uguale ad N si trova:
C = e E0/kT
dove E0 è un valore costante per l’energia (energia di riferimento). Per cui la relazione (**) diventa
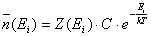
=>
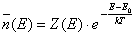
(1)
avendo eliminato, per semplicità, gli indici i.
La (1) sta ad indicare che il numero di molecole che hanno energia E ≠ E0 (energia di riferimento) è proporzionale al numero degli stati Z (E) che abbiamo a disposizione e aventi energia E secondo il fattore e – (E – E0)/kT. La grandezza che ci fornisce il numero medio di molecole, n (E), per semplicità trascritta senza barra sopra, può essere interpretata anche come il numero degli stati, ad energia E, occupati; mentre la grandezza Z (E) può essere interpretata come il numero degli stati che abbiamo a disposizione aventi energia E. Per cui, con quanto abbiamo o ra detto, il nostro problema diventa quello di ricercare tra tutti i possibili stati Z (E) quelli n (E) che sono effettivamente occupati [gli n(E) sono per noi i casi favorevoli mentre le Z (E) sono per noi i casi possibili].
Ricordando che la probabilità matematica è definita come il numero dei casi favorevoli sul numero dei casi possibili, possiamo dire che il rapporto n(E)/z(E) rappresenta la probabilità di avere un numero n(E) di molecole con energia E, di avere, cioè, molecole con energia E diversa da E0 (che era la nostra energia di riferimento). Possiamo indicare questa probabilità con il simbolo fB(E) e chiamarla funzione di distribuzione di Boltzmann:
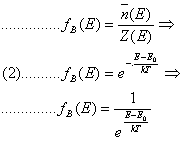
Per il numero medio di molecole a cui compete energia E ≠ E0 [poiché ogni molecola è in realtà u no stato energetico, si potrebbe dire che il numero n(E) medio è il numero degli stati occupati] si ha allora:
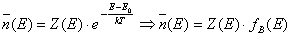
(3)
con: primo membro uguale al numero degli stati occupati; Z (E) = numero di stati a disposizione o, meglio, densità degli stati (per unità di energia e di volume); si può dimostrate che Z (E) = a .E½ , essendo a una costante; fB(E) = probabilità che uno stato sia occupato. La (3) dice che il numero di molecole con energia E ≠ E0 dipende dal numero degli stati che hanno energia E (dalla densità degli stati con energia E) e decresce esponenzialmente all’aumentare dell’energia E; oppure, in altre parole, il numero degli stati occupati è dato dal prodotto della densità degli stati per la probabilità che uno stato sia occupato (ricordo che, classicamente, se E = 0 tutte le molecole sono al livello energetico più basso).
Per comprendere meglio il significato delle relazioni scritte vediamo il grafico (abbastanza qualitativo) della (2):
Tenendo conto che fB (E) è una probabilità matematica essa può assumere 1 come suo massimo valore.
Imponiamo quindi che fB (E) sia uguale ad 1 e cerchiamoci le condizioni per l’energia E. Si ha:
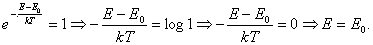
Quindi per E = E0 la fB (E) ha un massimo che vale 1. Si vede poi che per E che diventa molto grande (E -> ∞) segue che fB (E) diventa molto piccola [l’esponenziale della (2) tende a zero].
Il grafico della (2) diventa allora:
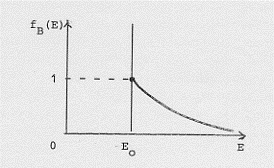
(Si osservi che sotto E0 non si può andare) .
Categorie:Matematica
Rispondi