J.J. THOMSON MISURA LA VELOCITA’ DEI RAGGI CATODICI
Joseph John Thomson nacque nel 1856 vicino Manchester, in Gran Bretagna. Nel 1870 iniziò gli studi di ingegneria all’Owens College (oggi Università di Manchester) per passare nel 1876 al Trinity College di Cambridge dove si laureò (BA) nel 1880 (risultando secondo sia ai Tripos che al Premio Smith) e prese il master (MA) nel 1883. Dal 1884 ebbe la cattedra Cavendish di fisica sperimentale a Cambridge dove successe a Rayleigh e dove restò fino al 1918.
J.J. Thomson
Nel 1884 vinse il premio Adams con Treatise on the Motion of Vortex Rings nel quale si vede con chiarezza che i suoi interessi riguardano la struttura dei costituenti la materia. Altri suoi lavori d’inizio carriera furono Application of Dynamics to Physics and Chemistry del 1886 e Notes on Recent Researches in Electricity and Magnetism del 1892 che riunisce tutti i lavori che seguirono al Trattato di elettricità e magnetismo di Maxwell tanto che ci si riferisce a questo lavoro chiamandolo il Terzo volume del Trattato.
Ma già Thomson era impegnato in ricerche sui raggi catodici e nel 1894 scrisse una memoria in cui comunicava gli importanti risultati di una sua esperienza(1).
Thomson conosceva i lavori e le teorie di Hertz, Lenard e Schuster e si propose di misurare la velocità con cui si propagano i raggi catodici. Era guidato dal dubbio sulla spiegazione ondulatoria dei raggi per il fatto che deviavano quando su di essi agiva un campo magnetico. Egli osservò che se i raggi catodici erano una specie di raggi ultravioletti o raggi elettromagnetici di altro tipo, per curvarli, il mezzo cioè l’etere, avrebbe dovuto avere una qualche struttura granulare che avesse una qualche relazione con il campo magnetico e questa idea non lo convinceva. Si fece l’idea che forse ai raggi fosse associato qualcosa di fortemente fosforogenico agente in modo che il vetro o altri materiali emettessero luce. In proposito scriveva:
Sono stato in grado di rilevare fosforescenza in pezzi di vetro ordinario posto ad una distanza di alcuni piedi dal tubo di scarica, benché in questo caso la luce che induceva tale fosforescenza doveva passare attraverso le pareti di vetro del tubo ed un considerevole spessore di aria prima di arrivare al corpo da rendere fosforescente.
Questa osservazione fa intendere quanto Thomson fosse vicino ad una scoperta clamorosa che mancò perché con la mente rivolta ad altri scopi e che vedremo più oltre. Thomson tentava di dimostrare che i raggi catodici non erano una specie di raggi ultravioletti anche se avevano la capacità di provocare fosforescenza. Era sicuro di poter mostrare ciò determinando la velocità dei raggi catodici mediante la misura del tempo che separava l’inizio della fluorescenza in due punti lungo il tubo, quando un fascio di raggi catodici era attivato. I due punti erano incisi sul nerofumo con cui erano state annerite le pareti interne del tubo ed il tempo era misurato osservando con uno specchio rotante il passaggio delle luce attraverso le due incisioni. Le misure di Thomson dettero per risultato che i raggi viaggiano ad una velocità di 200.000 metri al secondo, velocità che risulta più piccola di quella posseduta dalla radiazione ultravioletta (che viaggia alla velocità della luce) ed anche di molto: quest’ultima è infatti circa 1500 volte maggiore di quella dei raggi catodici. Più tardi, nel 1897, Thomson ripudiò il risultato di questa esperienza perché in altra esperienza trovò che la velocità dei raggi catodici è superiore a quella che aveva trovato. In ogni caso il risultato dell’esperimento aprì la strada a Thomson per tutta una serie di esperimenti che furono di forte sostegno alla natura corpuscolare dei raggi catodici.
L’ESPERIMENTO DI JEAN PERRIN
Nel 1895 intervenne sull’argomento il fisico francese Jean Perrin(2) che faceva ricerche per la sua tesi di dottorato. Egli ripeteva in qualche modo una delle esperienze di Hertz per verificare se i raggi catodici avessero o no carica elettrica. Egli, contrariamente a Hertz, dispose il collettore di carica dentro il tubo a raggi catodici come mostrato in figura.
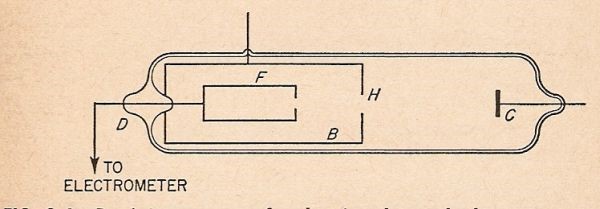
Il collettore di carica F era posto in una regione priva di carica all’interno dell’anodo B (che in questa sistemazione funzionava come una gabbia di Faraday)ed era collegato ad un misuratore di carica elettrica tramite il sostegno isolante D. I raggi catodici provenienti dal catodo C, entravano nell’anodo B attraverso un foro H. Alcuni di tali raggi erano catturati dal collettore di carica F e l’elettrometro segnava una carica negativa. Per mostrare che erano proprio i raggi catodici ad essere caricati negativamente, Perrin li deviò mediante un campo magnetico in modo che non entrassero più nel foro H: in queste condizioni l’elettrometro non segnava più carica perché, evidentemente, il collettore F non ne raccoglieva più. Queste brillanti prove furono offuscate da una circostanza estremamente sfortunata (è il caso di dirlo). Con il senno di oggi possiamo spiegare: il collettore era fatto di un metallo che colpito da particelle ad alta velocità emetteva più elettroni di quelli assorbiti con la conseguenza che il metallo risultava carico positivamente. Ciò creò qualche confusione sulla natura dei raggi catodici che, all’epoca, non si era in grado di risolvere.

Jean Perrin
L’ESPERIENZA DI THOMSON DEL 1897: L’ELETTRONE
Nel 1897 Thomson ritornò sulla questione già affrontata, con alcune informazioni in più e con propositi più ambiziosi. Lenard aveva trovato che i raggi catodici possono penetrare circa un centimetro d’aria (a temperatura e pressione ordinarie). Questa scoperta fu utilizzata da Thomson per dedurre che le supposte particelle costituenti i raggi catodici dovevano avere un diametro molto più piccolo di quello delle molecole che costituiscono l’aria. Con le sue dimensioni una molecola nell’aria può percorrere in media 10-5 centimetri prima di urtare un’altra molecola. Per percorrere circa un centimetro nello stesso ambiente senza una collisione, le supposte particelle dei raggi catodici avrebbero dovuto essere 105 volte più piccole di una molecola. Questa ipotesi insieme al fatto che il comportamento di queste particelle risultava indifferente alla natura del gas residuo nel tubo (qualunque gas vi fosse il comportamento era lo stesso) o del metallo costituente il catodo (qualunque esso fosse il comportamento era lo stesso), portò Thomson a suggerire l’idea che i raggi catodici fossero composti da particelle più piccole degli atomi o subatomiche e costituenti gli atomi di tutti gli elementi.
Gli esperimenti di Thomson del 1897 furono centrati proprio su questo. Usando tutti i risultati e le tecniche precedentemente raccolti, particolarmente quelli di Hertz, Schuster, Lenard e Perrin, egli si costruì un tubo in cui potessero agire sui raggi catodici sia campi elettrici che campi magnetici con lo scopo di misurare, non più solo la velocità delle particelle che veniva determinata a parte, ma il rapporto tra la loro carica e la loro massa. Il perché un rapporto tra grandezze e non delle singole grandezze è evidente ma va detto: perché nell’esperienza vi sono due grandezze ignote, la carica e la massa e, come con le equazioni in cui due incognite richiedono due equazioni, con un solo dato sperimentale non possono venire fuori i valori di ambedue le grandezze cercate. Sarebbe stato necessario capire, ad esempio, che le misure di Faraday nell’elettrolisi, opportunamente elaborate, erano relative a medesime grandezze e avrebbero potuto permettere di essere messe a sistema con le misure di Thomson.
Nella prima parte della sua memoria Thomson si servì, come aveva fatto Schuster, della curvatura del fascio di raggi catodici, realizzato con un campo magnetico noto, per trovare la relazione che esiste tra la velocità delle ipotetiche particelle, l’intensità del campo magnetico e il rapporto, già trovato da Schuster, tra carica e massa della particella da studiare,
(1) q/m = v/BR.
Qui Thomson aveva una sola equazione, quella fornita da Schuster, e due incognite: v e q/m. Si servì quindi di due metodi differenti per trovare v e q/m.

J.J. Thomson
Il primo metodo prevedeva di inviare il fascio di raggi in un collettore schermato elettricamente, come quello di Perrin ma più piccolo. Il fascio aveva due effetti sul collettore: da una parte gli trasferiva carica e dall’altra gli forniva calore a seguito dell’impatto meccanico. L’energia associata alla quantità di calore, H, fornita al collettore in un dato intervallo di tempo T, può essere determinata dalla massa del collettore, dal suo calore specifico e dalla temperatura raggiunta. La variazione di temperatura era misurata mediante una termocoppia collegata al collettore, mentre la quantità di carica Q arrivata al collettore era misurata con un elettrometro sensibile.
Assumendo che le particelle del fascio che colpiscono il collettore in un tempo T sono n, ciascuna di massa m, velocità v e che ciascuna particella ha carica q, da cui:
(2) Q = nq
è la carica che un dato gruppo di particelle rilascia sul collettore in un dato tempo per essere misurata che non deve però rilasciare alcuna emissione secondaria (e Thomson si assicurò di ciò mediante la citata schermatura del collettore che non avrebbe permesso la fuoriuscita di parte del fascio per rimbalzo).
L’energia cinetica rilasciata al collettore sotto forma di calore sarà la somma delle energie cinetiche di ciascuna particella:
(3) H = n.(½mv2)
Ricavando n dalla (2) e dalla (3) ed uguagliando le due espressioni, si ottiene:
(4)
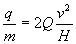
che è un’espressione che può essere uguagliata alla (1) per fornire valori numerici per v e q/m(4).
Con i dati delle misure sperimentali Thomson trovò per la velocità v ed il rapporto q/m i valori:
v ~ 3. 107 metri al secondo (circa 1/10 la velocità della luce)
q/m ~ 1,7.1011 coulomb per chilogrammo
Nella stessa memoria, come accennato, Thomson fece le misure con un metodo diverso per ricavare ancora q/m e v. Questa volta usò il tubo riportato in figura, disegnato schematicamente nelle altre due figure.

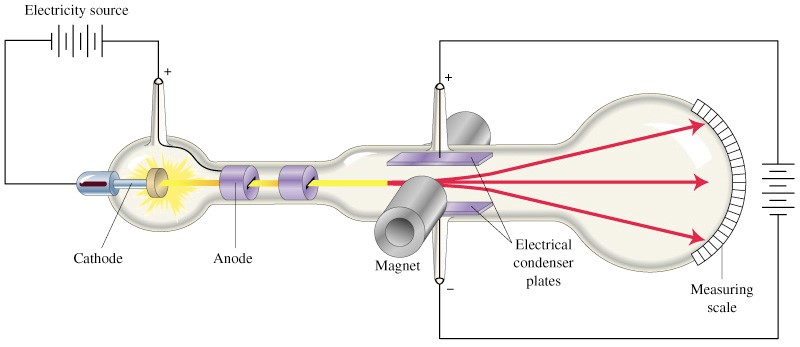
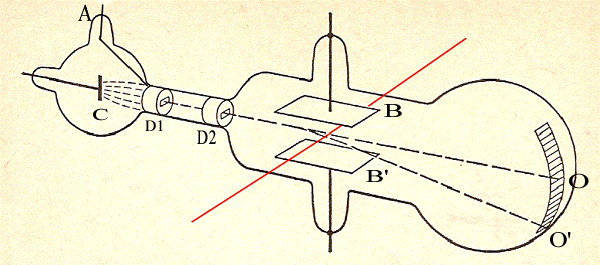
Riferendoci al tubo dell’ultimo disegno, in esso C è il catodo ed A è l’anodo mentre D1 e D2 sono due diaframmi (il primo collegato all’anodo) che servono per formare un fascio stretto di raggi catodici che determinano, in fondo al tubo, sullo schermo, una macchia fluorescente molto piccola. Le placche B e B’ che chiamiamo deviatrici, situate all’interno del tubo, generano il campo elettrico mentre il campo magnetico (misurabile con un galvanometro balistico), generato da un elettromagnete posto esternamente al tubo, agisce lungo l’asse (disegnato in rosso) perpendicolare al campo elettrico.
In assenza di campo elettrico applicato il fascio disegna un punto in O. Applicando un campo magnetico il fascio si sposta in su o in giù, andando ad esempio in O’, come mostrato in figura. Il fascio viaggia cioè in linea retta finché non entra nella zona d’azione del campo magnetico dove la traiettoria diventa un arco di cerchio di raggio R (quello che figura nella relazione 1) che può essere facilmente misurato dalla deflessione del fascio e dalle caratteristiche geometriche del tubo.
Supponiamo ora che, mentre agisce il campo magnetico, si applichi una differenza di potenziale V alle placche deviatrici. Se le placche sono a distanza D tra di esse vi sarà un campo elettrico E dato da:
(5) E = V/D
Una carica q, all’interno di tale campo, subirà una forzaelettrica Fe = Eq diretta verso l’alto o verso il basso dipendendo ciò dal segno di q e dalla direzione del campo E. Se regoliamo la differenza di potenziale applicata in modo da situare il puntino del fascio in O, da avere cioè un valore tale che la forza Eq sia numericamente uguale, ma opposta in direzione, alla forza esercitata sulla particella dal campo magnetico B, alla forza cioè di Lorentz data da Fm = Bqv, avremo:
(6) Fe = Fm
cioè:
(7) Eq = Bqv
ed in definitiva:
(8) v = E/B
Con i dati delle misure sperimentali Thomson trovò per il rapporto q/m il valore
q/m ~ 0,77.1011 coulomb per chilogrammo
Ed aggiungeva che questo valore risulta indipendente dalla natura del gas contenuto nel tubo e che il grande valore del rapporto può discendere o dal grande valore di q, o dal piccolo valore di m o da una combinazione dei due fattori.
Ancora in questa memoria Thomson espresse la sua convinzione che c’erano motivi per pensare che la carica q doveva essere più grande della carica degli ioni idrogeno nell’elettrolisi ed affermava:
In questo modo di vedere nei raggi catodici abbiamo la materia in un nuovo stato, uno stato in cui la suddivisione della materia va molto oltre che nell’ordinario stato gassoso: uno stato in cui tutta la materia – sia essa idrogeno o ossigeno o … – è di un solo tipo; essendo questa materia la sostanza da cui tutti gli elementi chimici sono costituiti.
Thomson tracciò a questo punto un segno fondamentale nella storia della fisica: non solo affermò che queste particelle erano la base di tutti gli elementi ma addirittura che erano una base. Egli propose questa idea cercando di individuare la natura e le proprietà dei vari elementi attraverso un suo supposto (sempre meno) suo costituente fondamentale. In ogni caso le scoperte di Thomson, come già avrà immaginato il lettore, non ebbero buona accoglienza nel mondo della fisica. Vi erano ancora aperte molte linee di ricerca in diversi campi perché si riuscisse ad individuare l’esperienza di Thomson come risolutiva. Una di queste linee nasceva dalla casuale scoperta che, nell’ambito delle ricerche sui raggi catodici, Röntgen aveva fatto nel 1895, una sciocchezza, i raggi X.

J.J. Thomson
L’EFFETTO ZEEMAN
E’ utile fare una digressione molto breve rispetto ai raggi catodici perché i risultati dell’esperienza che vedremo ora si ricollegano a quanto abbiamo visto scoperto da Thomson.
Nel 1889 Hertz aveva terminato di sottoporre a verifica sperimentale la teoria di Maxwell e nessuno più poteva mettere in dubbio l’esistenza delle onde elettromagnetiche, della loro propagazione a velocità finita e mediante azione a contatto. Inoltre da questo momento l’ottica e quindi la luce diventava un capitolo dell’elettromagnetismo. La teoria di Maxwell si poneva ormai come base consolidata dell’elettromagnetismo e dell’ottica. Le onde elettromagnetiche, in accordo con la teoria di Maxwell, sarebbero state originate da cariche elettriche oscillanti dentro (o in associazione con) atomi o molecole. Questa parte era puramente ipotetica tanto che lo stesso Hertz, che pure non era favorevole a teorie corpuscolari come già visto nell’articolo precedente, la aveva accettata senza problemi.

Pieter Zeeman
Nel 1896 il fisico olandese Pieter Zeeman (1865-1943) cercò di vedere il tipo di azione che un campo magnetico esterno avrebbe avuto sulla lunghezza d’onda della luce prodotta da questi ipotetici oscillatori. Si trattava in pratica di vedere anche se gli oscillatori erano o no ipotetici(5). Il suo apparato sperimentale era molto semplice: una sorgente luminosa (ad esempio, una lampada a vapori di sodio) era sistemata tra le espansioni polari di un potente elettromagnete e la luce che proveniva da questo apparato era studiata con uno spettroscopio. Nello spettroscopio trovò che le due ben note linee D del sodio (il doppietto del sodio) si erano leggermente allargate. In realtà, come fece notare il fisico britannico Oliver Lodge (1851-1940) poco tempo dopo(6) quasi simultaneamente allo stesso Zeeman, disponendo di uno spettroscopio con potere risolutivo maggiore, si sarebbe trovato che quell’allargamento era la sovrapposizione di alcune linee per ogni linea D (splitting), come mostrato nella foto(7).
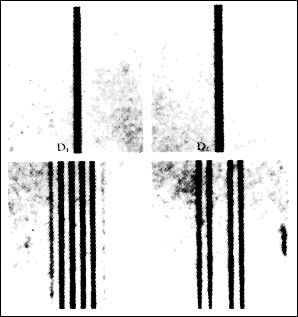
In alto le linee D1 e D2 del sodio come si osservano in condizioni normali. In basso le linee D1 e D2 diventano più linee quando la sorgente luminosa è sottoposta all’azione di un intenso campo magnetico.
Zeeman fece altre osservazioni. Mentre nell’esperienza citata l’osservazione era perpendicolare al campo magnetico, ne fece anche parallelamente ad esso scoprendo che la luce, in questo caso, risultava polarizzata circolarmente. Studiando accuratamente polarizzazione della luce e direzione del campo, Zeeman riuscì a stabilire che le particelle cariche che emettono la luce sono elettricamente dotate di carica negativa. A questo punto sembrava evidente che queste particelle oscillanti fossero le stesse che costituivano i raggi catodici.

H.A. Lorentz
Utilizzando la teoria degli elettroni di Lorentz, questo metodo di osservazione fu utilizzato per calcolare, a partire dalla dimensione dell’allargamento delle righe spettrali, il rapporto q/m che risultava lo stesso di quello che troverà Thomson.
Altre misure q/m vennero fatte con vari metodi in modi sempre più raffinati. Vale la pena ricordare la misura di Lenard del 1898 per sottolineare che egli si era convertito alla teoria corpuscolare ed è rilevante il fatto che la possente scuola tedesca inizi ad indirizzarsi su questo indirizzo speculativo e sperimentale.
Nel 1899 poi vi fu un’altra misura di Thomson, questa volta a partire dall’effetto fotoelettrico. Anche da qui si trovarono stessi valori per il rapporto q/m.
Sembrava quindi ormai scontata l’esistenza di queste piccole particelle dotate di carica negativa come costituenti dei raggi catodici. Esse si trovavano poi anche in vari altri fenomeni e sembravano un costituente comune di tutti gli elementi. A questo punto la parola doveva passare alla teoria per tentare di capire come tasli particelle potevano organizzarsi all’interno della materia che risulta comunque priva di carica. E presto si iniziò a lavorare su questo problema. A margine ci si chiese se, date queste particelle, ve ne fossero delle altre, di altro tipo e con altre caratteristiche. Vari fenomeni mostravano aspetti incomprensibili e forse riconducibili ad una visione diversa della struttura della materia. Uno di questi fenomeni era balzato clamorosamente all’attenzione del mondo della fisica, e non solo, sul finire del 1895.
WILHELM RÖNTGEN SCOPRE I RAGGI X
Wilhelm Röntgen (1845-1923) nacque nella Germania nordoccidentale da una famiglia agiata di commercianti che, per lavoro, si erano spostati in Olanda. Fu qui che Wilhelm fece i suoi primi studi, prima di passare in Svizzera. I suoi interessi iniziali furono per l’ingegneria, disciplina nella quale si laureò a Zurigo. Dopo la laurea, nel 1869, il suo professore di fisica, E.E. Kundt, lo convinse a fare ciò che non aveva mai fatto nel suo corso di laurea, ricerche sperimentali in fisica. Si dedicò all’insegnamento della fisica passando per varie scuole fino ad approdare all’Università di Würzburg (Baviera) nel 1888 e quindi a quella di Monaco nel 1900.

Wilhelm Röntgen
Nel 1895 egli si dedicava alle ricerche in cui una gran parte di fisici lavorava, quelle sui raggi catodici. Disponeva di svariati tubi, particolarmente di Crookes, Hittorf e Lenard e della strumentazione ordinaria che ogni ricercatore nel campo

Il laboratorio di Röntgen
aveva. Tra questa anche delle lastre ricoperte di varie sostanze, in particolare una di cartone, montata su un telaio di legno, ricoperta da una verniciata di platinocianuro di bario, un composto in grado di far risaltare gli effetti di fluorescenza. Mentre, con un tubo di Crookes-Hittorf (vedi figura) e con una

Il tubo utilizzato da Röntgen nei suoi primi esperimenti. © Science Museum/Science and Society Picture Library, London
schermatura di cartone nero (per oscurare completamente la stanza), era intento ad osservare un qualche fenomeno provocato dai raggi catodici si accorse che ad ogni scarica di raggi catodici, quella lastra ricoperta da platinocianuro di bario, situata casualmente lì vicino, si illuminava di una fluorescenza molto intensa(8). A questo punto la sua attenzione si spostò su questo fenomeno che studiò spostando quella lastra in varie posizioni ed in varie condizioni sperimentali. Ciò che ricavò Röntgen dalle sue osservazioni, delle quali non ci ha rilasciato documenti e dati esaurienti e precisi, era che il fenomeno doveva essere provocato da una radiazione misteriosa, per questo chiamata X. Questa radiazione invisibile proveniva dal tubo catodico e, oltre ad essere capace di impressionare lastre fotografiche ed avere un potere di penetrazione fino al momento ignoto, era in grado di attraversare il cartone nero (opaco per ogni altra luce nota, compresi i raggi ultravioletti) che schermava il tubo medesimo fino a provocare la fluorescenza della lastra posta su un tavolo prossimo a quello di lavoro. Varie altre proprietà individuò Röntgen: i raggi X trasformavano in conduttori i gas che attraversavano, scaricavano i corpi con carica elettrica, non erano deviati da campi magnetici e sembravano propagarsi in linea retta come la luce anche se non manifestavano le stesse proprietà della luce come la riflessione, la rifrazione e la diffrazione. Ma la cosa che più colpiva era appunto lo straordinario potere di penetrazione di tali raggi che variava con la natura del corpo attraversato. Fece varie prove con i materiali a disposizione nel laboratorio. Tra tubo e lastra interpose vari materiali e mentre alcuni, come la carta di un libro o un pezzo legno, facevano passare i raggi, altri, come il platino ed il piombo, li fermavano. Mise tra tubo e lastra la sua cassetta di legno contenenti i pesi della bilancia e riuscì a vederli all’interno della cassetta, mise il suo fucile da caccia e scoprì che nel ferro che lo costituiva vi era un’imperfezione. Venne naturale interporre anche la mano e qui vi fu un vero soprassalto perché sullo schermo comparve la radiografia della medesima. I raggi X risultavano penetrare la carne ma non le ossa ed anche la carne mostrava trasparenze diverse.
Röntgen non aveva documenti per far conoscere la sua scoperta e fu allora che pensò di utilizzare le lastre fotografiche per documentare la sua scoperta. Si trattava solo di sostituire la lastra ricoperta di platinocianuro di bario con una lastra fotosensibile ed ottenne risultati superiori ad ogni aspettativa. Per documentare

ciò chiese a sua moglie, Anna Bertha Ludwig, di disporre la sua mano sulla lastra fotografica e così si ottenne la prima radiografia nota della storia. Röntgen preparò una breve memoria di 10 pagine accompagnata da alcune foto che consegnò al

Radiografia della mano di Anna Bertha Ludwig Röntgen
segretario della Società di fisica medica di Würzburg. La memoria fu pubblicata il 28 dicembre 1895(9).

Anna Bertha Röntgen
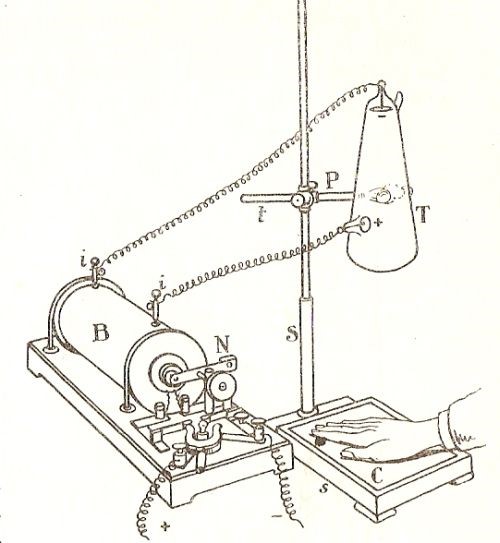
Già a gennaio 1986 tutto il mondo era al corrente della notizia. Cominciò la Presse di Vienna (5 gennaio), proseguì il New York Times (16 gennaio) e via via tutti. Vi furono gli scettici che pensarono ad un qualche scherzo e tra questi Kelvin che presto però si convinse. Naturalmente si parlava non della scoperta fisica ma delle foto che l’accompagnavano. La cosa non piaceva a Röntgen ma ormai non si poteva rimediare. In giro per il mondo si costruirono apparati rudimentali per ottenere dei raggi X in casa con ogni conseguenza sanitaria oggi intuibile. Dal 1899 numerosi medici utilizzarono l’esposizione ai raggi X per curare cancro, tubercolosi ed infiammazioni con conseguenze spesso molto brutte (al minimo forti ustioni). Qualcuno pensò addirittura di risolvere i problemi razzisti con i raggi X, cercando di utilizzarli per sbiancare i negri. Mentre l’imperatore Guglielmo II
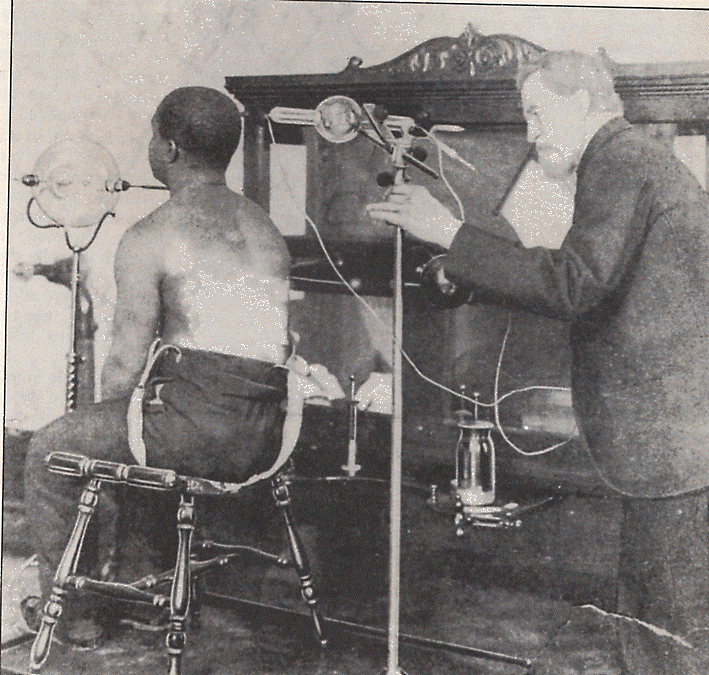
Un medico di Filadelfia (USA) mentre sbianca un negro (V. Forbin, Si possono sbiancare i negri ?, La Nature, 29 febbraio 1908).
organizzò subito una commissione per studiare le applicazioni militari della scoperta e Röntgen si rifiutò di partecipare. Sull’argomento egli scrisse ancora due brevi memorie (1896 e 1897) che riguardavano alcune proprietà dei raggi X, che era stato proposto dall’istologo E. Albert von Kölliker chiamare raggi Röntgen con il parere contrario dell’interessato, poi più nulla(10).
Altri ricercatori perfezionarono il tubo catodico utilizzato da Crookes e se ne realizzarono vari tipi. Il più noto è forse quello realizzato dal fisico americano William David Coolidge a partire dal 1913

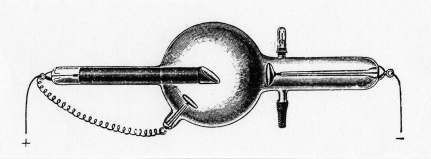
Coloro che si occupavano di fisica tentarono di capire la natura di questi raggi. Varie teorie furono proposte e tra queste due emersero in modo particolare. Una considerava i raggi X come impulsi di energia elettromagnetica emessi quando i raggi catodici urtavano della materia e ne erano bloccati. L’altra teoria considerava questi raggi come ordinarie onde elettromagnetiche ma con una frequenza molto più elevata. Solo nel 1912, con i lavori del fisico tedesco Max von Laue, si aprì la strada per rendere più accettabile la seconda teoria che si affermò piano piano con difficoltà. Anche se restava ancora da capire come tali raggi erano prodotti all’interno della materia.
BECQUEREL SCOPRE LA RADIOATTIVITA’
Il 20 gennaio del 1896 i due medici Oudin e Barthélemy presentarono all’Accademia delle Scienze di Parigi le foto delle radiografie fatte da Röntgen ed il fisico matematico Henri Poincaré (1854-1912) discusse i primi dettagli dei lavori dello stesso Röntgen. Poincaré si soffermò particolarmente sul fatto che i raggi X nascevano nell’urto dei raggi catodici sulla parte terminale del tubo quella che diventa fluorescente con i raggi catodici. Egli avanzò una prima ipotesi che i due fenomeni, la fluorescenza e la creazione di raggi X in quella parte di vetro fossero tra loro collegati. Oggi sappiamo che questa ipotesi non era corretta ma essa stimolò il desiderio di fare ricerche in proposito.

Henri Poincaré
Tra i più interessati vi era un antico condiscepolo di Poincaré alla Scuola Politecnica di Parigi, socio dell’Accademia e professore di fisica presso il Museo di Storia Naturale, Henri Becquerel (1852-1908). In lui si fece subito strada il pensiero che discendeva dall’ipotesi fatta da Poincaré: è possibile che altre sostanze per il solo fatto di essere fluorescenti o fosforescenti abbiano la caratteristica di emettere raggi X o radiazioni simili ? La cosa aveva per lui grande interesse perché era figlio di Edmond Becquerel (1820-1891) che aveva dedicato la vita allo studio delle azioni chimiche della luce, della fluorescenza nei composti dell’uranio. E subito iniziò una ricerca in tali direzione, a partire da alcune sostanze che aveva in abbondanza nel suo laboratorio e cioè di alcuni composti del potassio e dell’uranio (uranile osolfato doppio di uranio e potassio).

Henri Becquerel
Nella prima esperienza che fece iniziò con l’originare la fosforescenza dell’uranile esponendone una quantità alla luce del sole ed accertandosi di ciò mediante una lastra fotografica. Espose quindi per 4 ore alla radiazione solare una lastra fotografica protetta con molta cura con spessi fogli di carta nera per evitare che fosse impressa dalla luce. Sopra questa lastra sistemò un frammento di uranile. La fosforescenza di questo materiale avrebbe dovuto impressionare la lastra fotografica. Passate le 4 ore ritirò il tutto e controllò la lastra fotografica che presentava impressionato il profilo del frammento che era stato sistemato su di essa sotto forma di una macchia scura. Era un immediato successo che sembrava mostrare la correttezza dell’ipotesi fatta: la fosforescenza di un dato materiale attraversava fogli di carta nera, non attraversati dalla luce, ed impressionava una lastra fotografica, proprio come i raggi X. Il 24 febbraio 1896 Becquerel annunciò la sua scoperta(11).

Una lastra fotografica impressionata dal minerale di uranio
L’idea era di fare altre esperienze per il 26 ed il 27 febbraio ma, poiché il cielo era coperto di nubi, rimandò i suoi lavori. Nel frattempo, dispose alcuni minerali di uranio che aveva sul tavolo da lavoro dentro un cassetto della sua scrivania, cassetto nel quale erano conservate anche le lastre fotografiche rigorosamente protette da involti di carta nera. Nel cassetto non entrava luce ed i minerali di uranio erano poggiati sulle lastre fotografiche. Quando finalmente ricomparve il sole, Becquerel estrasse le lastre ed il minerale di uranio per fare le sue esperienze. Ebbe cura di controllare lo stato delle lastre e le trovò rovinate, completamente inutilizzabili per le macchie scure che presentavano, simili a quelle disegnate nel primo esperimento. Eppure questo minerale di uranio non era stato esposto alla luce per provocarne la fosforescenza … Volle accertarsi che non vi fossero stati difetti di alcun tipo nella cura dei materiali e ripeté quanto accaduto come esperienza controllata. Sistemò un sale di uranio non esposto alla luce sopra una lastra fotografica protetta dalla luce e mise il tutto per qualche giorno dentro un recipiente buio. Il risultato fu molto chiaro: senza che si fosse prodotta fosforescenza o fluorescenza mediante luce, la lastra era impressionata con la silhouette del metallo che era stato sistemato su di essa. Una sola conclusione era possibile: quel materiale emetteva una qualche radiazione diversa da quella X(12). Più oltre, nello stesso anno, lo stesso Becquerel arrivò ad una conclusione di grande importanza: quella radiazione proviene dall’uranio indipendentemente dal suo stato di composizione chimica ed essa è emessa con continuità. Era la scoperta della radioattività che impegnò subito i fisici in tutti i laboratori del mondo con un susseguirsi frenetico di scoperte.
Nei Laboratori Cavendish, diretti all’epoca da J.J. Thomson, il giovane fisico chimico Ernest Rutherford (1871-1937), arrivato dalla Nuova Zelanda nel 1895, iniziò a studiare la radiazione di Becquerel e scoprì che era formata da due componenti con comportamenti differenti che egli chiamò raggi α (alfa) e raggi β (beta). La prima era assorbita da un foglio di carta o da una sottile foglia metallica mentre la seconda penetrava invece in spessori considerevolmente più grandi (ad esempio: poco meno di mezzo centimetro di alluminio)(13).
Nel 1898 la fisica chimica polacca Maria Skłodowska (1867-1934) con suo marito il fisico francese Pierre Curie (1856-1906) in Francia e Schmidt in Germania scoprirono che il torio ha le stesse proprietà dell’uranio. Nello stesso anno, ancora Maria e Pierre Curie riuscirono a separare dalla pechblenda (un minerale che contiene uranio) due nuovi elementi, ambedue radioattivi, il polonio (nome dato a questo elemento in onore del Paese natale di Maria Curie) ed il radio (poiché questo elemento aveva intense proprietà di emettere radiazioni, fu chiamato da Maria Curie radio). Ancora in quell’anno Rutherford (trasferito momentaneamente ad insegnare a Montreal) insieme ad Owens scoprì il thoron, un gas emesso dal torio (che oggi sappiamo essere un isotopo del radon). A partire da qui si susseguirono le scoperte di nuovi elementi radioattivi. Furono ancora Rutherford e Soddy che tra il 1900 ed il 1903 capirono le successive trasformazioni delle sostanze radioattive ed introdussero il concetto di decadimento. Anche il concetto di isotopia nacque in questi anni con i lavori di Crookes, Hahn, Soddy, Baltwood ed altri. Si capì che le particelle alfa che sono deflesse da un campo magnetico, sono nuclei di elio e quindi corpuscoli carichi positivamente.
Nel 1899, Geiser, Becquerel, Meyer e Schweilder, mostrarono indipendentemente che i raggi beta sono deflessi da un campo magnetico e quindi che sono composti da corpuscoli negativi. A questo proposito Kaufmann mostrò che il rapporto tra carica e massa per i raggi beta è approssimativamente lo stesso trovato per i raggi catodici.
Nel 1900 il fisico francese Paul Ulrich Villard (1860-1934) mostrò che vi è un terzo tipo di radiazione emessa dalle sostanze radioattive. Si tratta di raggi estremamente penetranti che non sono deflessi da campi magnetici. Sono simili ai raggi X ma con frequenza maggiore. Li chiamò raggi γ (gamma)(14).
GOLDSTEIN SCOPRE I RAGGI CANALE
Occorre a questo punto dare un cenno di una scoperta fatta qualche anno prima dal fisico tedesco Eugene Goldstein (1850-1930). Egli, studiando i raggi catodici, pensò di fare dei buchi sul catodo di un tubo a vuoto per vederne l’effetto.

In queste condizioni Goldstein osservò un altro tipo di radiazione che si aggiungeva a quella ordinaria dei raggi catodici che andava dal catodo verso l’anodo(15). Questa nuova radiazione (chiamata kanalstrahlen o raggi canale o raggi positivi) passava attraverso i buchi (i canali) del catodo per andare ad urtare l’involucro di vetro del tubo catodico dietro il catodo medesimo. Questi raggi viaggiano quindi in direzione opposta ai raggi catodici e devono quindi trasportare una carica opposta che deve essere positiva. E le proprietà di tali raggi furono mostrate da Wien nel 1897(16). Egli trovò, tramite l’azione di campi magnetici ed elettrici, che essi hanno carica positiva ed un rapporto tra carica e massa molto più grande di quello dei raggi catodici. Per avere misure precise su questo, per le difficoltà che nascono dal fatto che tali raggi ionizzano fortemente l’aria residua nel tubo, occorrerà aspettare le misure di J.J. Thomson del 1913(17).
A CHE PUNTO SIAMO
Una lettura anche superficiale di quanto qui riportato mostra con chiarezza che sul finire dell’Ottocento vi è una messe di risultati che si accumulano con grandi difficoltà teoriche di ordinarli ed interpretarli in una qualche teoria complessiva. Raggi catodici, raggi canale, raggi X, raggi alfa, beta e gamma …sono capitoli enormi e creano problemi grandissimi. Se questi problemi li sommiamo a quelli posti dal corpo nero ed a quelli che nascono dalle elaborazioni della teoria elettromagnetica e del suo rapporto con un preteso etere, ci si rende conto che la fisica era in difficoltà enormi. Molti fisici di grandissima levatura erano comunque all’opera e, pur tra grandi contraddizioni, piano piano incanalarono il tutto in visioni che iniziarono ad andare d’accordo, ad essere esplicative e propositive di nuovi problemi e gigantesche sfide. Da tutte queste scoperte e difficoltà stavano per nascere: la fisica dei quanti, iniziata da Planck proprio sul finire dell’anno 1900; la fisica relativistica introdotta da Einstein nel 1905; poi la nascita della fisica nucleare, quella delle alte energie, la teoria dei campi, …. Insomma un mondo completamente diverso ma ben ancorato ai principi che faticosamente erano stati messi insiemi in secoli di faticoso e complesso lavoro. La sfida più immediata che nasceva all’alba del nuovo secolo e che merita di essere discussa è quella della struttura della materia con la nascita della fisica atomica. Un discorso che partendo dall’antichità classica porta fino ai modelli atomici più recenti l’ho già fatto e si può trovare in Atomi e Molecole e pagine seguenti. Dovrò aggiungere qualcosa in prossimi lavori.
NOTE
(1) J. J. Thomson, Phil. Mag. 38, 358, 1894.
(2) Jean Perrin, Comptes Rendus 121, 1130 (1895).
(3) J. J. Thomson, On Cathode Rays, Phil. Mag., 44, 293, aprile 1897.
J. J. Thomson, On Cathode Rays, Phil. Mag., 44, 311, aprile 1897
(4) Il fisico irlandese George Francis Fitzgerald (1851-1901), subito dopo la pubblicazione del lavoro di Thomson, scrisse un articolo (Electrician, 39, 103, maggio 1897) nel quale sostenne che il lavoro di Thomson era pieno di ipotesi non apertamente affermate. L’equazione (3) del testo è vera solo se si fanno delle ipotesi come le seguenti: ciascuna particella carica deve dare tutta la sua energia al collettore e tutta questa energia deve essere convertita in calore; nessuna quantità di energia termica deve essere dispersa negli elementi che circondano il collettore. Inoltre una termocoppia non sembrava a Fitzgerald in grado di misurare differenze di temperatura così piccole così come l’elettrometro ad evidenziare la carica accumulata dal collettore.
(5) P. Zeeman, Zittingsversl. Amsterdam 5, 181, 242, 1896.
(6) O. Lodge, Proc. Roy. Soc. London 60, 466, 513, 1896.
O. Lodge, Proc. Roy. Soc. London 61, 413, 1896.
(7) L’interpretazione di questo fenomeno (lo splitting delle linee spettrali) non era semplice e Zeeman la fece con l’ausilio del grande fisico olandese Hendrik Antoon Lorentz (1853-1928), il padre della teoria degli elettroni. Si deve osservare che questa idea di particelle cariche era stata anticipata teoricamente dalla teoria degli elettroni di H. A. Lorentz sin dai primi anni ‘90 dell’Ottocento ( H. A. Lorentz, La théorie électromagnetique de Maxwell et son application aux corps mouvants, Arch. néerl., 25, p. 363, 1892), una teoria alla quale aveva dato il suo contributo anche Poincarè (J. H. Poincaré, A propos de la thèorie de M. Larmor, L’Eclairage électrique, 3, pp. 5-13, 285-295, 1895 e 5, pp. 5-14, 385-392, 1895) prima della scoperta sperimentale del 1897 da parte di Thomson. Secondo Lorentz (Phil. Mag. 43, 232, 1897) se si assume che l’emissione di luce ha luogo da piccole particele cariche che ruotano in orbite negli atomi, si può predire una piccola contrazione o espansione delle orbite quando viene applicato un campo
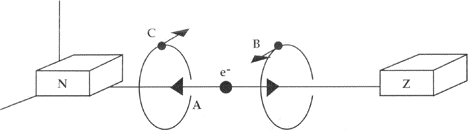
magnetico esterno. L’espansione o contrazione delle orbite avrà l’effetto di una piccola variazione della lunghezza d’onda della radiazione elettromagnetica emessa. E questa variazione può essere calcolata se si conosce il rapporto q/m delle particelle orbitanti e l’intensità del campo magnetico. Ecco allora che dal lavoro combinato dei due fisici olandesi nasce la predizione di piccole particelle cariche ruotanti negli atomi e, dall’allargamento delle linee spettrali, anche il calcolo di quel rapporto q/m, molto vicino al valore trovato da Thomson un anno dopo con l’esperienza raccontata più su.
(8) I fenomeni osservati da Röntgen erano certamente stati osservati da altri ma nessuno prestò ad essi la dovuta attenzione. Si sa per certo che intorno al 1880 Crookes aveva osservato che le lastre fotografiche poste vicino ai tubi per raggi catodici si rovinavano presentando dell macchie sulla loro superficie. Le rimandava al suo fornitore lamentando i difetti che esse presentavano.
(9) W. K. Röntgen, Über eine neue Art von Strahlen (Su una nuova specie di raggi) Sitzungsberichte der Würzburger Physikalischen-Medicinischen Gesellschaft, 28 dicembre 1895. Questo lavoro venne rapidamente tradotto in inglese:
Stanton, Arthur (1896-01-23), Wilhelm Conrad Röntgen On a New Kind of Rays: translation of a paper read before the Würzburg Physical and Medical Society, 1895, Nature 53: 274–6, (23 January 1896).
Riporto di seguito l’intera prima memoria in traduzione italiana come riportata in Pizzetti:
UNA NUOVA SPECIE DI RAGGI
di Wilhelm Conrad Rontgen
1. Lasciando passare attraverso un tubo Hittorf ad alta rarefazione oppure attraverso un apparato Lenard, Crookes e simili, sufficientemente rarefatto, la scarica di un grande rocchetto di Ruhmkorff e coprendo il tubo con un mantello aderente di leggero cartone nero, si può vedere, in una camera completamente buia, come uno schermo di carta, messo nelle vicinanze dell’apparato coperto di cianuro di bario e di platino, si illumina e diventa fluorescente a ogni scarica, non importando se la parte ricoperta dal cianuro oppure l’altra siano rivolte verso l’apparecchio di scarica. La fluorescenza può essere vista a due metri di distanza dall’ apparato. Ci si convince facilmente che la fluorescenza proviene dall’apparto di scarica e da nessun altro luogo.
2. In primo luogo ciò che ci sorprende in questo fenomeno è che attraverso il cartone nero, che non lascia passare alcun raggio visibile, né ultravioletto della luce solare o elettrica, passi un agens che è in grado di produrre una viva fluorescenza: bisogna però studiare se altri corpi hanno tale facoltà.
Si scopre che tutti i corpi vengono attraversati ma in gradi molto differenti. Cito alcuni esempi: la carta viene penetrata molto facilmente. Ho visto illuminarsi notevolmente lo schermo dietro un libro rilegato di circa 1000 pagine; la stampa non offre infatti un ostacolo visibile.
Ugualmente fu per un doppio mazzo di carte di whist: una singola carta tenuta tra lo schermo e l’apparato non è quasi visibile per l’occhio umano; lo stesso avviene per un semplice foglio di stagnola: solamente dopo averne messi vari strati se ne vede l’ombra sullo schermo. Grandi blocchi di legno, assi di legno di pino dello spessore di 2-3 cm. vengono attraversati assorbendo pochissimo.
Uno strato di alluminio dello spessore di 15 mm. indeboli notevolmente l’effetto senza però fare scomparire. la fluorescenza. Fogli di gomma dura, alti alcuni centimetri, lasciano passare i raggi. Lastre di vetro di uguale spessore si comportano diversamente, secondo se contengono piombo (flitglas) o no. Le prime offrono un maggior ostacolo delle seconde. Tenendo la mano tra lo schermo e l’apparato di scarica, si vedono le ombre pili scure delle ossa della mano e una più lieve causata da tutta la mano. Acqua, carburo di zolfo e altri liquidi, sperimentati in recipienti di mica, sono risultati di assai facile penetrazione. Non ho trovato che l’idrogeno venga attraversato molto più facilmente dell’aria. Attraverso lastre di zinco, argento, piombo, oro, platino la fluorescenza si vede chiaramente solo se lo spessore delle lastre non è notevole. Platino di 0,2 mm. viene ancora attraversato. Le lastre di argento e di zinco possono essere di spessore anche maggiore. Piombo di 1,5 mm. non viene penetrato ed è quindi molto usato per queste sue qualità. Un bastone di legno, dalla sezione trasversale 20 per 20 mm., una parte del quale era imbiancato di biacca, si comporta diversamente secondo come viene messo tra l’apparato e lo schermo. Non viene quasi attraversato se i raggi X passano parallelamente alla parte imbiancata, si vede un’ ombra nel caso contrario.
In una sequenza simile a quella dei metalli, anche i sali si possono ordinare secondo la possibilità di venir attraversati.
3. I risultati degli esperimenti riferiti, portano alla conseguenza che varie sostanze, con uguale spessore di strati, vengono penetrate essenzialmente in rapporto alla loro densità: nessuna altra qualità viene notata in così alto grado. I seguenti esperimenti dimostrano però, che non solo la densità è decisiva. Ho voluto provare come venissero penetrate lastre di uguale spessore di vetro, alluminio, spato d’Islanda, quarzo; la densità di tali sostanze era quasi uguale, ma risultò evidente che lo spato d’Islanda veniva penetrato molto meno delle altre sostanze, che si comportavano similmente tra di loro. Non ho notato una fluorescenza maggiore dello spato di Islanda nei confronti del vetro.
4. Se lo spessore aumenta, le sostanze vengono penetrate meno profondamente: per arrivare a un rapporto ho scattato alcune fotografie, per le quali la lastra fotografica era parzialmente ricoperta da strati di stagnola, il cui numero dei fogli diveniva sempre maggiore: una misurazione fotometrica verrà effettuata, quando avrò un fotometro.
5. Di platino, piombo, zinco, alluminio vennero preparate delle lamiere di spessore tale da venir penetrate. […] i diversi metalli non vengono penetrati nel medesimo modo quando il prodotto dello spessore e della densità è uguale. La penetrazione aumenta in modo molto maggiore di quanto il prodotto diminuisce.
6. La fluorescenza del cianuro di platino e bario non è il solo effetto provocato dai raggi X. Per prima cosa bisogna far notare che altri corpi possono essere fluorescenti; così anche i composti di calcio, il vetro di uranio, il vetro comune, lo spato d’Islanda e il salgemma.
Di importanza notevole è il fatto che lastre fotografiche asciutte si sono dimostrate sensibili ai raggi X. Siamo in grado di fissare alcuni fenomeni, cosi le mistificazioni vengono via via escluse; io ho controllato con una fotografia, appena ne avevo la possibilità, tutte le osservazioni importanti che ho fatto sullo schermo. Con ciò si può dimostrare la facoltà dei raggi di penetrare quasi indisturbati gli strati di legno, carta e stagnola: si può fare una fotografia in una camera illuminata se la lastra fotografica è in una piccola cassa o in una scatola di cartone. D’altra parte, questa facoltà ha come conseguenza che non si possono lasciare per lungo tempo le lastre non sviluppate in prossimità dell’apparato di scarica, protette solo dall’abituale coperchio di cartone e carta. E’ ancora incerto se l’effetto chimico sui sali d’argento della lastra fotografica derivi direttamente dai raggi X. E’ possibile che questo provenga dalla luce fluorescente che, come detto sopra, si forma nella lastra di vetro o nello strato di gelatina. “Pellicole” possono venire usate con lo stesso risultato delle lastre di vetro. Non ho ancora sperimentato se i raggi X abbiano il potere di emanare calore; ma si può ritenerla una qualità certa: giacché abbiamo dimostrato che i raggi X possono venire mutati per mezzo del fenomeno della fluorescenza, è certo anche che non tutti i raggi X visibili escano da un corpo nello stesso stato in cui sono entrati. La retina dell’ occhio non è sensibile ai nostri raggi; posto vicinissimo all’apparato di scarica, esso non vede nulla, anche se secondo le nostre esperienze l’occhio dovrebbe venir penetrato abbastanza sensibilmente dai raggi.
7. Dopo aver visto che vari corpi, di spessore relativamente grande, venivano penetrati, mi affrettai a vedere come si comportavano i raggi X passando attraverso un prisma, se cioè venivano deviati o no. Esperimenti con acqua e carburo di zolfo in prismi di mica con l’angolo di rifrazione di circa 30° non hanno lasciato scorgere alcuna deviazione, né sullo schermo fluorescente né sulla lastra fotografica. Per un paragone si osservò la deviazione della luce normale negli stessi rapporti: la deviazione era di 10-20 mm. in rapporto ai raggi non deviati. Per mezzo di un prisma di alluminio e uno di gomma dura, mantenendo l’angolo di rifrazione di circa 30°, ho ottenuto delle fotografie sulla lastra fotografica, nelle quali si può forse notare una deviazione. Ma la cosa è incerta e la deviazione, se veramente esiste, è cosi piccola che l’esponente di rifrazione dei raggi X sarebbe al massimo 1,05. Con lo schermo fluorescente non ho potuto constatare, nemmeno in questo caso, una deviazione. Non ho ottenuto fin’ora dei risultati sicuri con prismi di metalli più compatti, dato che essi non possono venire profondamente penetrati e l’intensità dei raggi uscenti è perciò molto piccola. Considerato da un lato lo stato di cose, e dall’altro l’importanza della domanda se i raggi vengono rifratti passando da un mezzo all’altro, è molto utile che ciò si possa determinare con un metodo diverso da quello dei prismi. Corpi polverizzati, con uno spessore di strati sufficiente, lasciano passare la luce che vi cade in parte minima, a causa della rifrazione e della riflessione: se le polveri lasciano passare i raggi nel modo simile ai corpi compatti (la massa deve essere naturalmente uguale) allora si è data la dimostrazione che non vi è né una rifrazione né una riflessione regolare in quantità visibile. Gli esperimenti furono fatti con salgemma polverizzato, con polvere di argento fine, ottenuta per via elettrolitica e con polvere di zinco, usata spesso negli esperimenti chimici. In tutti questi esperimenti non si rilevò nessuna differenza rispetto a quelli compiuti con i corpi, né sullo schermo né sulla lastra fotografica. Che non si possano concentrare i raggi con la lente, è chiaro da quanto è stato detto: infatti una grande lente di gomma dura e una lente di vetro si dimostrarono completamente inutili. L’ombra di un bastone rotondo è più scura nel mezzo che ai lati; quella di un tubo contenente una sostanza che lasci penetrare i raggi più facilmente del materiale del tubo, è più chiara nel mezzo che ai lati.
8. La domanda sulla riflessione dei raggi X può essere risolta con gli esperimenti del paragrafo 7: non vi è cioè una regolare riflessione dei raggi per nessuna delle sostanze sopra sperimentate. Altri esperimenti che descriverò più avanti conducono allo stesso risultato. Vi è da aggiungere un’osservazione che al primo sguardo sembra contrastare. Io esposi ai raggi X una lastra fotografica, protetta dalla luce con carta nera, con il lato del vetro verso 1’apparato di scarica: la parte sensibile era ricoperta, ad eccezione di un pezzo libero, di lastre di platino, piombo, zinco e alluminio, disposte a forma di stella. Sulla negativa si può vedere che l’ombra nera sotto il platino, il piombo, e specialmente sotto lo zinco, è più forte che in altre parti. L’alluminio non ha esercitato alcun effetto. Sembra con ciò che i tre metalli riflettano i raggi, ma ci sarebbero altre cause per l’ombra nera, e per essere sicuro misi tra lo strato sensibile e le lastre di metallo un leggero pezzo di foglia di alluminio, che non lascia passare i raggi ultravioletti, ma lascia passare molto facilmente i raggi X. Dato che anche il secondo esperimento ebbe il risultato del primo, si è dimostrata la riflessione dei raggi X per i detti metalli. Se si tiene presente questo fatto, con 1’osservazione che la polvere viene penetrata come i corpi compatti, che i corpi con superficie ruvida si comportano ugualmente dei corpi lisci, come risulta dall’ultimo esperimento, si viene alla determinazione che non avviene una riflessione regolare, ma che i corpi si comportano verso i raggi X come i mezzi torbidi con la luce.
Dato che non ho potuto dimostrare una rifrazione per il passaggio da un mezzo all’ altro, cosi penso che i raggi X si muovano con uguale velocità in tutti i corpi, e cioè in un mezzo esistente in ogni cosa, nel quale si trovano gli elementi del corpo. Questi ultimi sono di ostacolo per la diffusione dei raggi X, ostacolo generalmente tanto più grande quanto pili compatto è il corpo.
9. Perciò potrebbe essere possibile che anche l’ordinamento degli elementi influisca sul modo come il corpo viene penetrato, che per esempio un pezzo di spato d’Islanda con spessore uguale, venga penetrato in modo differente se i raggi lo attraversano in direzione dell’ asse o verticalmente ad esso. Esperimenti con spato e quarzo hanno dato risultati negativi.
10. E’ noto che Lenard, con i suoi esperimenti sui raggi catodici Hittorf attraverso un leggero foglio di alluminio, sia arrivato al risultato che questi raggi sono emessi nell’atmosfera e scorrono diffusamente in tutti i corpi. Dei nostri raggi possiamo dire qualche cosa di simile. Nel suo ultimo lavoro, Lenard ha stabilito la capacità di assorbimento dei vari corpi per i raggi catodici e per l’aria con pressione atmosferica di 4,10 3,40 3,10 in rapporto a 1 cm. secondo la rarefazione dei gas contenuti nell’apparato di scarica. Calcolando la tensione di scarica secondo la lunghezza di scintilla, ho avuto nei miei esperimenti quasi sempre la stessa rarefazione e raramente essa fu maggiore o minore. Riuscii, con un fotometro L. Weber (non ne posseggo uno migliore), a paragonare nell’ aria atmosferica l’intensità della luce fluorescente del mio schermo a due distanze diverse, circa 100 e 200 mm. dall’apparato di scarica. Ho trovato da tre esperimenti riusciti perfettamente, che l’intensità è inversamente proporzionale alla distanza dello schermo dall’ apparato di scarica. Perciò l’aria ritiene una percentuale molto minore dj raggi X che non di raggi catodici. Questo risultato è concorde con l’osservazione che la luce fluorescente può essere vista a 2 m. di distanza. Similmente all’aria si comportano gli altri corpi: essi lasciano passare meglio i raggi X dei raggi catodici.
11. Un’ altra differenza notevole tra i raggi X e quelli catodici sta nel fatto che non sono riuscito, malgrado vari sforzi, a ottenere una deviazione dei raggi X con un magnete, anche in presenza di campi magnetici molto forti. È invece una caratteristica dei raggi catodici il venir deviati da una calamita; è vero che Hertz e Lenard avevano osservato che vi sono vari tipi di raggi catodici, che si distinguono secondo la produzione di fosforescenza, il potere di assorbimento e la deviazione per mezzo di magnete, ma fu constatata una grande deviazione in tutti gli esperimenti da loro eseguiti, e non credo che si capovolgerà questa convinzione se non per un motivo che costringa a farlo.
12. Secondo esperimenti fatti appositamente per tale scopo, si può considerare quale punto di partenza per il diffondersi dei raggi X in tutte le direzioni, il luogo nella parete dell’apparato di scarica che è maggiormente fluorescente. I raggi X escono dal punto dove, secondo i dati di molti scienziati, i raggi catodici toccano la parete di vetro. Se si deviano i raggi catodici nell’ apparato di scarica per mezzo di un magnete, si vede che anche i raggi X escono da un’altra parte, cioè dal punto finale dei raggi catodici. Anche da questo punto, i raggi X che non possono essere deviati, non possono essere raggi catodici riflessi o lasciati passare dalla parete di vetro. Un maggior spessore del vetro fuori dell’apparato di scarica non è ritenuto responsabile, secondo Lenard, della grande differenza di deviazione. Arrivo perciò al risultato che i raggi X non sono uguali ai raggi catodici, ma che essi vengono prodotti dai raggi catodici nella parete di vetro dell’apparato di scarica.
13. Essi non vengono prodotti esclusivamente dal vetro, ma anche nell’ apparato chiuso da lamiera di alluminio spessa 2 mm. Altre sostanze devono essere sperimentate più avanti.
14. Il diritto di usare il nome di “raggio” per l’agens proveniente dalla parete dell’ apparato di scarica, lo prendo dal formarsi regolare dell’ombra, che appare mettendo corpi differenti tra l’apparato e lo schermo fluorescente (o la lastra fotografica). Ho osservato e fotografato tali ombre la cui apparizione ha un interesse particolare: così sono in possesso di fotografie del profilo di una porta, che divide due camere, in una delle quali vi è l’apparato, nell’altra la lastra fotografica; delle ombre delle ossa della mano; dell’ombra di un filo arrotolato su una bobina di legno; di una serie di pesi contenuta in una cassetta; di una bussola nella quale l’ago magnetico è tutto incapsulato in metallo; di un pezzo di metallo la cui inomogeneità viene messa in rilievo dai raggi X, ecc. Per la diffusione rettilinea dei raggi X è importante una fotografia che ho eseguito con l’apparato di scarica avvolto in carta nera: la fotografia è debole ma esattissima.
15. Ho cercato di constatare gli effetti di interferenza per i raggi X, ma purtroppo senza risultato, forse per la debole intensità di questi raggi.
16. Abbiamo iniziato degli esperimenti per constatare se forze elettrostatiche influiscano in qualche modo sui raggi X, ma tali esperimenti non sono terminati.
17. Se ci si pone la domanda che cosa siano i raggi X, dato che non sono raggi catodici, si potrebbe pensare, in un primo momento, che essi siano luce ultravioletta, considerando la loro forte fluorescenza e i loro effetti chimici. Ma subito si è in controsenso in quanto:
a – passando dall’aria all’acqua, al carburo di zolfo, all’alluminio, al salgemma, al vetro, allo zinco ecc. essi non vengono rifratti notevolmente;
b – essi non possono venire riflessi regolarmente dai corpi sopraindicati;
c – essi non possono venire polarizzati dai mezzi usati comunemente;
d – Il loro assorbimento viene determinato solamente dalla compattezza del corpo.
Ciò vorrebbe dire che questi raggi ultravioletti si comportano differentemente dai raggi infrarossi, visibili e ultravioletti fino ad ora conosciuti. Poiché io non sono convinto di ciò, ho cercato un’altra soluzione. Sembra esistere una parentela fra i nuovi raggi e la luce, cosi indicano la formazione dell’ombra, la fluorescenza e l’effetto chimico, che sono uguali per ambedue i raggi. Da molto tempo si sa che oltre le oscillazioni della luce in direzione trasversale, vi potrebbero essere anche, quelle longitudinali nell’atmosfera e, secondo vari fisici, devono esserci. In verità la loro esistenza non è ancora provata e perciò le loro qualità non sono state sperimentate. I nuovi raggi non potrebbero essere oscillazioni longitudinali ? Devo confessare che nel corso degli esperimenti mi sono posto questo problema sempre di più e mi azzardo a scriverlo anche qui, sebbene sappia che questa spiegazione avrebbe bisogno di una nuova dimostrazione.
Wiirzburg. Istituto di Fisica dell’Università.
Dicembre 1895.
(10) C’è solo da ricordare che Röntgen, per la sua scoperta, fu insignito del Premio Nobel per la fisica. Il primo premio Nobel, quello del 1901. Vari altri premi Nobel vennero assegnati sulle ricerche relative ai raggi catodici: nel 1902 Hendrik A. Lorentz e Pieter Zeeman; nel 1905 Philipp Lenard; nel 1906 J.J. Thomson. Altri Nobel sono poi andati a due fisici dei quali mi sono occupato: 1904 Lord Rayleigh e 1911 Wilhelm Wien. Ed altri saranno dati a Maria e Pierre Curie, Henri Becquerel (1903) e per la chimica a Rutherford (1908) ed ancora a Maria Curie (1911).
(11) H. Becquerel, Comptes Rendus, 122, 406, 1896.
(12) H. Becquerel, Comptes Rendus, 122, 501, 1896.
(13) E. Rutherford, Phil. Mag., 47, 109, 1899.
(14) P. Villard, Comptes Rendus, 130, 1178, 1900.
(15) E. Goldstein, Berlin Sitzungber. p. 691, 1886.
(16) W. Wien, Verhandl. deut. physik. Ges. zu Berlin, 16, 165, 1897.
(17) J.J. Thomson, Proc. Roy. Soc. London, 59, 1, 1913.
BIBLIOGRAFIA
(1) AA. VV. – Scienziati e Tecnologi dalle origini al 1875 – EST Mondadori 1975
(2) Emilio Segrè – Personaggi e scoperte nella fisica classica – EST Mondadori 1983
(3) E. Whittaker – A History of Theories of Aether and Electicity – Nelson and Sons 1952
(4) Articoli di Enrico Bellone in: Paolo Rossi (diretta da) – Storia della scienza – UTET 1988
(5) Max Born – Atomic Physics – Blackie & Son, London 1962
(6) Max Born – La sintesi einsteniana – Boringhieri 1969
(7) Guido Tagliaferri – Storia della fisica quantistica – Franco Angeli 1985
(8) Mario Gliozzi – Storia della fisica – in: N. Abbagnano (diretta da) – Storia delle Scienze, UTET 1965
(9) René Taton (diretta da) – Storia generale delle scienze – Casini 1965
(10) John L. Heilbron – I dilemmi di Max Planck – Bollati Boringhieri 1988
(11) Piero Caldirola – Lezioni di fisica teorica – Viscontea, Milano, dopo 1950
(12) Samuel Tolansky – Introduzione alla fisica atomica – Boringhieri 1966
(13) Donald S.L. Cardwell – Tecnologia, scienza e storia – Il Mulino 1976
(14) A. Baracca, S. Ruffo, A. Russo – Scienza e industria 1848 – 1915 – Laterza 1979
(15) Enrico Persico – Gli atomi e la loro energia – Zanichelli 1970
(16) Jean Perrin – Les atomes – Gallimard 1970
(17) René Taton – Causalités et accidents de la découverte scientifique – Masson et Cie., 1967
(18) Giorgio Cosmacini – Röntgen – Rizzoli 1984
(19) Maurice de Broglie – Atomes, radioactivité, transmutations – Flammarion 1939
(20) David L. Anderson – The Discovery of the Electron – D. van Nostrand Company 1964
(21) William Bragg – Il mondo della luce – Tumminelli & C. 1935
(22) Samuel Glasstone – Sourcebook of Atomic Energy – D. van Nostrand 1950
(23) Graham Farmelo – La scoperta dei raggi X – Le Scienze 329, gennaio 1996
(24) L. Pearce Williams – Michael Faraday – Chapman & Hall Limited 1965
(25) Michael Faraday – Esperimental Researches in Elecricity – Encyclopedia Britannica 1952
(26) Giuseppe Bruzzaniti – Dal segno al nucleo – Bollati Boringhieri 1993
(27) Pino Donizetti – I cacciatori di ombre – Mondadori 1978
Categorie:Senza categoria
Rispondi