PRECEDENTI(1)
Sul finire dell’Ottocento si accumulavano indizi sempre più solidi su una possibile costituzione corpuscolare della materia. Vi erano state anche alcune misure, tra cui quella di J.J. Thomson, e alcune ripetute più volte che rafforzavano tale indizio. Questi indizi erano però del tutto incompleti ed a margine vi erano varie cose fuorvianti. Intanto era un dato indiscutibile che la materia era ed è neutra, non presenta cioè, in condizioni normali, carica elettrica. Ad un certo punto sorgono, da esperienze sui raggi catodici, dei corpuscoli dotati di carica negativa, quelli che saranno chiamati elettroni(2). Vi sono poi delle cariche positive che vengono individuate nei raggi canale. Come i due tipi di carica siano organizzati nella materia (ammesso che da lì provengano) non si sa. D’altra parte in esperienze di natura diversa dai raggi catodici vengono fuori altre radiazioni prive di carica che non si capisce bene cosa siano e quale ruolo ricoprirebbero in una eventuale organizzazione nella materia. Da esperienze del tutto diverse vengono fuori indizi simili. Nei fenomeni radioattivi si individuano dei corpuscoli con carica positiva che fuoriescono da alcuni materiali, poi vengono trovati quelli di carica negativa ed infine altre radiazioni prive di carica. Vi sono i corpuscolaristi, soprattutto britannici, che lavorano fermamente sulla strada del capire qual è la struttura della materia tentando di capire l’organizzazione in essa dei corpuscoli e delle radiazioni individuate. Altri, quelli che rifiutano l’idea di materia corpuscolare, sempre in minor numero, tentano in tutti i modi di ricondurre i fenomeni sperimentalmente dimostrati ad una qualche teoria ondulatoria e quindi del continuo. Cercherò ora di seguire i vari contributi che si sono susseguiti nei primi anni del Novecento sulla comprensione dei fenomeni scoperti ed accennati, andando ad indagare la nascita ed i primi sviluppi della teoria atomica con i modelli di atomo che via via furono proposti.
Debbo avvertire che le cose sono molto più complesse di come vengono qui raccontate. Per quanto uno si sforzi, nella realtà, non vi è mai un filone preciso ed una sequenza causale delle ricerche e dei successi. Spesso si seguono strade che non portano a nulla e non per questo sono meno utili. Siamo poi noi che per economia di pensiero ricostruiamo la storia non occupandoci di tutto ciò di cui dovremmo. Insomma non vi è linearità nella ricerca scientifica. Non vi è un successo dietro l’altro verso chissà quale traguardo. Vi sono filoni di ricerca che viaggiano paralleli che spesso, nella loro evoluzione, neppure si conoscono. Poi, all’improvviso, qualcuno si accorge che quel remoto risultato, all’apparenza del tutto insignificante, è una chiave esplicativa possente in altri ambiti. E chi, come me, tenta di raccontare questo lavora solo in una dimensione non riuscendo a rendere la complessità dell’insieme che è a molte dimensioni. Si perde molto in questa difficoltà che diventa enorme in un’epoca in cui fare scienza è diventata una professione e gli scienziati sono in grande quantità. Anche qui entrano in gioco i fattori produttivi, il fatto che la scienza viene scoperta come fattore possente di crescita produttiva e di dominio politico-economico. Se si vanno a sovrapporre scienziati e risultati scientifici con la geopolitica si scopre che al di fuori del potere economico e del dominio politico non vi è spazio per elaborazioni scientifiche se non altro perché la ricerca costa sempre di più e solo importanti finanziamenti possono garantire i successi agognati in ambiti applicativi.
GLI SPETTRI DI KIRCHHOFF
A partire del 1859, come abbiamo già discusso, Kirchhoff e Bunsen gettarono le basi della moderna spettroscopia, distinguendo con chiarezza la differenza esistente tra spettri di emissione e spettri di assorbimento: se sul becco si fa bruciare del sodio, lo spettro presenta due righe gialle che coincidono esattamente con le più brillanti delle linee oscure dello spettro del Sole (riga D); osservando poi lo spettro della luce solare lungo la cui traiettoria è interposto il becco con del sodio che brucia, non appare più la riga D nello spettro solare ed al suo posto vi sono le righe gialle del sodio; questo ultimo fenomeno si verifica solo quando la luce solare è molto attenuata, in caso contrario si continua a vedere la linea D; lo stesso fenomeno si può ottenere mantenendo costante l’intensità della luce solare e aumentando o diminuendo la temperatura della fiamma del becco. Da ciò Kirchhoff capì il significato dello spettro solare ed in particolare delle sue linee scure: la superficie del Sole emette radiazioni (fotosfera) di tutti i colori e l’atmosfera di gas incandescenti del Sole (cromosfera e corona), molto meno calda della fotosfera, assorbe una parte delle radiazioni emesse dal Sole, ed assorbe quelle che sono emesse dagli elementi componenti l’atmosfera solare. Come dice Kirchhoff: le fiamme colorate nei cui spettri si presentano linee brillanti e marcate [spettro di emissione: quello di figura è del sodio], indebolisce talmente i
raggi del colore di queste linee quando passano attraverso di esse, che in luogo delle linee brillanti compaiono linee scure [spettro di assorbimento: quello di figura è ancora del sodio con la riga gialla di emissione che diventa nera in

assorbimento quando si colloca dietro la fiamma una fonte di luce di sufficiente intensità e nel cui spettro mancano queste linee]. Concludo quindi che le linee scure dello spettro solare, che non sono prodotte dall’ atmosfera terrestre, nascono dalla presenza nella infuocata atmosfera del Sole, di quelle sostanze che nello spettro di una fiamma presentano le linee brillanti nella stessa posizione. Ed in questo modo Kirchhoff e Bunsen riuscirono a stabilire la presenza sul Sole di alcuni elementi: confrontando le righe che compongono lo spettro solare con quelle, ottenute in laboratorio, per elementi noti (all’esistenza di un dato insieme di righe nello spettro corrisponde sempre la presenza di un dato elemento).
Altro fondamentale risultato ottenuto da Kirchhoff nello stesso anno è il cosiddetto principio di inversione secondo il quale una sostanza assorbe le stesse radiazioni che è in grado di emettere.
Nel parlare di Kirchhoff, avevo riportato parte del contenuto di una sua memoria scritta con Bunsen. E’ utile rileggere ora quelle righe.
Nel 1860 Kirchhoff e Bunsen scrissero una memoria, Analisi chimiche mediante osservazioni spettroscopiche (Annalen der Physik, 110, pp. 161-189, 1860), in cui si indicava il modo di utilizzare la spettroscopia per fare analisi chimiche.
Leggiamo alcuni brani di tale memoria discorsiva::
È ben noto che molte sostanze, quando sono esposte alla fiamma, hanno la proprietà di produrre certe righe brillanti nello spettro. Possiamo fondare su queste righe un metodo di analisi qualitativa che allarga enormemente il campo delle reazioni chimiche e porta alla soluzione di problemi finora irrisolti. Ci limiteremo qui solo all’estensione del metodo alla rivelazione dei metalli degli alcali e delle terre alcaline e all’illustrazione del suo valore in una serie di esempi.
Le righe suddette appaiono più facilmente, quanto più alta è la temperatura e più debole il potere illuminante naturale della fiamma. La lampada a gas descritta da uno di noi fornisce una fiamma di temperatura molto alta e luminosità molto bassa; essa è quindi particolarmente adatta alle ricerche su quelle sostanze caratterizzate da righe brillanti. […]
Da queste ricerche accurate e complete, i cui dettagli possono essere omessi, si deduce che la differenza delle combinazioni in cui i metalli sono usati, la molteplicità dei processi chimici nelle diverse fiamme, e le loro enormi differenze di temperatura non esercitano alcuna influenza sulla posizione delle righe spettrali corrispondenti ai singoli metalli. […] Sembra indubbio quindi che le righe brillanti degli spettri indicati possano essere considerate prove sicure della presenza del metallo in questione. Esse possono servire come reazioni per mezzo delle quali questo materiale può essere rivelato con maggiore certezza, e più velocemente e in quantità più piccole che con qualsiasi altro metodo analitico. […]
Per coloro che hanno familiarità con i singoli spettri mediante osservazioni ripetute non è necessaria una misura accurata delle singole righe; il loro colore, la loro posizione relativa, la loro caratteristica definizione e sfumatura, la gradazione della loro brillantezza, sono criteri del tutto sufficienti per un sicuro riconoscimento anche per gli inesperti. […]
Le posizioni che [le linee] hanno nello spettro determinano una caratteristica chimica di natura altrettanto inalterabile e fondamentale del peso atomico della sostanza, e perciò ci consente di determinarla con esattezza quasi astronomica. Ciò che, tuttavia, dà al metodo analitico spettrale un’importanza particolare, è il fatto che essa supera di gran lunga i limiti raggiunti dall’analisi chimica della materia prima d’ora. Essa ci consente di trarre le conclusioni più valide sulla distribuzione e la sistemazione delle sostanze geologiche nella loro formazione. Già le poche ricerche, che questa memoria contiene, conducono alla conclusione inaspettata che non solo il potassio ed il sodio ma anche il litio e lo stronzio devono essere annoverati tra le sostanze terrestri più largamente diffuse, sebbene solo in piccole quantità. L’analisi spettrale giocherà anche una parte non meno importante nelle scoperte di elementi non ancora rivelati. Giacché se vi sono sostanze che siano così irregolarmente disseminate in natura che i metodi di analisi usati prima d’ora per separarle ed osservarle falliscano, possiamo sperare di rivelare e di determinare molte di esse, mediante il semplice esame dei loro spettri alla fiamma, che sfuggirebbe ai metodi ordinari di analisi chimica. Abbiamo già avuto l’opportunità di mostrare che esistono realmente tali elementi prima d’ora sconosciuti. Pensiamo di essere quindi in grado di dichiarare con assoluta certezza, confortati dai risultati indiscutibili dell’analisi spettrale, che oltre al potassio, al sodio ed al litio, vi è ancora un quarto metallo appartenente al gruppo degli alcali che darà uno spettro altrettanto caratteristico del litio – un metallo che mostra, col nostro apparato spettroscopico, solo due righe, una riga blu debole, che quasi coincide con la riga SI’ & dello stronzio ed un’altra riga blu, che giace solo un po’ oltre verso l’estremità violetta dello spettro, paragonabile in intensità e nettezza con la riga del litio.
Da un lato l’analisi spettrale offre, come crediamo di aver già dimostrato, un mezzo di meravigliosa semplicità per rivelare le più leggere tracce di certi elementi nelle sostanze terrestri, e dall’altro essa dischiude alla ricerca chimica un campo completamente chiuso prima d’ora, che si estende ben al di là dei limiti della Terra anche al nostro stesso sistema solare. Giacché, col metodo di analisi che stiamo discutendo, è sufficiente semplicemente vedere il gas in uno stato incandescente per poter fare l’analisi, ne segue subito che lo stesso è applicabile pure all’atmosfera del Sole e delle più brillanti stelle fisse. Occorre qui introdurre una modifica rispetto alla luce che il nucleo di questi corpi celesti irradia. In una memoria Sulla relazione tra l’emissione e l’assorbimento dei corpi per il calore e la luce uno di noi ha mostrato, per mezzo di considerazioni teoriche, chelo spettro di un gas incandescente è invertito, cioè che le righe brillanti sono trasformate in righe nere quando una sorgente di luce di intensità sufficiente, che dia uno spettro continuo, è posta dietro lo stesso. Da ciò possiamo concludere che lo spettro solare, con le sue righe nere, non è altro che l’inverso dello spettro che l’atmosfera del sole stessa mostrerebbe. Quindi l’analisi chimica dell’atmosfera solare richiede solo l’esame di quelle sostanze le quali, quando siano poste in una fiamma, producono righe brillanti che coincidono con le righe nere dello spettro solare.
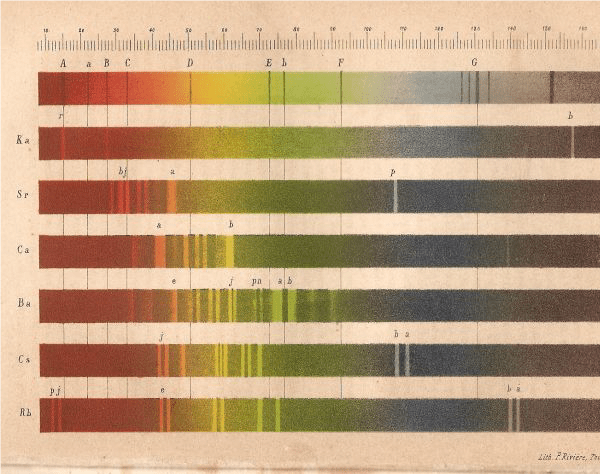
Nella figura, che compare nel lavoro di Kirchhoff e Bunsen Analisi chimiche mediante osservazioni spettroscopiche (Annalen der Physik, 110, pp. 161-189, 1860, Pl. II) sono rappresentati gli spettri di alcuni metalli alcalini confrontati con lo spettro solare e le sue linee oscure. Tratto da: Daguin, Traité elémentaire de Physique, Lagrave, Paris 1868, p 199.
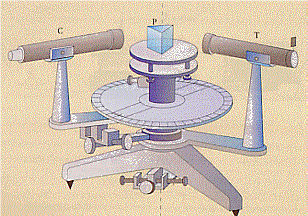
Per portare avanti le loro ricerche Kirchhoff e Bunsen si servirono di uno spettroscopio, strumento da loro realizzato e costruito da K. A. von Steinheil (famoso costruttore di strumenti ottici) nel 1853. Sulla destra della figura seguente vi è una fenditura regolabile in ampiezza da cui far passare la luce. La luce può essere quella di una lampada (luce bianca) o quella ottenuta con un becco Bunsen sul quale è sistemata una retina metallica sulla quale si mettono delle sostanze che si fanno bruciare per vederne gli spettri. Questa “luce” passa attraverso il collimatore T, va sul prisma P dove viene separata, quindi entra nel cannocchiale C (mobile su una ghiera graduata) ai cui estremi vi è un osservatore o una lastra fotografica (al posto di P, per avere immagini più sofisticate si possono sistemare dei reticoli di diffrazione).
Gli studi in questo campo portarono a stabilire senza ombra di dubbio che ciascun elemento aveva un suo spettro che differiva da tutti gli altri. Se si aveva un composto, lo spettro che veniva fuori era semplicemente la sovrapposizione degli spettri dei vari elementi che lo costituivano. Per questa via si scoprirono nuovi elementi poiché in dati composti comparivano serie di linee che non erano mai state osservate per nessun elemento. Esemplifico con gli spettri di due elementi, il primo dell’elio (elemento prima sconosciuto e che, appunto, fu trovato per via spettroscopica, analizzando lo spettro solare), il secondo del neon.


Ebbene, i dati osservativi stavano lì, avevano permesso importanti scoperte, ma non si riusciva a capire quale fosse l’origine degli spettri. Si provò a metterli dentro delle formule empiriche che rendessero conto della frequenza da assegnare ad ogni riga per differenti elementi. Nel 1885, il matematico e fisico svizzeroJohann Jakob Balmer (1825-1898) riuscì a elaborare una formula empirica(3) che rendeva conto della frequenza delle varie righe dello spettro dell’idrogeno (nel visibile):
ν = ν0 (1 – 4/m2)
dove ν0 è una costante ed m, che rappresenta il numero d’ordine della riga dello spettro, è un intero positivo che può valere: m = 3, 4, 5, ….
La formula di Balmer fu migliorata dal fisico svedese Johannes Rydberg(1854-1919) che estese la sua validità a tutti i metalli alcalini nel 1890, che la scrisse nella forma seguente(4):
ν = R(1/4 – 1/m2)
dove R è la costante di Rydberg che ha la proprietà di essere comune a tutte le serie di tutti gli elementi e che vale 109677,576cm-1 ed m è, come già detto, il numero d’ordine della riga dello spettro dell’idrogeno della quale si vuole misurare la frequenza (si osservi che, nel visibile, sperimentalmente m va da 1 a 6).
Dallo studio di questa formula si riuscirono a prevedere alcuni fatti:
1) devono esistere delle righe relative ad n = 7, 8, 9, ……, ∞ nella regione dell’ultravioletto (queste righe furono osservate subito dopo con uno spettroscopio opportuno);
2) devono esistere delle righe relative ad 1/12 (nella formula) situate nel lontano ultravioletto (queste linee furono osservate sempre con uno spettroscopio opportuno da Lyman nel 1906: serie di Lyman);
3) devono esistere altre righe relative a 1/32 (nella formula) nella regione dell’infrarosso (queste righe furono osservate da Paschen nel 1908);
4) devono esistere altre righe relative a 1/42, 1/52, … nella regione dl lontano infrarosso (queste righe furono osservate negli anni seguenti da diversi ricercatori, tra cui Brackett e Pfund).
La fenomenologia degli spettri, con una serie impressionante di studi che accompagnarono e seguirono quelli appena accennati, è quindi nota ma è un vero mistero la loro comprensione. Ci si deve adattare a formulette empiriche che dicono a priori dove uno può trovare una linea spettale. Una sorta di formulario da consultare all’occorrenza. E’ certo comunque che la struttura di un dato elemento è determinata dal suo spettro o viceversa.
LE PRIME SUGGESTIONI ATOMICHE IN AMBITO FISICO: KELVIN
Alcune suggestioni atomiche non corpuscolari risalivano ad una memoria di Kelvin del 1867. Egli era rimasto impressionato dallo studio dei vortici idrodinamici fatto da Helmholtz nel 1858 in una grande memoria (alla quale ne seguirà un’altra nel 1868)(5), vortici dei quali ricavò le equazioni differenziali,. Questo lavoro era stato tradotto da Peter Guthrie Tait e pubblicato in Gran Bretagna proprio nel 1867. In tale occasione Tait scrisse che quanto vi era nella memoria di Helmholtz si poteva perfettamente ricollegare con quanto William Thomson studiava da molto tempo. Inoltre anche Rankine aveva insistito sull’idea dei vortici molecolari e ne aveva trattato in un suo lavoro(6) del 1864. Questi vortici, in definitiva, suggerirono a W. Thomson una struttura della materia basata appunto su atomi vortice(7) con la doppia finalità di avere un modello idrodinamico alternativo rispetto a quello che avevano elaborato altri e di avere altri argomenti per negare il corpuscolarismo avanzante soprattutto in connessione con l’affermarsi della teoria cinetica dei gas. Sulle questioni corpuscolari vi fu una polemica, soprattutto nei riguardi di Clausius, molto aspra e rinfocolata dal collega ed amico di Thomson, Tait, ma in realtà l’argomento del contendere era il modo di fare fisica, o meglio, il modo di ragionare, di usare modelli di avere o meno un’idea meccanicista del mondo (Thomson). Mentre Thomson non voleva saperne di una struttura molecolare dettagliata, Clausius lavorava proprio nell’interpretazione microscopica di fenomeni macroscopici. E Thomson era indispettito perché altri iniziavano a muoversi nella direzione dell’interpretazione molecolare e cinetica della materia, come James Clerk Maxwell (1831 – 1879) e Ludwig Boltzmann (1844 – 1906), anche se il primo ebbe delle discussioni con Clausius sull’interpretazione molecolare (la disgregazione come misura della configurazione molecolare del corpo) del concetto di entropia.
Egli tentò così la strada di offrire un suo modello di materia, in chiara alternativa a quello di Clausìus, Maxwell e Boltzmann, che sarebbe potuto servire sia in elettromagnetismo che in termodinamica. A tal fine elaborò, appunto, la teoria dell’atomo vortice pensato in analogia all’idrodinamica che egli stesso aveva elaborato circa venti anni prima(8). Tra l’altro un merito va certamente assegnato a Thomson, quello di essere stato il primo a cimentarsi con un modello atomico. La sua memoria partiva dalla scoperta di Helmholtz della legge relativa al moto vorticoso, wirbelbewegung, in un fluido perfetto (assenza di viscosità) e dall’affermazione che gli anelli di Helmholtz siano i soli veri atomi (gli atomi vortice di Helmholtz era stati fatti conoscere ad Helmholtz da Tait che li aveva illustrati in una lezione mediante anelli di fumo nell’aria). E dice questo perché gli sembra l’unico modo per mantenere una trattazione mediante atomi e, nel contempo, esorcizzare la mostruosa assunzione di pezzi di materia infinitamente duri ed infinitamente rigidi, la cui esistenza viene affermata in termini di ipotesi verosimile da alcuni dei maggiori chimici moderni nelle loro sconsiderate proposizioni introduttive, che riesumano Lucrezio. Per Thomson i vortici di Helmholtz godevano proprio della proprietà che era richiesta agli atomi di Lucrezio, l’essere indistruttibili e quindi perenni. Allora, diceva subdolamente Thomson, coloro che erano o sono stati costretti a fare le loro belle ricerche con atomi alla Lucrezio (Bernouilli, Herapath, Joule, Krönig, Clausius, Maxwell), potrebbero ritrovare le stesse proprietà nei vortici anulari di Helmholtz. L’idea di fondo era che in un fluido ideale, come egli riteneva l’etere, dati alcuni vortici, essi sono sempre composti dalle stesse particelle, mantengono sempre la stessa struttura, possono intrecciarsi tra loro, proprio in analogia agli anelli di fumo. Vi era dietro questi ragionamenti quanto aveva già elaborato soprattutto in elettromagnetismo. Vi erano le linee di forza di Faraday che diventeranno tubi di forza in Maxwell, ma addirittura i punti atomi di Boscovich che già nel 1860 egli aveva pubblicamente esaltato in una conferenza alla Royal Institution, come gli unici enti in grado di superare la barbarie delle azioni a distanza del Settecento. In un etere inteso ancora come fluido perfetto l’idea di un vortice che si creasse nei tubi di forza era esteticamente molto affascinante come visione del campo.
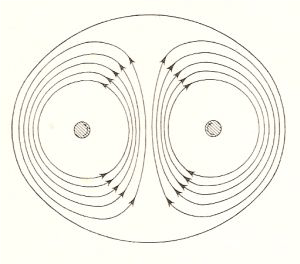
Il profilo convesso di un vortice doppio costituito da due vortici retti, paralleli, infinitamente lunghi e dotati di rotazioni uguali di senso opposto. In figura sono anche rappresentate le linee del moto del fluido trasportato dal vortice.
Come Thomson precisò ed elaborò in lavori successivi (1869 e 1876), quando volle dare una spiegazione dei legami chimici, i suoi atomi divennero piccoli anelli legati tra loro da nodi (studiati e disegnati da Tait), variando i quali variava il tipo di atomo e quindi il tipo di legame fino a spiegare addirittura le line spettrali.
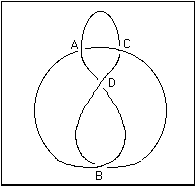
Un “atomo” di Thomson-Tait con una tra le tante disposizioni possibili di nodi ed anelli
Altra cosa però sono i vortici nei fluidi reali che svaniscono dopo un certo tempo e, poiché questo etere qualche proprietà materiale doveva averla, per spiegare alcune cose per cui era stato inventato, ecco che la teoria di Thomson risultò completamente falsificata. Fu il matematico francese Joseph Louis François Bertrand (1822 – 1900) che nel 1873 mostrò che la memoria di Helmholtz del 1858 conteneva degli errori(9) e che, da una parte spinse Maxwell ad indagare il problema e dall’altra affossò definitivamente l’atomo vortice. Ma Thomson non si perse d’animo e continuò a sostenere le sue idee, con articolate elaborazioni matematiche, fino a che non fu costretto ad ammetterne il fallimento che discendeva proprio da quella stabilità dei vortici che non ci poteva essere Fu comunque un lungo periodo di grande sofferenza per lui che si trovò anche costretto ad ammettere, sul finire della sua vita, che la strada dei modelli atomici sarebbe stata l’unica a portare dei risultati importanti alla spiegazione dei fenomeni naturali.
IL PRIMO MODELLO ATOMICO CORPUSCOLARE: HANTARO NAGAOKA
Hantaro Nagaoka (1865-1950) è stato un importante fisico giapponese che noi occidentalocentrici facciamo difficoltà a ricordare. Nagaoka si laureò in fisica all’Università di Tokio nel 1887. Per ottenere il master studiò ancora in Giappone spostandosi in Europa tra il 1892 ed il 1896 (Vienna, Berlino e Monaco) dove rimase profondamente colpito da Boltzmann e dai lavori di Maxwell. Tornato in Giappone insegnò fisica all’Università di Tokio dal 1901 al 1925 e, fatto notevole, tra i suoi alunni vi fu il famoso Hideki Yukawa (1907-1981), premio Nobel per la fisica nel 1949 per la sua teoria dei mesoni.
Nel dicembre del 1903 Nagaoka annunciò alla Physico-Mathematical Society di Tokyo una sua proposta di modello atomico che successivamente inviò alla Royal Society di Londra per la pubblicazione. Nel 1904 il Philosophical Magazine pubblicò il suo lavoro che era un primo tentativo di organizzare le conoscenze sperimentali e teoriche che si avevano per tentare di pensare in modo corpuscolare la struttura della materia(10). Egli partì dai fenomeni relativi agli spettri e da quanto veniva fuori dai fenomeni radioattivi ed organizzò il tutto in un modo che faceva aperto richiamo al modello degli anelli di Saturno studiati da Maxwell. Elaborò quindi un modello di atomo costituito da una grande massa centrale dotata di carica positiva intorno alla quale, come gli anelli di Saturno, ruotavano gli elettroni negativi.
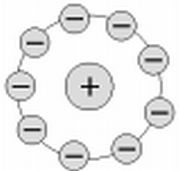
Modello saturniano di Nagaoka
Nagaoka partiva proprio da una discussione degli spettri che a suo giudizio devono descrivere un qualche sistema vibrante all’interno degli atomi costituenti la materia. Ricordava che vari fisici avevano tentato di accordare sistemi vibranti all’interno dell’atomo con le formule di Balmer e Rydberg ed altri. E notava che era stata indagata poco la differenza esistente tra lo spettro ordinario e quando si agisce sulla sostanza che lo emette con un campo magnetico. Quindi annunciava il suo programma:
Invece di cercare di trovare un sistema i cui modi di vibrazione vadano completamente d’accordo con la regolarità osservata nelle linee spettrali, visto che le formule empiriche sono ancora materia di discussione, propongo di discutere un sistema le cui piccole oscillazioni siano d’accordo qualitativamente con la regolarità osservata negli spettri di differenti elementi e con il quale siano facilmente spiegabili le influenze di un campo magnetico sulle linee spettrali medesime.
Nagaoka avvertiva che il suo sistema era il più semplice concepibile e quindi non in grado di spiegare le complessità delle proprietà chimiche soprattutto per la difficoltà di una trattazione matematica. Ed il sistema era il seguente:
Il sistema che io ho discusso consiste in un gran numero di particelle di massa uguale sistemate su di un cerchio alla medesima distanza angolare e che si respingono l’un l’altra con forze inversamente proporzionali al quadrato della distanza; al centro del cerchio è situata una particella di grande massa che attrae le altre particelle con la stessa legge di forze. Se queste particelle che si respingono rimangono a ruotare con quasi la medesima velocità intorno al centro che le attrae, il sistema resterà generalmente stabile, perché la forza che le attrae verso il centro è sufficientemente intensa rispetto a dei piccoli disturbi. Il sistema differisce da quello saturniano ideato da Maxwell nell’avere particelle che si respingono in luogo di satelliti che si attraggono. Quanto sostengo ora è approssimativamente realizzato rimpiazzando questi satelliti da elettroni negativi ed il centro attrattivo con una particella carica positivamente
e questo sistema può ben rappresentare un atomo come hanno mostrato le esperienze sui raggi catodici e quelle sulla radioattività.
Lo stesso Nagaoka proseguiva con l’evidente difficoltà di tale sistema affermando che essa consiste nel problema dell’energia radiante Per capire questo punto occorre risalire ai lavori elettromagnetici di Lorentz, alla sua teoria degli elettroni ed in particolare ai suoi lavori del 1895. Vediamolo in modo semplice.
Per capire perché un elettrone in un atomo debba irradiare energia elettromagnetica (e quindi perdere energia e quindi implodere), cominciamo con il ricordare alcuni concetti di elettricità e magnetismo.
Una corrente elettrica è un flusso di cariche elettriche in moto. A questo flusso di cariche elettriche lungo un filo è associato un campo magnetico con le linee di forza circolari e concentriche al filo stesso:
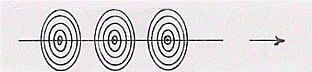
Il campo magnetico B è tangente punto per punto a queste linee di forza con verso dato dalla regola di Maxwell o del cavatappi (il verso è quello di rotazione del cavatappi che avanza nel senso della corrente):
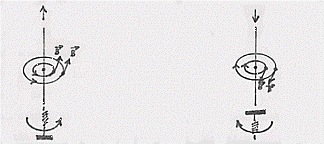
Supponiamo ora di avere una singola carica q in moto (e l’elettrone è una carica). E’ spontaneo assumere che questa carica costituisca una piccolissima corrente elettrica lungo la linea su cui avanza la carica:

Sappiamo già che una carica elettrica ferma ha intorno a sé un campo elettrico E radiale (le linee di forza possono essere interpretate come i prolungamenti dei raggi della sferetta che ci rappresenta la carica):
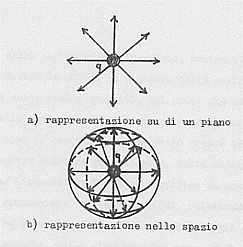
Se questa carica si muove, poiché origina una piccolissima corrente elettrica, al campo elettrico si aggiungerà un campo magnetico le cui linee di forza saranno circonferenze concentriche alla linea del moto.
Questo campo magnetico risulterà essere trasversale (il vettore campo magnetico B è in ogni punto perpendicolare al vettore campo elettrico E); esso sarà nullo sulla linea del moto ed avrà il suo massimo sul piano perpendicolare a questa linea e passante per la carica.
I due campi, elettrico e magnetico, risultano così strettamente legati originando il cosiddetto campo elettromagnetico.
Consideriamo ora una carica elettrica che si muove di moto rettilineo uniforme. Questa particella, nel suo moto, trasporta con sé il campo elettromagnetico e l’energia che compete a questo campo. Supponiamo ora che la carica si sposti nel verso indicato in figura con velocità costante v:
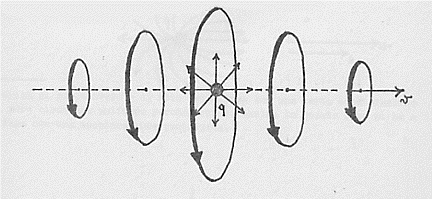
Il campo elettrico della carica rimane invariato, mentre il campo magnetico: nei punti che sono dietro la carica (a sinistra della carica in figura) decresce gradualmente della stessa quantità, nei punti che sono davanti alla carica (a destra della carica in figura) cresce gradualmente della stessa quantità. In definitiva il campo elettromagnetico cresce gradualmente a destra della carica mentre decresce gradualmente, della stessa quantità a sinistra della carica. L’aumento di un campo significa un aumento dell’energia e viceversa per la diminuzione del campo, quindi, relativamente alla nostra carica in moto, si ha un continuo trasferimento di energia da sinistra verso destra o, più precisamente, nella direzione del moto. Si ha così un continuo flusso di energia nel verso del moto della carica.
Se si fanno i conti si vede che, data la simmetria dei campi elettrico e magnetico, non si ha irraggiamento di energia verso l’esterno, ma solo un trasferimento dell’energia nel verso del moto della carica. Ciò è comprensibile se si tiene conto che la carica vede intorno a sé, istante per istante, sempre lo stesso campo e quindi ha sempre una energia costante. Se questa energia è costante per la carica lo deve essere anche per un ipotetico osservatore.
In conclusione: una carica elettrica che si muove di moto rettilineo uniforme non irradia energia elettromagnetica verso l’esterno.
Consideriamo ora una carica che si muova di moto accelerato. Il campo elettrico di questa carica non è più radiale ma risulta dissimetrico con un addensamento delle linee di forza dalla parte verso cui si muove la carica:
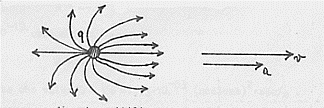
Quando questa carica si muove non si avrà più la situazione vista precedentemente (aumento di campo a destra uguale alla diminuzione di campo a sinistra); ora il campo a destra crescerà di più di quanto diminuisca il campo a sinistra proprio a causa della accelerazione della carica e della conseguente dissimetria destra-sinistra del campo stesso. A questo aumento di campo corrisponde, come già sappiamo, un aumento di energia ed il bilancio destra-sinistra della carica in moto è tale per cui c’è un eccesso di energia risultante nella direzione del moto. Questo eccesso di energia originato a spese della carica che crea il campo si trasferirà in tutto lo spazio circostante sotto forma di radiazione elettromagnetica.
In conclusione: una carica elettrica che si muove.di moto accelerato irradia energia elettromagnetica verso l’esterno nello spazio circostante.
Se la carica q in considerazione si muove di moto accelerato (con accelerazione a) nel vuoto (e con buona approssimazione nell’aria), l’energia al secondo, W, che essa irradia (nel sistema MKSA) è data da (come ha ricavato il fisico nordirlandese Joseph Larmor nel 1897)(11):
W = K . q2.a2
dove K è una costante che vale: K = 0,44.10-15 s/m, q è la carica elettrica, a è l’accelerazione che compete alla carica(12).
In definitiva gli elettroni che considerava Nagaoka si trovavano a ruotare intorno ad un nucleo centrale ed anche se la velocità era costante, in un moto circolare occorre sempre tener conto dell’accelerazione centripeta. In queste condizioni gli elettroni dovevano emettere energia radiante verso l’esterno dell’atomo, quindi perdere energia ed in definitiva precipitare sul centro di rotazione facendo di fatto implodere l’intero atomo. Era a ciò che faceva riferimento Nagaoka ed egli stesso presentava ciò come una difficoltà grave della sua teoria.
Sullo stesso numero del Philosophical Magazine nel quale era apparso l’articolo di Nagaoka vi era un altro articolo sull’argomento, quello di J.J. Thomson(13).
IL MODELLO ATOMICO DI KELVIN E J. J. THOMSON
Già nel 1899, J. J. Thomson stava elaborando idee sulla struttura della materia che rendessero conto dei fenomeni fisici osservati(14). Egli si era convinto che all’interno di un atomo doveva, in qualche modo, esservi della carica positiva. La presenza degli elettroni negativi nella materia doveva prevedere la presenza di un qualcosa di positivo che andasse a neutralizzare la carica di segno opposto. Egli scriveva: Benché gli elettroni si comportino individualmente come ioni negativi, quando sono incorporati in un atomo neutro, il loro effetto è controbilanciato da un qualcosa che fa in modo che lo spazio in cui queste particelle sono distribuite si comporti come se avesse una carica positiva uguale alla somma delle cariche negative di queste particelle. Ma su questa supposta carica positiva non si sapeva nulla. Fu Kelvin che nel 1901 suggerì che la carica positiva dovesse essere assegnata ad una massa omogenea e continua, da pensarsi come ordinariamente sono pensati i fluidi (una specie di massa gelatinosa a bassissima densità)(15). Kelvin iniziava con il ricordare la teoria fluidistica dell’elettricità ad un solo fluido di Epino, secondo la quale le elettrizzazioni positive e negative consistono di eccessi e di deficienze rispetto ad un quantum naturale di un fluido, detto fluido elettrico, il quale permea tutto lo spazio compreso tra gli atomi della materia ponderabile. Porzioni di materia prive di fluido elettrico si respingono reciprocamente; porzioni di fluido elettrico si respingono reciprocamente; porzioni di fluido elettrico e di materia priva di fluido si attraggono reciprocamente. Quindi proseguiva con quanto egli pensava, scrivendo:
Il mio suggerimento è questo: che il fluido di Epino consista di atomi identici e straordinariamente piccoli che io chiamo ‘elettrioni’ e che sono molto più piccoli degli atomi della materia ponderabile; essi viaggiano liberamente attraverso gli spazi occupati da questi atomi di dimensioni maggiori, così come liberamente viaggiano nello spazio non occupato da questi atomi.
Ed in definitiva, come meglio spiegherà oltre, egli immaginava un fluido omogeneo dentro cui sono situati gli elettroni che in una determinata porzione di tale fluido si fanno equilibrio elettrico. Ciò vuol dire che il fluido ha carica opposta agli elettrioni che vi sono dentro. La carica posseduta da elettrioni e fluido è, per Kelvin, convenzionale ed egli assume come negativa (che egli chiama resinosa) quella dell’elettrione e positiva (che egli chiama vetrosa) quella del fluido. Con queste premesse egli affermava le cose seguenti:
Farò quindi l’ipotesi che i nostri elettrioni agiscano come particelle estremamente piccole di materia elettrizzata resinosamente; che un atomo vuoto agisca semplicemente come un piccolo globo di sostanza atomica, il quale possiede, alla stregua di una qualità essenziale, un’elettricità vetrosa uniformemente distribuita al proprio interno, o entro un globo concentrico più piccolo; e che l’ordinaria materia ponderabile, non elettrizzata, consista di un grande insieme di atomi, non vuoti ma tali da contenere, entro le porzioni di spazio che essi occupano, proprio quel numero di elettrioni che è sufficiente per annullare la forza elettrica in tutte quelle zone la cui distanza dall’atomo più vicino è grande in confronto al diametro di un atomo, o di un gruppo molecolare di atomi.
A questo punto il problema principale che si pone Kelvin è quello del come sono sistemati questi elettrioni all’interno del globo uniformemente positivo. E la discussione è lunga perché riguarda non solo gli atomi isolati dei gas dei quali occorre indagare l’equilibrio stabile degli elettrioni in essi ma anche quelli di sostanze solide poiché si deve rendere conto di come si sistemano i globi tra loro ad evitare che inizino repulsioni tra gli elettrioni contenuti in essi. In modo estremamente meticoloso Kelvin si calcolava le situazioni più stabili per un numero diverso di elettrioni in un dato globo. Disponendo di due elettrioni essi sono sistemati agli estremi di un diametro; tre agli estremi di un triangolo equilatero; quattro ai vertici di un quadrato o di un tetraedro equilatero; …. E, quando il numero degli elettrioni supera il quattro, dobbiamo pensare alla tendenza ad un affollamento esterno ad una superficie sferica.
Queste elaborazioni eminentemente teoriche furono riprese da J.J. Thomson in alcune conferenze (le Silliman Lectures) che tenne nell’Università di Yale (USA) nel 1903(16). Facendo anche riferimento ad alcuni esperimenti del fisico americano Alfred M. Mayer (1836-1897) del 1878 scriveva in proposito J.J. Thomson:
[…] è necessario considerare più attentamente il modo in cui i corpuscoli [gli elettroni] si dispongono nell’atomo. Cominceremo col caso in cui i corpuscoli sono a riposo. Si suppone che i corpuscoli si trovino in una sfera di elettrificazione positiva che produce una forza attrattiva radiale su ogni corpuscolo proporzionale alla sua distanza dal centro della sfera, e il problema è di disporre i corpuscoli nella sfera in modo che essi siano in equilibrio sotto l’azione di questa attrazione e delle loro mutue repulsioni. Se vi sono solo due corpuscoli, A B, si può vedere subito che essi saranno in equilibrio se disposti in modo che A B e il centro della sfera siano sulla stessa linea retta e OA = OB = ½ del raggio della sfera.
Ed anche Thomson percorre tutta la casistica che era stata fatta da Kelvin arricchendo il tutto con figure:
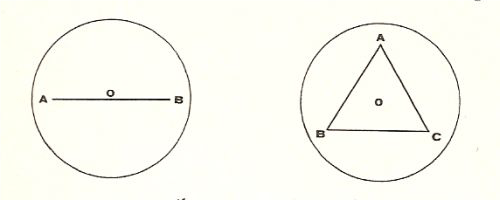
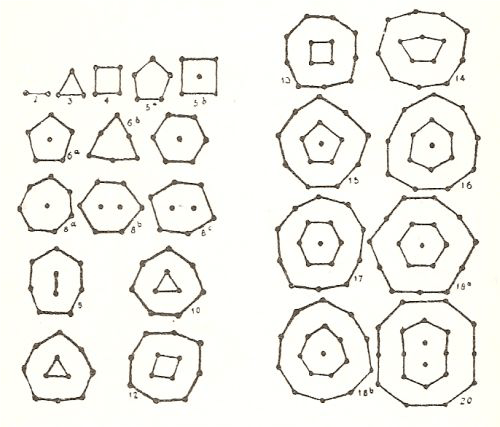
Da Am. Journ. Sci., 116, 248-249, 1878
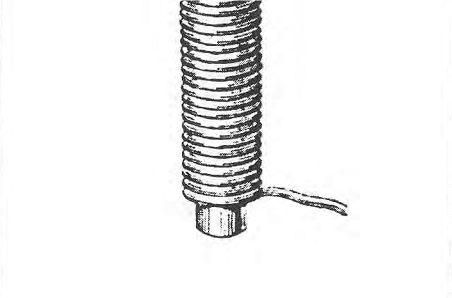
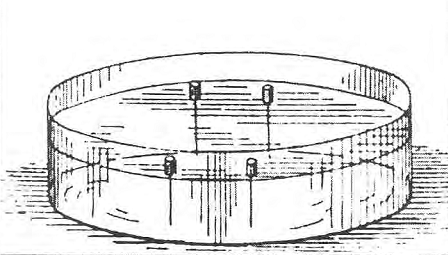
Da notare che le configurazioni elettroniche fornite fa J.J. Thomson gli furono suggerite, come egli stesso afferma, anche da alcuni semplici esperimenti che aveva realizzato il citato fisico americano Mayer utilizzando dei piccoli magneti galleggianti in una bacinella(17):
In questo esperimento un. certo numero di piccoli magneti si fanno galleggiare in un catino d’acqua. I magneti sono aghi di acciaio magnetizzato di ugual forza e si fanno galleggiare essendo infilati in piccoli dischi di sughero. I magneti sono posti in modo che i poli positivi siano o tutti sopra o tutti sotto la superficie dell’acqua. Questi positivi come i corpuscoli, si respingono tra loro con forze che variano inversamente con la distanza tra di essi. La forza attrattiva è fornita da un polo negativo (se i piccoli magneti hanno i poli positivi al di sopra dell’acqua) sospeso ad una certa distanza sopra la superficie dell’acqua. Questo polo eserciterà sui poli positivi dei piccoli magneti galleggianti una forza attrattiva la cui componente, parallela alla superficie dell’acqua, sarà radiale, diretta verso O, la proiezione del polo negativo sulla superficie dell’acqua, e se il polo negativo e ad una qualche distanza sulla superficie la componente della forza verso O sarà approssimativamente proporzionale alla distanza da O. Quindi le forze sui poli dei magneti galleggianti saranno molto simili a quelle che agiscono sui corpuscoli del nostro ipotetico atomo; la maggiore differenza è che i corpuscoli sono liberi di muoversi in tutte le direzioni dello spazio mentre i poli dei magneti galleggianti sono vincolati a muoversi in un piano parallelo alla superficie dell’acqua.
Le configurazioni che i magneti galleggianti assumono al crescere del numero dei magneti da due a diciannove è mostrato nella figura [ultima riportata], che fu data da Mayer. […]
Dopo questa illustrazione della disposizione elettronica, J.J. Thomson passava ad illustrare le proprietà degli atomi che egli immaginava.
Veniamo ora alle proprietà del modello atomico. Esso contiene un numero molto grande di corpuscoli in rapido movimento. Abbiamo evidenza dai fenomeni connessi con la conduzione dell’elettricità nei gas che uno o più di questi corpuscoli possono venire staccati dall’atomo. Questi possono sfuggire a causa della loro alta velocità che consente loro di superare l’attrazione dell’atomo. Essi possono venire staccati anche per la collisione dell’atomo con altri atomi o corpuscoli liberi muoventisi velocemente. Una volta che un corpuscolo è sfuggito da un atomo questo avrà una carica positiva. Ciò renderà più difficile per un secondo corpuscolo elettrizzato negativamente sfuggire, perché in conseguenza della carica positiva sull’atomo esso attrarrà il secondo corpuscolo maggiormente del primo. Ora possiamo pensare facilmente che la facilità con cui una particella sfuggirà da un atomo, o ne verrà espulsa, possa variare molto negli atomi di elementi diversi. In alcuni atomi le velocità dei corpuscoli possono essere così grandi che un corpuscolo sfugge subito dall’atomo. Può anche accadere che dopo che uno è sfuggito, l’attrazione dell’elettrizzazione positiva residua nell’atomo non sia sufficiente ad impedire ad un secondo corpuscolo, od anche a un terzo di sfuggire. Tali atomi acquisterebbero cariche positive di una, due, o tre unità, a seconda che abbiano perso uno, due, o tre corpuscoli. D’altra parte, possono esservi atomi in cui le velocità dei corpuscoli sono così piccole che pochi corpuscoli, o anche nessuno di essi, riescono a sfuggire, o piuttosto, essi possono anche essere in grado di ricevere uno o anche più di un corpuscolo prima che la repulsione esercitata dall’elettrizzazione negativa su questi corpuscoli estranei espella qualcuno dei corpuscoli originari. Atomi di questo tipo posti in una regione in cui siano presenti corpuscoli acquisterebbero una carica negativa per aggregazione con questi corpuscoli. L’entità della carica negativa dipenderebbe dalla forza con cui l’atomo tiene i suoi corpuscoli. Se una carica negativa di un corpuscolo non fosse sufficiente ad espellere un corpuscolo mentre la carica negativa di due corpuscoli potrebbero farlo, la carica negativa massima sull’atomo sarebbe di un’unità. Se due corpuscoli non fossero sufficienti ad espellere un corpuscolo, ma tre lo fossero, la carica negativa massima sarebbe di due unità, e così via. Così, gli atomi di questa classe tendono a divenire carichi di elettricità negativa e corrispondono agli elementi chimici elettro-negativi, mentre gli atomi della classe considerata prima, i quali perdono facilmente corpuscoli, acquistano una carica positiva e corrispondono agli atomi degli elementi elettro-positivi. Potremmo concepire atomi in cui l’equilibrio dei corpuscoli fosse così esattamente bilanciato che benché essi non perdano da soli un corpuscolo, e quindi non acquistino una carica positiva, la repulsione esercitata da un corpuscolo estraneo che giunga all’atomo fosse sufficiente ad espellere un corpuscolo. Un tale atomo sarebbe incapace di ricevere una carica di elettricità sia positiva che negativa.
Si può a questo punto osservare che i lavori di J.J. Thomson seguivano ed in qualche modo perfezionavano quelli del suo più anziano collega, Kelvin. Con la differenza che quest’ultimo non gradiva sentir parlare di corpuscoli.
Finalmente nel 1904, J. J. Thomson pubblicò una memoria nella quale mise insieme le sue idee sull’argomento proponendo un modello atomico definito(13). Dopo molte pagine di conti per mostrare la stabilità di un tale modello atomico, J. J. Thomson passava a descrivere un modello in cui n particelle elettrizzate negativamente sono situate dentro una sfera uniformemente elettrizzata. Egli supponeva che gli n elettroni, ciascuno con carica e, erano sistemati ad intervalli angolari uguali sul bordo di una circonferenza di raggio a. Supponiamo che la carica positiva sia νe e che b [con a < b] sia il raggio della sfera in cui si trova tale carica, l’attrazione radiale di un elettrone dovuta alla carica
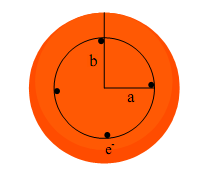
positiva sarà ne2a/b2; quando gli elettroni sono immobili, tale attrazione dovrà essere bilanciata dalla repulsione che si esercita tra elettroni. E qui Thomson iniziava tutta una serie di conti studiando la situazione di vari elettroni nelle diverse posizioni che aveva indicato nel lavoro precedente che si riferiva alle esperienze di Mayer. Alla fine della discussione di tutti i casi che riteneva utili discutere, continuava:
Noi supponiamo che l’atomo sia costituito da un numero di corpuscoli che si muovono in una sfera elettrizzata positivamente in modo uniforme: i problemi che dobbiamo risolvere sono: (1) quale deve essere la struttura di tale atomo, ad esempio come devono essere sistemati i corpuscoli nella sfera; e (2) quali proprietà una tale struttura dovrebbe assegnare a tale atomo. La soluzione di (1), quando i corpuscoli sono costretti a muoversi in un piano, ci viene indicata dai risultati che abbiamo appena ottenuto: i corpuscoli si sistemeranno in una serie di anelli concentrici. Questa sistemazione è obbligata dal fatto che un gran numero di corpuscoli(18) non può trovarsi in equilibrio stabile quando si trova su un solo anello, mentre questo anello può essere reso stabile sistemando dentro di esso un appropriato numero di corpuscoli. Quando invece i corpuscoli non sono costretti in un piano ma possono muoversi nella sfera in tutte le direzioni, essi si sistemeranno in una serie di gusci concentrici; per cui possiamo facilmente osservare che, come nel caso dell’anello, un numero di corpuscoli distribuiti sulla superficie di un guscio non sarà in equilibrio stabile se il numero dei corpuscoli è grande a meno che non vi siano altri corpuscoli all’interno del guscio, mentre l’equilibrio può essere reso stabile introducendo nel guscio un appropriato numero di altri corpuscoli.
Tutto ciò portava al risultato
secondo il quale un numero elevato di corpuscoli che ruotano rapidamente, si distribuiscono nelle seguenti configurazioni. I corpuscoli formano una serie di anelli: i corpuscoli di ciascun anello giacciono in un piano posto perpendicolarmente all’asse di rotazione e il loro numero diminuisce al diminuire del raggio dell’anello. Se i corpuscoli si possono muovere perpendicolarmente al piano dell’orbita, gli anelli saranno disposti in piani diversi, in modo tale che la repulsione tra gli anelli sia bilanciata dall’ attrazione esercitata dalla sfera positiva nella quale sono immersi. Si ha così, per prima cosa, una sfera uniforme di carica positiva, e, all’interno di questa, un certo numero di corpuscoli distribuiti in una serie di anelli paralleli, dove il numero dei corpuscoli presenti in ciascun anello varia da un anello all’altro; ogni corpuscolo viaggia a velocità elevata lungo la circonferenza in cui è situato e gli anelli sono disposti in modo tale che quelli che contengono un numero elevato di corpuscoli sono vicini alla superficie della sfera, mentre quelli che ne contengono un numero minore sono più interni.
A questo punto Thomson ammetteva che le difficoltà sono grandi e che egli non era capace di risolverle in modo generale e completo. Il problema diventava a molti corpi perché la cercata condizione di equilibrio dei vari elettroni dipendeva dalla repulsione su un elettrone degli altri n – 1. Si doveva poi considerare che gli anelli (o i gusci) potevano ruotare con una data velocità angolare ω e questa eventualità modificava le condizioni di equilibrio facendole dipendere da un valore determinato della velocità angolare. Questa condizione era evidente per quanto si sapeva sull’emissione di radiazione da parte di cariche elettriche in moto e Thomson aveva fatto un’ipotesi ad hoc: per valori di ω grandi, scendendo fino ad un dato valore critico, non vi era emissione di radiazione. Scriveva Thomson:
Il nostro studio della stabilità dei sistemi di corpuscoli ci ha fatto conoscere sistemi che sono stabili quando i corpuscoli ruotano con una velocità angolare maggiore di un certo valore, ma che divengono instabili quando la velocità cade al di sotto di questo valore […] Consideriamo ora le proprietà di un atomo contenente un sistema di corpuscoli … [inizialmente] in moto con velocità eccedenti di molto la velocità critica; in conseguenza dell’irraggiamento dei corpuscoli in moto, le loro velocità diminuiranno lentamente – molto lentamente; quando, dopo un lungo intervallo, la velocità raggiunge la velocità critica, avverrà qualcosa di equivalente a una esplosione dei corpuscoli, i corpuscoli si allontaneranno assai dalle loro posizioni iniziali, la loro energia potenziale diminuirà, mentre la loro energia cinetica aumenterà. L’energia cinetica acquistata in questo modo potrebbe esser sufficiente a trascinare il sistema fuori dell’atomo, e avremmo, come nel caso del radio, l’espulsione violenta di una parte dell’atomo. In conseguenza della lentissima dissipazione di energia per irraggiamento la vita dell’atomo sarebbe lunghissima.
Thomson ammette quindi che gli elettroni irradino nel loro moto ma lo farebbero molto lentamente, tanto da garantire la stabilità dell’atomo. Ma l’irradiazione è una perdita d’energia e quindi gli elettroni la perdono attraverso la perdita di velocità dell’anello (o guscio) in cui si trovano. Quando si arriva però al valore critico di questa velocità, nell’atomo si verifica una sorta di esplosione: i corpuscoli acquistavano energia cinetica sufficiente per essere scagliati al di fuori dell’atomo stesso. Ed in questo modo con il suo modello, il nostro tentava pure di avviare una spiegazione dei fenomeni radioattivi.
Ma, tornando al modello di atomo, nonostante le difficoltà annunciate, Thomson forniva un set di n equazioni le cui soluzioni avrebbero permesso di valutare la stabilità degli anelli attraverso la frequenza q di vibrazione (rispetto alla loro posizioni di equilibrio) delle singole cariche nell’anello medesimo:
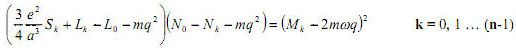
(dove S, L, M, ed N sono quantità che Thomson si era calcolato precedentemente ed ω è la velocità angolare dell’anello). Ora le radici di queste equazioni devono essere reali per fornirci le soluzioni delle frequenze di oscillazione. Dopo una serie laboriosa di calcoli, Thomson mostrò che tutte le radici di queste equazioni sono certamente reali per n < 6, mentre per altri valori di n occorre fare una serie molto complessa di operazioni per capire come stanno le cose, anche mettendo in relazione tali risultati con la frequenza ω d’oscillazione dell’anello. In particolare per n = 6 e k = 3, l’equazione precedente diventa:
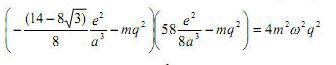
ed una delle radici di q2 risulta immaginaria.
Questi conti gli servivano per interpretare la periodicità della tavola periodica ed infatti egli poteva a questo punto affermare:
Possiamo pertanto dividere i vari gruppi di atomi in serie, ciascun membro di una serie essendo derivato dal membro precedente (cioè dal membro di peso atomico immediatamente inferiore) con l’aggiunta di un ulteriore anello di elettroni. Ci dovremmo aspettare che gli atomi appartenenti a una tale serie presentino molte caratteristiche simili
e, poiché aveva individuato delle regolarità nel confrontare la tavola periodica con il numero degli elettroni in anelli, commentava:
Possiamo … dividere i vari gruppi di atomi in serie, ciascun membro di una serie essendo derivato dal membro precedente (cioè dal membro di peso atomico immediatamente inferiore) con l’aggiunta di un ulteriore anello di elettroni … Quando l’atomo del membro p-mo è derivato dall’atomo del membro (p – 1)-mo per l’aggiunta di un singolo anello di corpuscoli, questi atomi appartengono entrambi a elementi che si trovano nell’ordinamento degli elementi secondo la legge periodica nello stesso gruppo, ossia formano una serie, che, se ordinata secondo la tavola di Mendeleev(19), dovrebbe trovarsi tutta sulla stessa colonna verticale
In definitiva, per Thomson, un atomo deve essere pensato come un continuo sferico di carica positiva dentro cui si trovano queste piccole masse che sono gli elettroni. Riguardo poi a come sono distribuiti gli elettroni nella gelatina positiva, dipende dal loro numero: se l’atomo ha un solo elettrone questo si dispone al centro della sfera; se gli elettroni sono più di uno, probabilmente, si disporranno in superfici sferiche concentriche con la sfera ed interne ad essa. Questi elettroni saranno, inoltre dotati di moto rotatorio intorno al centro della sfera ma, come accennato, con alcune limitazioni alla velocità angolare degli anelli su cui sono situati.
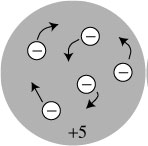
Il modello di Thomson chiamato Plum-Pudding nel caso di 5 elettroni. La parte grigia è carica di elettricità positiva equivalente a quella dei 5 elettroni.
Una osservazione è a questo punto utile. Il fatto che Thomson sia riuscito a legare la tavola periodica con la distribuzione degli elettroni nell’atomo, pur essendo il risultato abbastanza fortuito e raggiunto a partire da premesse errate, dette credibilità e sostegno al suo modello di atomo. Restava vaga e non supportata da nulla la spiegazione della radioattività e non vi erano che brevissimi cenni alla massa che un tale atomo avrebbe dovuto possedere (egli dice che la massa di un atomo è la somma delle masse dei corpuscoli che contiene). E siamo qui ancora ai grandi numero di elettroni costituenti un atomo. Ad esempio, in questa epoca, un atomo di idrogeno avrebbe dovuto avere circa 2000 elettroni. Questo modello di atomo, era comunque non incompatibile con i dati sperimentali (pochi) che allora si avevano. Spiegava molte cose almeno da un punto di vista qualitativo e, come osserva Tagliaferri, avrebbe potuto tentare la stessa operazione relativamente alle differenze registrate sperimentalmente nell’assorbimento dei raggi α e β. Tali differenze erano state fatte notare a Thomson in una lettera di W. H. Bragg dell’agosto 1904 (citata da Tagliaferri):
Ci sono […] notevoli differenze nei fenomeni di assorbimento dei raggi α e β, sebbene in molti aspetti i due tipi di raggi si assomiglino. La differenza essenziale è, senza dubbio, che i raggi α sono atomi e i β elettroni: ma, andando un passo oltre, la causa più diretta della dissimilarità negli effetti di assorbimento è che i raggi β sono soggetti a deflessioni nelle collisioni (o scontri), e i raggi α no […]. Sembra ragionevole supporre che siccome un elettrone singolo può penetrare centinaia di migliaia di atomi con scarso rischio di seria deflessione, allora un atomo considerato meramente come un insieme di elettroni deve anch’esso possedere un grande potere penetrante: inoltre, lo scontro accidentale di uno dei suoi elettroni con un elettrone dell’atomo attraversato può essere una faccenda seria per ciascuno degli elettroni, ma può avere un piccolissimo effetto sul movimento dell’atomo. Dal che segue che la penetrazione delle particelle α deve essere proporzionale alla densità della materia attraversata, che [questa] radiazione deve essere assolutamente rettilinea […] e che non ci devono essere particelle α diffuse, come nel caso della radiazione β […]. Quindi i raggi α sono assorbiti, vale a dire le particelle α sono fermate, semplicemente consumando la loro energia in ionizzazione. Se esse hanno tutte in partenza la stessa velocità, devono percorrere tutte esattamente la stessa distanza.
Ponendo attenzione a ciò che accade più in generale nel mondo della fisica, a questo punto siamo vicini al 1905, un anno fondamentale negli sviluppi della fisica. In questo anno Einstein ha utilizzato i quanti che Planck ha introdotto alla fine dell’anno 1900. Il fatto è di notevole importanza perché quei quanti di Planck sembravano, anche nel giudizio di Planck, un artificio matematico per risolvere il problema del corpo nero. Einstein mostrava invece che essi permettevano di spiegare fenomeni rimasti incompresi, come l’effetto fotoelettrico. Quindi i quanti iniziano ad essere presi in considerazione come strumento in grado di entrare nella spiegazione fisica. Einstein ha anche fornito una fondamentale sistemazione dell’elettromagnetismo in un articolo che banalmente è noto come relatività. Per ora la relatività ed i quanti restano lontani dall’atomo ma ben presto si dimostreranno indispensabili per comprendere quasi tutti i meccanismi che abbiamo introdotto. Basti solo dire che l’ipotesi di Abraham (1903) di atomo elettromagnetico e rigido sarà falsificata completamente proprio dalla contrazione relativistica.
Intanto, nel 1906, J.J. Thomson tornò a discutere della struttura dell’atomo con una memoria in cui studiava il numero di corpuscoli in un atomo(20). Egli prendeva le mosse da alcuni fatti sperimentali come la dispersione della luce e lo scattering e l’assorbimento dei raggi X da parte dei gas. Dopo aver affermato che ognuno dei tre metodi usati dava pochi dati affidabili e che la correttezza della conclusione discendeva dal fatto che tutti e tre i metodi davano risultati molto simili, egli stabiliva che il numero dei corpuscoli non è molto differente dal peso atomico e che il rapporto tra il numero dei corpuscoli nell’atomo ed il peso atomico dell’elemento è lo stesso per tutti gli elementi. E ciò vuol dire che gli elettroni contribuiscono solo per una piccolissima frazione alla massa di un atomo e di conseguenza che la massa posseduta dall’unità di carica positiva è grande rispetto a quella posseduta dall’unità di carica negativa. Sappiamo che questa conclusione è corretta ma essa non è conciliabile con la precedente idea di J.J. Thomson della struttura dell’atomo e della carica positiva diffusa.
NOTE
(1) La storia della teoria atomistica dall’antichità fino alla fisica del Novecento la si può trovare in Atomi e Molecole.
(2) I corpuscoli negativi che aveva scoperto Thomson erano quelli che da allora vennero chiamati elettroni. Il termine elettrone (dal termine greco ήλεκτρον che vuol dire ambra, il primo materiale noto ad avere proprietà elettriche)non è stato però coniato da Thomson ma dal fisico irlandese Johnstone George Stoney che utilizzò il temine, per denotare l’unità elementare di carica elettrica in elettrochimica, nella relazione On the Physical Units of Nature che tenne al Convegno della British Association tenuto a Belfast nel 1874. Una delle leggi di Faraday dell’elettrolisi (1833) sosteneva: perché ad un elettrodo si liberi un grammo-atomo di un elemento di valenza z, facente parte del composto in questione, la soluzione elettrolitica deve essere attraversata da una quantità di elettricità data da z volte 96.522 coulomb. Era il primo tangibile indizio della natura discontinua dell’elettricità, dell’esistenza dell’elettrone. Se ciascun atomo di materia, nel passare attraverso la soluzione elettrolitica, porta con sé una quantità di carica definita e ben determinata, allora la quantità di materia depositata su di un elettrodo sarà direttamente proporzionale a questa quantità di carica. Ora, un grammo-atomo di materia contiene un numero di atomi pari al numero N di Avogadro e quindi ciascun atomo trasporta una carica q pari a:
q = z . (96.522/N) coulomb
con z numero intero. Così la carica che ogni ione elettrolitico, di qualsiasi tipo esso sia, trasporta è sempre multipla di 96.522/N, che risulta quindi essere la carica elementare. Stoney osservò che le leggi di Faraday sull’elettrolisi viste dal punto di vista della materia dicono che l’elettricità è costituita da particelle uguali non ulteriormente divisibili. La cosa fu ripresa da Helmholtz nel 1881 e la cosa è importante per l’autorità che aveva il fisico e fisiologo tedesco. Stoney ritornò sul termine elettrone nel 1894 e lo estese alle supposte particelle di carica negativa che già apparivano come le unità elementari di carica elettrica nella costituzione della materia (Of the “Electron” or Atom of Electricity, Philosophical Magazine 38 (5): 418–420; 1894).
(3) Johann Jakob Balmer, Notiz über die Spektrallinien des Wasserstoffs (Nota sulle righe spettrali dell’idrogeno), Verhandlungen der Naturforschenden Gesellschaft in Basel, 7 p. 548–560, 1885.
(4) J. Rydberg, On the structure of the line-spectra in the chemical elements (Struttura degli spettri a righe degli elementi chimici), Philosophical Magazine, 29, p. 331-337, 1890.
(5) H. Helmholtz, Über Integrale der hydrodynamischen Gleichungen, welche den Wirbelbewegungen entsprechen (Gli integrali delle equazioni idrodinamiche esprimenti il Moto Vorticoso), Journal für die reine und angewandte Mathematik, Vol. 55 pp. 25-55, 1858.H. Helmholtz, Über discontinuirliche Flüssigkeitsbewegungen, Monats. Königi. Preuss. Akad. Wiss. Berlin, 23, 215-228, 1868.
(6) W. J. M. Rankine, Hypothesis of Molecular Vortices, Phil. Mag. S. 4, Vol. 27, p. 313, 1864.
(7) W. Thomson, On Vortex Atoms (Sugli atomi vortice), Proceedings of the Royal Society of Edinburgh, 6, pp. 94-105, 1867.
(8) W. Thomson, Notes on Hydrodynamics. On the Vis-viva of a Liquid in Motion, in Cambridge and Dublin Mathematical Journal, 1849.
(9) J. L. F. Bertrand, Théorème relatif au mouvement d’un point attiré vers un centre fixe, in C. R. Acad. Sci. 77: 849–853.
(10) H. Nagaoka, Proc. Tokyo Math. Phys. Soc., 2, 92, 1903 e Kinetics of a System of Particles illustrating the Line and the Band Spectrum and the Phenomena of Radioactivity, Phil. Mag. S 6. Vol. 7, N. 39, pp. 445-455, Marzo 1904.
(11) J. Larmor, On a Dynamical Theory of the Electric and Luminiferous Medium, Part 3, Relations with material media, Phil. Trans. Roy. Soc. 190: 205–300, 1897.
(12) Anticipando qualcosa, si può dire che: nel caso in cui la carica sia quella e dell’elettrone, si ha:
W = K . e2. a2
ed essendo e = 1,6.10-19coulomb, si ha:
W = G . a2
essendo G una costante che vale: G = K . e2 =1,13.10-53 (coulomb)2 s/m .
(13) J.J. Thomson, On the Structure of the Atom: an Investigation of the Stability and Periods of Oscillation of a number of Corpuscles arranged at equal intervals around the Circumference of a Circle; with Application of the Results to the Theory of Atomic Structure, Phil. Mag., S 6, Vol. 7, N. 39; pp. 237-265, Marzo 1904.
(14) J.J. Thomson, On the Masses of the Ions in Gases at Low Pressures, Philosophical Magazine, Series 5, Vol. 48, No. 295, p. 547-567, Dicembre 1899. Questa memoria era stata preceduta da un’altra in cui si affrontavano medesimi problemi: J.J. Thomson, On the Charge of Electricity carried by the Ions produced by Röntgen Rays, Philosophical Magazine, Series 5, Vol. 46, p. 528-545, Luglio-Dicembre 1898. Si tenga conto che lo stesso J. J. Thomson si era abbondantemente occupato dell’idrodinamica dei vortici nel suo libro A Treatise on the Motion of Vortex Rings, London: Macmillan, 1883.
(15) Lord Kelvin (William Thomson) – Aepinus Atomized – From the Jubilee Volume presented to Prof. Boscha in November, 1901. Baltimore Lectures, 1904, Appendix E, pp. 541-568. Riguardo alla richiesta stabilità dei vortici c’è da ricordare che in un fluido perfetto da un punto di vista idrodinamico la forza di cui dispone un vortice è la stessa in ogni punto del vortice stesso ed è data dal prodotto della vorticità (il rotore della velocità) per la sezione trasversale.
(16) Le conferenze furono raccolte e pubblicate nel libro: Electricity and Matter, Westminster, New York 1904.
(17) Di queste esperienze di Mayer era venuto a conoscenza Kelvin nel 1878 ed aveva ringraziato il fisico americano in un articolo su Nature (2 maggio 1878) affermando che gli esperimenti di Mayer avevano fornito una perfetta illustrazione meccanica (e noi già sappiamo quanto Kelvin fosse legato ai modelli meccanici) dell’equilibrio cinetico di gruppi di vortici a colonna rotanti in cerchio intorno al loro comune centro di gravità ed aveva in tal modo fatto luce su alcuni problemi che nascevano riguardo alla costituzione della materia.
(18) J. J.Thomson lavorò in un modo quasi ossessivo su corpuscoli, particelle ed atomi. Rispetto al numero di elettroni in un atomo egli, agli inizi, credeva ve ne dovessero essere intorno ai 10 mila, mentre in questo modello del 1904 si erano ridotti intorno al centinaio.Più in generale:
– Egli iniziò con l’atomo vortice che poi abbandonò.
– Nel 1890 iniziò a parlare di atomi primordiali come costituenti base degli atomi degli elementi del sistema periodico.
– Nel 1897 iniziava a parlare di corpuscoli e a riferirsi alle esperienze di Mayer
– Nel 1899 fornì un disegno qualitativo dell’atomo: Considero l’atomo costituito da un gran numero di corpi più piccoli che chiamerò corpuscoli […] In un atomo normale questo insieme di corpuscoli forma un sistema elettricamente neutro. Sebbene i corpuscoli individuali si comportino come ioni negativi, ciononostante quando sono sistemati in un atomo neutro l’effetto negativo è bilanciato da qualcosa che causa un’azione dello spazio in cui i corpuscoli sono disposti come se ci fosse una carica positiva uguale alla somma delle cariche negative dei corpuscoli.
– Nel 1903 continuò con il modello qualitativo.
– A partire dal 1904 e fino al 1909 studiò la stabilità dei supposti anelli su cui erano sistemati gli elettroni.
(19) Dmitrij Ivanovič Mendeleev (1834-1907) è un chimico russo che sistematizzò gli elementi noti ordinandoli in termini del loro aumento di massa e delle loro proprietà chimiche in una tavola (tavola periodica) lasciando liberi gli spazi per gli elementi ancora non conosciuti ma che sarebbero dovuti esistere (come poi si dimostrò) e determinando addirittura le proprietà che tali elementi ignoti avrebbero dovuto avere. Comunicò la sua scoperta alla Società Chimica Russa nel marzo del 1869 con il titolo: The Dependence between the Properties of the Atomic Weights of the Elements.
(20) J.J. Thomson, On the Number of Corpuscles in an Atom, Philosophical Magazine, 11, p. 769-781, giugno 1906.
Devo sottolineare che i modelli che presento non esauriscono i vari tentativi che in quegli anni furono elaborati. Riporto qui di seguito almeno i titoli di alcuni tentativi fatti (tratto da http://skullsinthestars.com/2008/05/27/the-gallery-of-failed-atomic-models-1903-1913/ ). Non discuto il loro funzionamento che potrà essere trovato nelle memorie originali o nel link fornito.
– Nel 1901 Jean Perrin aveva scritto una memoria discorsiva, resoconto di una conferenza agli Amici dell’Università di Parigi, sulla possibile esistenza di un atomo planetario, Les hypothèses moléculaires, Rev. Scientifique, 15, p. 449-461, 1901. Un tale lavoro egli ipotizzava un nucleo positivo circondato da elettroni negativi. L’atomo sarebbe costituito da una o più masse con una forte carica positiva…..e da una moltitudine di corpuscoli simili a piccoli pianeti negativi. Egli mostrò che gli elettroni debbono muoversi nelle loro orbite con velocità corrispondenti alla frequenza delle onde luminose e che gli elettroni più esterni si sarebbero potuti staccare facilmente per produrre raggi catodici, radiazioni β e fenomeni simili.
– Nel 1903 vi fu il modello atomico dinamico di Lenard, Über die Absorption der Kathodenstrahlen verschiedener Geschwindigkeit, Ann. Physik, 12, 714-744, 1903.
Atomo di Lenard
– Nel 1906 vi fu la memoria di Rayleigh che illustrava il suo modello di elettrone fluido,On electrical vibrations and the constitution of the atom, Phil. Mag., Ser. 6, Vol. 11, 117-123, 1906.
Atomo di Rayleigh
Vi è una importante conclusione che trovò Rayleigh a proposito dei tentativi di mettere in relazione le vibrazioni degli elettreoni con gli spettri atomici e che suona ora come una premonizione estremamente fondata. Scriveva Rayleigh:
Le frequenze osservate nello spettro possono non essere affatto frequenze di oscillazione nel senso ordinario, ma formare piuttosto una parte essenziale della costituzione originale dell’atomo, come determinata da condizioni di stabilità.
– Nel 1906 James Jeans scrisse una memoria sulla costituzione dell’atomo con l’elettrone vibrante, On the constitution of the atom, Phil. Mag., Ser. 6, Vol. 11, 604-607, 1906.
Atomo di Jeans
– Nel 1906 vi fu ancora la memoria di G.A. Schott che illustrava il suo modello atomico di elettrone in espansione, On the electron theory of matter and the explanation of fine spectrum lines and of gravitation, Phil. Mag., Ser. 6, Vol. 12, 21-29, 1906.
Atomo di Schott
– Nerl 1910 vi su il modello archion di J. Stark, Prinzipien der Atomdynamik: Die Elektrischen Quanten (Leipzig, Verlag von S. Hirsel, 1910).
Modello di Stark 1
Modello di Stark 2
Noto a margine che nella memoria di Thomson in oggetto vengono citati alcuni risultati trovati dal fisico teorico italiano Ottaviano Fabrizio Mossotti.
BIBLIOGRAFIA
(1) AA. VV. – Scienziati e Tecnologi dalle origini al 1875 – EST Mondadori 1975
(2) Emilio Segrè – Personaggi e scoperte nella fisica contemporanea – EST Mondadori 1983
(3) E. Whittaker – A History of Theories of Aether and Electicity – Nelson and Sons 1952
(4) Articoli di Enrico Bellone in: Paolo Rossi (diretta da) – Storia della scienza – UTET 1988
(5) Max Born – Atomic Physics – Blackie & Son, London 1962
(6) Max Born – La sintesi einsteniana – Boringhieri 1969
(7) Guido Tagliaferri – Storia della fisica quantistica – Franco Angeli 1985
(8) Mario Gliozzi – Storia della fisica – in: N. Abbagnano (diretta da) – Storia delle Scienze, UTET 1965
(9) René Taton (diretta da) – Storia generale delle scienze – Casini 1965
(10) John L. Heilbron – I dilemmi di Max Planck – Bollati Boringhieri 1988
(11) Piero Caldirola – Lezioni di fisica teorica – Viscontea, Milano, dopo 1950
(12) Samuel Tolansky – Introduzione alla fisica atomica – Boringhieri 1966
(13) Donald S.L. Cardwell – Tecnologia, scienza e storia – Il Mulino 1976
(14) A. Baracca, S. Ruffo, A. Russo – Scienza e industria 1848 – 1915 – Laterza 1979
(15) Enrico Persico – Gli atomi e la loro energia – Zanichelli 1970
(16) Jean Perrin – Les atomes – Gallimard 1970
(17) René Taton – Causalités et accidents de la découverte scientifique – Masson et Cie., 1967
(18) Giuseppe Bruzzaniti – Dal segno al nucleo – Bollati Boringhieri 1993
(19) Maurice de Broglie – Atomes, radioactivité, transmutations – Flammarion 1939
(20) David L. Anderson – The Discover- D. van Nostrand Company 1964
(21) William Bragg – Il mondo della luce – Tumminelli & C. 1935
(22) Kelvin – Opere (a cura di Enrico Bellone) – UTET 197
Categorie:Senza categoria
Rispondi