IL PRIMO CONSIGLIO SOLVAY: BRUXELLES 30 OTTOBRE – 3 NOVEMBRE 1911
Inizio a parlare di Bohr attraverso alcune osservazioni sul Primo Convegno o Congresso Solvay del 1911.
Ernest Solvay, un industriale belga della soda con la passione per la fisica, volle dedicare un poco dei suoi soldi allo sviluppo della conoscenza scientifica. Con l’aiuto del suo amico e collega di Planck a Berlino, il fisico tedesco Walther Nerst, organizzò a Bruxelles un Convegno (il nome originale corretto è Consiglio) ad invito (21 furono gli invitati) su uno dei temi allora più attuali e dibattuti della fisica: La teoria dell’irraggiamento ed i quanti. Questo era il tema del Congresso che era presieduto da uno dei più eminenti fisici del mondo: H. A. Lorentz. Le relazioni dei partecipanti furono: La teoria dell’irraggiamento (Lorentz, Jeans, Warburg, Rubens, Planck, Sommerfeld), I calori specifici (Einstein, Nernst), Le prove della realtà delle molecole (Perrin), La teoria cinetica dei gas (Knudsen), La resistenza elettrica alle basse temperature (Kamerlingh Onnes), Il magnetismo (Langevin)
I lavori del Convegno rivelarono, a partire dalla relazione di Lorentz, l’inconciliabilità della meccanica classica con la legge che Planck aveva trovato per il corpo nero e la necessità di introdurre concezioni nuove. Due fisici tentarono disperatamente di salvare il salvabile delle teorie classiche, Planck e Sommerfeld. Un altro dei teorici del salvare il salvabile, Poincarè, non lo ammise in quell’occasione ma, tornato a Parigi, mostrò di essersi convertito. Ma, per quanto si tentasse di recuperare, almeno questo Convegno una cosa la originò: da questo momento la meccanica, prima solo meccanica, acquistò il rango di meccanica classica e con ciò stesso fu relegata ad un capitolo della fisica. Fu l’inizio di uno scontro tra posizioni divergenti. Da una parte vi era una nuova fisica non ancora sistemata e piena di lacune ed incongruenze ma forte nella spiegazione di vari fatti sperimentali che non si erano potuti spiegare con la fisica classica, dall’altra vi era il possente edificio classico che mostrava lacune su spiegazioni che non riusciva a dare. I termini dei problemi in ballo furono ben descritti da Lorentz nel suo discorso introduttivo:
Le ricerche moderne hanno messo sempre più in evidenza le gravi difficoltà che si incontrano quando si cerca di rappresentarsi i movimenti delle più piccole particelle dei corpi ponderabili e il legame tra queste particelle e i fenomeni che si producono nell’etere. Al momento attuale siamo lontani da quella piena soddisfazione di spirito che la teoria cinetica dei gas, estesa successivamente ai fluidi, alle soluzioni diluite e a insiemi di elettroni, poteva dare ai fisici solo dieci o vent’anni fa. Al suo posto noi abbiamo adesso la sensazione di trovarci in un vicolo cieco essendosi mostrate le antiche teorie sempre più impotenti a fugare le tenebre che ci circondano da ogni lato.
In questo stato di cose, la bella ipotesi sui quanti di energia, enunciata per la prima volta da Planck e applicata a numerosi fenomeni da Einstein, Nernst e altri, è stato un prezioso raggio di luce. Essa ci ha aperto delle prospettive inattese e anche coloro che la considerano con un certo sospetto devono riconoscere la sua importanza e la sua fecondità. Essa ben merita dunque di essere il soggetto principale delle nostre discussioni, e certamente l’autore di questa nuova ipotesi e coloro che hanno contribuito al suo sviluppo meritano che noi rendiamo loro un sincero omaggio.
Ciononostante questa nuova idea, per bella che sia, solleva a sua volta delle serie obiezioni. Io non le rimprovererò di essere m contraddizione con le idee sul moto e sull’azione delle forze che sono state accettate per secoli; capisco perfettamente che non abbiamo alcun diritto di credere che nelle teorie fisiche del futuro tutto si farà conformemente alle regole della Meccanica classica. Ma è fuori di dubbio che, quali che siano i principi che esse utilizzeranno, questi dovranno essere altrettanto precisi di quelli della Meccanica attuale. Ebbene è proprio questa precisione che mi sembra ancora far difetto nelle nuove teorie, cosa del resto ben naturale, vista la difficoltà dei problemi in gioco e il carattere necessariamente provvisorio di esse.
Dal punto di vista della precisione non ci si saprebbe contentare di ammettere che un oscillatore molecolare, esposto al bombardamento degli atomi di un gas, non potesse prendere energia che per quantità finite di grandezza determinata; noi abbiamo il diritto di esigere che ci si possa rappresentare un modo di interazione tra le molecole gassose e l’oscillatore che conduca a tale risultato. È solo in questo modo che si arriverà a stabilire, attraverso pazienti tentativi casuali o per qualche felice ispirazione, questa nuova meccanica destinata a prendere il posto della vecchia.
Ed anche Einstein, in questo Convegno affermò che la questione che si pone ora è quella di sapere quali sono i principi generali della fisica su cui possiamo contare per risolvere i problemi che stiamo trattando.
Dal Congresso non venne fuori nulla di nuovo a parte la consapevoilezza acquisita più o meno da tutti dell’inizio di una nuova era ed io ne parlo solo per rendere conto dello stato di sfiducia esistente verso ogni novità che si affacciava nella spiegazione scientifica, verso l’impatto dirompente della fisica quantistica sui fisici classici. E lo faccio attraverso una lettera di Einstein, il principale innovatore, lì presente con l’onore di chiudere i lavori della Conferenza, o il sabba delle streghe come la definì prima di andare, con una relazione sulla teoria quantistica dei calori specifici che egli trasformò nei problemi che aveva davanti la fisica quantistica. Appena tornato dal Congresso, nel novembre del 1911, Einstein così scriveva al suo caro amico, il professor Heinrich Zangger, direttore dell’Istituto di medicina forense all’Università di Zurigo:
Lorentz ha presieduto con incomparabile tatto e incredibile virtuosità. Parla tutte e tre le lingue ugualmente bene e possiede un’acutezza scientifica unica. Sono riuscito a persuadere Planck ad accettare molti dei miei concetti, dopo che, per anni, egli vi aveva opposto resistenza. È un uomo assolutamente onesto che pensa agli altri anziché a se stesso … Il congresso di Bruxelles è stato interessante all’estremo. Oltre ai partecipanti francesi Curie, Langevin, Perrin e Poincaré, e ai tedeschi Nernst, Rubens, Warburg e Sommerfeld, erano presenti Rutherford e Jeans. E inoltre, naturalmente, H. A. Lorentz e Kamerlingh-Onnes. Lorentz è una meraviglia di intelligenza e di tatto squisito. Un’opera d’arte vivente! A mio avviso era ancora il più perspicace fra i teorici presenti … Poincaré è stato in genere semplicemente ostile (alla teoria della relatività) e, nonostante tutta la sua acutezza, ha dimostrato di capire poco la situazione(1). Planck è bloccato da alcuni preconcetti indubbiamente falsi … ma nessuno sa niente. L’intera faccenda sarebbe stata pura gioia per i diabolici gesuiti. … Il congresso faceva l’effetto di una lamentazione sulle rovine di Gerusalemme.
E si era parlato di soli quanti senza neppure sfiorare la relatività perché lì ci si sarebbe azzuffati. Il fatto è che, come sempre, si tenta di aggrapparsi alle certezze piuttosto che tentare di cambiare. La resistenza alle novità è sempre molto grande e ci vuole davvero una abilità molto grande per convertire i fondamentalisti del passato. E, nella fisica, erano da poco state introdotte appunto due grosse novità che mettevano in grande e grave discussione l’intero edificio della fisica fino a lì costruito con enormi difficoltà. Ne faccio un cenno nel prossimo paragrafo rimandando a quanto ho già abbondantemente scritto in proposito per una comprensione più consapevole sia sui quanti di Planck (anche in modo divulgativo), sia sui quanti di luce di Einstein (effetto fotoelettrico), sia sulla relatività di Einstein (anche in modo divulgativo).
RELATIVITA’ E QUANTI: QUALCHE CENNO
Il lavoro più famoso di Einstein è certamente quello del 1905 e noto come Teoria della Relatività (anche se questo è un modo molto limitativo e banale di chiamare il suo lavoro che aveva per titolo L’elettrodinamica dei corpi in movimento). In somma sintesi, di fronte alle gravissime difficoltà che incontrava l’elettrodinamica a costruire equazioni che descrivessero i fenomeni osservati, di fronte al fatto che tutti i tentativi di risolvere i gravi problemi andavano nel senso di modificare e ritoccare l’elettrodinamica medesima per salvaguardare l’intoccabile meccanica, Einstein azzardò la via copernicana: intervenne modificando la meccanica nei suoi concetti fondamentali (spazio, tempo, movimento, massa, energia) e riportando così le equazioni dell’elettrodinamica a rispondere dei fatti sperimentali. Naturalmente ciò ebbe un impatto clamoroso nel mondo dei fisici (e non solo). Il lavoro di Einstein fu pubblicata sulla più prestigiosa rivista tedesca, gli Annalen der Physik, solo per la fortunata combinazione che alla sua direzione vi era un altro grande della fisica, Max Planck. Davvero non è prevedibile la reazione di molti altri, anche grandi, fisici a tale radicale modifica del modo di vedere il mondo.
Da varie osservazioni astronomiche, da varie equazioni che da Maxwell si elaboravano, Einstein affermò come postulato una cosa che veniva fuori da tutte le parti ma che nessuno osava sostenere con chiarezza traendone tutte le conseguenze. In tutte le equazioni compariva una costante che era di carattere elettromagnetico ma che riguardava anche la meccanica. Questa costante coincideva con la velocità c della luce nel vuoto. Inoltre tutte le esperienze note, a cui occorre aggiungere le osservazioni astronomiche da poco realizzate (Michelson, De Sitter), mostravano sempre velocità che non superavano mai quelle della luce. Sembrava cioè che la luce non sommasse la sua velocità con nulla e che quella fosse una velocità limite, insuperabile. E qui si aveva una violazione intollerabile proprio di quel principio galileiano di relatività: le velocità sembrava non si sommassero algebricamente.
Einstein, che aveva ben presente tutto ciò, partì con due postulati
1) Tutte le leggi della fisica, non solo quelle della meccanica ma anche quelle dell’elettromagnetismo, ubbidiscono al principio di relatività.
2) La velocità della luce nel vuoto ha sempre lo stesso valore da dovunque e comunque la si misuri. Essa non si somma o sottrae ad altre velocità e risulta una velocità limite.
Come si vede, sembra che questi due postulati siano innocui. Sembrano petizioni di principio che in realtà modificano poco o nulla. Invece hanno rivoluzionato radicalmente la fisica e la concezione del mondo. Ma prima di proseguire occorre avvertire che nella nostra vita ordinaria noi non ci imbattiamo né con la relatività né con i quanti. Queste due fisiche riguardano da un lato, relatività, oggetti in moto con velocità dell’ordine di grandezza di quella della luce; dall’altro, quanti, oggetti di dimensioni dell’ordine di grandezza atomica. Ma, nonostante quanto ora detto, ambedue queste fisiche sono indispensabili per capire, almeno un poco, della struttura dell’universo.
Tutti sanno che nella fisica classica i tempi per ciascun osservatore di fenomeni erano sempre gli stessi, dati cioè due osservatori, se uno misurava un tempo t, l’altro avrebbe misurato un tempo t’ che era indiscutibilmente risultava t’ = t. … La relatività prevede invece che i tempi, per due osservatori che siano in movimento a velocità costante l’uno rispetto all’altro, ubbidiscano ad una relazione come la seguente:
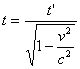
.
Per capire cosa vuol dire occorre considerare quel v2/c2 che compare sotto radice quadrata al denominatore. Questo rapporto può essere molto piccolo (per le velocità ordinarie) ed allora si trascura con la conseguenza che sotto la radice resta un uno, con l’ulteriore conseguenza che t = t’. Se invece v è grande, dell’ordine di grandezza di c, ad esempio tale che quel rapporto valga 3/4, avremmo che t = 2 t’. Ed il risultato è generale: ogni volta che lavoriamo con velocità vicine a c, il tempo passa più lentamente per chi viaggia a velocità dello stesso ordine di grandezza di quella della luce. E’ da osservare una cosa estremamente importante che in futuro chiamerò semplicemente reciprocità. Colui che viaggia a velocità prossime a quelle della luce, in base al principio di relatività, può essere considerato immobile e dal suo punto di vista vedere colui che sta immobile muoversi ad una velocità vicina a quella della luce in verso opposto. Quindi, dal punto di vista del viaggiatore, il tempo passa più lentamente per chi lo vede passare da una situazione di immobilità. Cosa accade in realtà ? Non lo sappiamo, perché per saperlo occorrerebbe fermare chi viaggia a fantastiche velocità e confrontare gli orologi. Ma per far ciò occorrerebbe mettere in ballo delle accelerazioni negative ed usciremo fuori dalla relatività ristretta. Il problema resta quindi quello di una misura e di un confronto di misure. Ci troviamo quindi con una clamorosa novità rispetto alla fisica di Galileo e Newton.
Ma la grandezza tempo è, in meccanica classica strettamente connessa con la grandezza lunghezza e se si modifica il tempo rendendolo funzione della velocità, anche le lunghezze subiranno la stessa sorte con al conseguenza che le lunghezze di oggetti in moto si contraggono, nel verso del moto (anche qui, per il principio di relatività vale la reciprocità).
Supponiamo ora di avere due oggetti con velocità rispettive u e v. La somma di queste velocità, per quanto affermato da uno dei postulati di Einstein, può essere al massimo c. La formula einsteniana per questa somma W è:
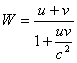
;
supponiamo ora che u sia uguale a c. Si ha:

.
Ed ecco che la somma di due velocità ci fornisce al massimo c. Per confermare ciò nel caso limite di c + c, vediamo cosa accade:
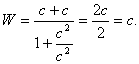
Einstein è noto per una sua formula tanto semplice quanto rivoluzionaria:
E = mc2
Provo a dire la grande novità che essa rappresenta rispetto al passato newtoniano. Noi sapevamo che in una relazione in cui compare energia, massa e velocità al quadrato, avevamo a che fare con le due variabili energia e velocità e con una costante: la massa. Ricordiamo ad esempio l’espressione che ci fornisce in fisica classica l’energia totale di un sistema: essa è:
E = mv2
Si può vedere che si tratta apparentemente della stessa cosa: nella prima relazione compare la velocità c della luce, nella seconda una velocità v qualunque. Ho detto apparentemente perché qui vi è una differenza sostanziale. Nella relazione classica, come detto, le variabili sono E e v. Mentre nella relazione einsteniana le variabili sono E ed m (ricordo che c è una costante). Si ha quindi:
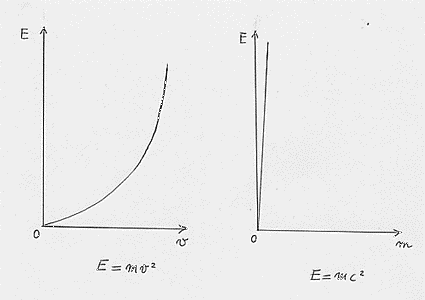
e si può vedere che la relazione di Einstein introduce il concetto di massa variabile, di massa che è la stessa cosa dell’energia, di una piccolissima massa che equivale ad una infinitamente grande quantità di energia. In modo un poco estemporaneo si può pensare alla massa come ad un concentrato di energia ed all’energia come massa sfumata, diffusa nello spazio. Ma vi è un qualcosa nelle considerazioni che abbiamo fatto che ci porta a pensare a massa che debba variare? Sembrerebbe di no, a meno che non si faccia attenzione. Il tutto nasce sempre da lì: dalla velocità c che non può essere superata. Vediamo.
Supponiamo un oggetto in caduta in uno spazio enorme. Esso è soggetto, supponiamo, ad una gravità come quella terrestre. La sua velocità, cadendo, aumenta di circa 10 metri al secondo ogni secondo. Con questa accelerazione di gravità l’oggetto, dopo circa una caduta di un anno e mezzo solare, raggiungerebbe la velocità della luce. Ma l’oggetto continua a cadere pur non potendo aumentare la sua velocità. Vedete che siamo in difficoltà? Qual è l’altra grandezza che compare nella formula che ci dà la caduta di un oggetto? Proprio la massa! A velocità che non può aumentare, inizia a cambiare il valore della massa. E’ un modo solo intuitivo, ma mostra alcune conseguenze della relatività che, in alcun modo possono essere messe d’accordo con la meccanica newtoniana.
Non è qui il caso di entrare in dettagli ma queste modifiche radicali nella meccanica hanno comportato modifiche semplici nelle equazioni di Maxwell-Lorentz, tali da accordarle con alcuni fenomeni prima non riconducibili ad esse.
Vediamo ora quali sono le questioni messe in ballo dalla fisica dei quanti.
Secondo la teoria ondulatoria l’energia trasportata da un’onda è proporzionale alla sua ampiezza. Tale energia non dipende in alcun modo dalla frequenza dell’onda. Per intenderci, a parità di ampiezza, un’onda luminosa rossa ed una viola, trasportano la stessa energia. Quindi se inviamo un’onda rossa ed una viola (con medesime ampiezze A) contro un ostacolo, esse dovrebbero cedere all’ostacolo la stessa quantità di energia. Sperimentalmente però le cose non vanno così. Se disponiamo di una lamina metallica e, su di essa, inviamo luce gialla o viola, anche con ampiezze differenti (maggiore la gialla della viola), accadono fatti straordinari o, perlomeno, non comprensibili con l’ordinaria teoria ondulatoria.

fig. 7
Il fatto straordinario è che anche una debolissima luce ultravioletta (UV) è capace di strappare elettroni da un metallo, mentre un faro da 1000 watt giallo non ci riesce. Sembra incontrovertibile che qui sia la frequenza e non l’ampiezza a giocare un ruolo fondamentale che comunque non rientra in alcun modo nei canoni esplicativi ondulatori. A questi fatti si somma un altro sorprendente fenomeno che, questa volta, non rientra nei canoni interpretativi della teoria ondulatoria: il corpo nero che abbiamo visto abbondantemente. E si ricorderà che non vi era modo di accordare la fisica nota con i fatti sperimentali.
Planck, ed anche qui lo abbiamo visto, prese a trattare la teoria del corpo nero ed operò teoricamente ed analiticamente su di essa in vari modi. Si accorse che solo effettuando un ardito passaggio la teoria avrebbe coinciso con i fatti sperimentali. Si trattava di toccare una delle grandezze fondamentali della fisica, l’energia. Questa grandezza era sempre stata comunemente intesa come continua, come un qualcosa che si prende o si dà in quantità a piacere. Planck si trovava di fronte ad un problema probabilistico del tipo: come sistemare un certo numero di oggetti in un numero dato di caselle (come suddividere l’energia tra vari stati energetici). Si trattava di “frantumare” quella grandezza continua in tante piccole parti (la cosa era già stata fatta da Boltzmann) da sistemare nelle differenti caselle. Ma mentre Boltzmann aveva fatto l’operazione di limite facendo tendere a zero le dimensioni delle quantità discrete di energia, continuando a trovare il disaccordo della teoria con l’esperienza, Planck non fa questa operazione e mantiene queste energie in quantità piccole e discrete, i quanti. Cosa vuol dire una cosa del genere? Semplicemente che, a livelli microscopici l’energia si distribuisce in quantità discrete. La cosa risultava veramente straordinaria. La si doveva ammettere solo perché questo artificio di calcolo rimetteva a posto il disaccordo esistente tra teoria ed esperienza nel fenomeno del corpo nero. La cosa comunque non piaceva, ad iniziare dallo stesso Planck … Si trattava in definitiva, di sostituire ad una grandezza continua (l’energia E) la somma di n, con n numero intero,piccole grandezze discrete (i quanti hν, con h costante di Planck e ν frequenza della radiazione):
E = hν
Quindi un corpo può cedere o acquistare energia cedendo o acquistando quanti, sempre in numero intero e mai in frazione. Dai conti fatti e successivamente perfezionati la scala dei quanti era la seguente:
1/2 h ν; 1/2 h ν + 1 h ν; 1/2 h ν + 2 h ν; 1/2 h ν + 3 h ν; ……..
in pratica vi era una quantità 1/2 hν che si aveva all’inizio della scala e che rimaneva sempre sommata ai singoli quanti interi (questa vicenda, vedremo, sarà fondamentale per capire moltissime cose). In tal modo, la formula precedentemente data diventa:
E = (1/2 + n) . h ν
Si può notare un fatto fondamentale: l’energia dipende dalla frequenza! Maggiore frequenza, maggiore energia. Ricordando che 1/2 ed n sono numeri puri, l’energia risulta uguale ad una frequenza ν per quella costante h che non può essere un numero puro ma deve avere delle dimensioni, quelle cioè di una energia moltiplicata per un tempo (grandezza nota come azione e mai ben chiarita). Inoltre h, invariante spazio temporale, ha un valore numerico enormemente piccolo (un 1 diviso per un numero con 34 zeri):
h = 6,63.10-34 joule.secondo
e questa piccolezza di h fa si che i quanti abbiano un peso solo in un mondo microscopico (atomico, molecolare, nucleare). Nel mondo che cade sotto i nostri sensi i quanti sono assolutamente trascurabili. Sto dicendo che la fisica ordinaria (classica o newtoniana) va benissimo per trattare il mondo macroscopico.
Dicevamo che l’energia dipende dalla frequenza. Dicevamo pure che il mondo dei fisici non era soddisfatto dei lavori di Planck. Serviva l’intervento di un giovane fisico, Einstein, per comprendere tutta la potenza di quanto Planck aveva trovato. Il primo uso dei quanti per una spiegazione di un fenomeno fisico lo fece lui con l’effetto fotoelettrico. Usò di quella energia dipendente dalla frequenza e con un brillantissimo lavoro (che gli valse il Nobel nel 1921) spiegò l’effetto fotoelettrico, fenomeno che da venti anni sfuggiva ad ogni elaborazione. Servono proiettili di una data energia per staccare elettroni da un atomo e la radiazione UV ha questa energia perché dotata di maggiore frequenza della radiazione. Questi proiettili sono quanti di luce, i fotoni come li ribattezzò Lewis nel 1926. Si ritorna così ad una sorta di teoria corpuscolare con particelle (i fotoni) che hanno caratteristiche ondulatorie (la frequenza) e si comportano come particelle. Vedremo più avanti, quando parleremo dell’energia di punto zero, le enormi implicazioni di tale affermazione.
Abbiamo quindi due teorie che hanno mostrato il loro funzionamento esplicativo e predittivo su moltissimi fenomeni noti da molto tempo e non riconducibili ad una spiegazione classica. Abbiamo anche una generale avversione a queste teorie da un mondo di fisici che non vogliono rinunciare alla elegante e spesso brillantissima fisica classica. Ci vuole molto coraggio perché vi è il prestigio da difendere di fronte agli altri e questo coraggio, in genere, lo hanno solo i giovani. Tra ciò che sfuggiva ad una completa descrizione classica, oltre a quanto accennato, vi era, come visto, la struttura atomica. Si era più o meno capito con Rutherford come stavano le cose ma se non si sistemava la stabilità il tutto era un castello costruito sulla sabbia.
LA CARICA DELL’ELETTRONE
Vi è un qualcosa di rilievo che accade tra il 1900 ed il 1914, la determinazione della carica dell’elettrone. Sapevamo che J.J. Thomson nel 1897 aveva misurato il rapporto della carica divisa la massa (e/m) dell’elettrone ed avevo allora detto che sarebbe servita una qualche misura diversa da mettere a sistema con quella di J.J. Thomson per avere separatamente le misure di carica e massa. Da quella misura di e/m era passato del tempo e molti dati si erano accumulati a partire da due diversi ambiti di ricerca, da una parte le misure delle cariche trasportate dalle particelle β nei fenomeni radioattivi e le considerazioni dello stesso Rutherford tra la carica del nucleo rispetto a quella degli elettroni (1911), dall’altra le elaborazioni teoriche che discendevano dallo studio del corpo nero in relazione con il numero N di Avogadro. Fu proprio Planck che, nel suo lavoro sulla radiazione del corpo nero del 1900, fornì il valore della carica dell’elettrone a partire da una determinazione teorica del numero di Avogadro. Planck ottenne per N il valore N = 6,175.1023 molecole per mole. Essendo nota poi la costante F = N.e di Faraday, la carica cioè di una mole monovalente, F = 96.485 coulomb/mole, dividendo F per N si otteneva la carica di un elettrone, cioè e = 4,69.10-10 u.e.s.. Questo era il miglior valore di e, da una determinazione indiretta, che si ebbe prima del 1900 ma non lo si sapeva e rimase abbastanza trascurato. Su un altro fronte Rutherford lavorava con Geiger alla determinazione della radioattività di un grammo di radio e della carica totale trasportata nell’unità di tempo dalle particelle emesse da una quantità nota di radio. Nel 1908 Rutherford comunicò alla Royal Society di Londra che la carica positiva E portata da una particella α del radio C è 9,3.10-10 u.e.s. Da ciò egli trasse alcune conseguenze di rilievo: il valore di e, la carica di un atomo d’idrogeno, diviene 4,65.10-10 u.e.s.. E nel lavoro che illustrava la comunicazione alla Royal Society Rutherford diede solo un cenno in nota al fatto che un simile valore era stato trovato per altra via da Planck. E’ da notare che Rutherford non dette importanza a questa determinazione che invece fu usata da Einstein al Congresso di Salisburgo del 1909 per sostenere la validità della teoria di Planck.
Va ricordato che nel 1899 vi erano state delle misure dirette di e (e quindi, sostituendo il valore di e nel rapporto e/m, si riusciva a conoscere m) da parte di J.J. Thomson che si era servito di alcune tecniche introdotte (1895) da C.T.R. Wilson (camera a nebbia: cariche elettriche negative servono come nuclei di condensazione nella formazione della nebbia da un vapore soprasaturo. Il diametro o il volume delle goccioline che formavano la nebbia si poteva ricavare dalla loro velocità di caduta). Thomson aveva trovato per e il valore e = 3.10-10 u.e.s. Questo metodo delle goccioline in caduta fu perfezionato ed utilizzato dal fisico americano Robert Millikan nel 1910 che, insieme al suo collega Harvey Fletcher, per e trovò e = 4,78.10-10 u.e.s. Millikan pubblicò da solo i risultati iniziando una pesante controversia con il suo collega. Obiezioni all’esperienza di Millikan vennero dal fisico austriaco Felix Ehrenhaft che sostenne di aver misurato cariche elettriche più piccole di quelle del per lui supposto elettrone. Milikan ripeté allora l’esperienza migliorandola e pubblicò di nuovo i risultati nel 1913(2).
Altro fatto notevole è che all’epoca da varie fonti venivano fatte ricerche sulla carica dell’elettrone. Una di esse, quella di A.E. Haas, aveva trovato il valore e = 3,18.10-10 (3).
BIOGRAFIA SCIENTIFICA DI NIELS BOHR
Le cose stavano a questo punto nel 1911 quando il neolaureato all’Università di Copenaghen, Niels Bohr si recò a Cambridge per approfondire la sua preparazione con J.J. Thomson.
Niels Bohr era nato a Copenhagen da una ricca famiglia, suo padre era professore di fisiologia all’Università mentre sua madre Ellen Adler aveva interessi nel mondo bancario e finanziario. Dopo studi superiori fatti al Collegio Grammelholms, nel 1903 si iscrisse all’Università di Copenhagen per studiare fisica, come disciplina principale, quindi matematica, astronomia e chimica. Suo professore di fisica fu Christian Christiansen e di filosofia Harald Hoffding. Nel 1909 conseguì il Master in fisica e nel 1911 divenne Dottore. La sua tesi dottorale era eminentemente teorica e riguardava la spiegazione delle proprietà dei metalli mediante la teoria degli elettroni di Lorentz, lavoro che rimane ancora un classico sull’argomento. Portando a termine questo lavoro, Bohr si confrontò per la prima volta con la teoria della radiazione e dei quanti di Planck.

Bohr nel 1911
A settembre del 1911, grazie ad una borsa di studio della fondazione Carlsberg, scelse di recarsi, come accennato, a Cambridge per approfondire quanto iniziato nella sua tesi di dottorato, nel luogo dove c’era il maggior conoscitore di elettroni i laboratori Cavendish di J.J. Thomson. Sembra però che non si trovasse a suo agio con J. J. Thomson, forse per la lingua o per i diversi costumi o ancora perché Thomson gli aveva assegnato un lavoro in laboratorio o infine perché Thomson dopo oltre un mese e mezzo non aveva ancora letto la sua tesi di dottorato. Conobbe però, ad un convegno che si tenne a Cambridge, Ernest Rutherford con il quale si trovò subito in sintonia e con il quale iniziò a lavorare nell’estate del 1912. E proprio a luglio di quell’anno consegnò a Rutherford una bozza memorandum di un lavoro che stava facendo Sulla costituzione degli atomi e delle molecole, per conoscere le sue opinioni. E qui merita leggere le condivisibili argomentazioni di Baracca, Ruffo e Russo in proposito:
Bohr parte dall’aspetto sperimentale della diffusione delle particelle α per accettare senza riserve il modello di atomo nucleare di Rutherford anche se questo (nel 1912) non appare per nulla il più adatto a spiegare l’insieme dei fenomeni fisici e chimici, come sembra promettere al contrario il modello di Thomson. Egli d’altra parte è convinto che il problema della stabilità di tale struttura (in particolare nel caso dell’atomo di idrogeno, con un solo elettrone) non può essere risolto nell’ambito delle leggi classiche e ricorre quindi ad un’ipotesi «per la quale non si farà alcun tentativo di fondazione meccanica» per fissare le diverse orbite elettroniche. Si possono forse già cogliere qui le prime radici di una svolta che si produrrà nell’elaborazione delle teorie dei quanti: anziché partire dall’analisi di dati fenomenologici all’interno di un generale approccio termodinamico per giungere, come avviene ad esempio in Einstein, a princìpi di quantizzazione, Bohr capovolge il procedimento postulando direttamente una regola di quantizzazione. Anche se a prima vista non sembra trattarsi di un cambiamento così radicale, l’adozione sistematica di questo metodo condurrà ad una vera e propria contrapposizione rispetto alle «vecchie» teorie dei quanti. Nel caso specifico l’ipotesi quantistica che Bohr introduce consiste nel postulare che l’energia cinetica posseduta da un elettrone che ruota su di un’orbita stabile – senza cioè emissione di radiazione, altrimenti l’elettrone perderebbe energia(4) – intorno al nucleo sia proporzionale alla frequenza di rotazione(5). A proposito di quest’ipotesi quantistica si devono fare due osservazioni. In primo luogo essa viene enunciata nel memorandum senza alcun riferimento alla costante di Planck h, con la quale essa ha però un legame molto stretto(5). In secondo luogo, dall’esistenza di orbite stabili sulle quali l’elettrone non irradia si deve dedurre che cade il legame che tutti postulavano tra frequenza della radiazione emessa o assorbita dall’atomo e frequenze proprie degli elettroni al suo interno: una intuizione di cui vedremo tra poco tutta la portata a proposito degli spettri. Nel memorandum infatti Bohr non fa alcuna menzione delle righe spettrali. In esso invece lo spazio maggiore viene dedicato al problema dei legami chimici, che gioca quindi ancora un ruolo fondamentale, ma di solito del tutto trascurato, nella formulazione che risulterà decisiva del modello d’atomo: Bohr sostiene che i legami chimici possono essere perfettamente spiegati in base al nuovo modello supponendo che gli anelli elettronici vengano in qualche modo «messi in comune» tra gli atomi che si combinano, un’idea che sembra precorrere quelle sul legame «non polare».
Manca invece nel memorandum, come si diceva, qualsiasi riferimento agli spettri atomici, che pure costituiranno il punto di partenza delle tre memorie pubblicate nel 1913.
Leggiamo allora alcuni brani iniziali di questa bozza memorandum:
N. BOHR
Prima bozza delle considerazioni contenute nel lavoro, Sulla costituzione degli atomi e delle molecole’ (scritta per mostrare queste considerazioni al prof. Rutherford)
[A.1] Secondo il modello atomico proposto dal prof. Ruutherford, per spiegare la grande diffusione (big scattering) delle particelle α, gli atomi consistono di una carica positiva concentrata in un punto (in una regione molto piccola a confronto delle dimensioni degli atomi) circondata da un sistema di elettroni, la cui carica totale è uguale a quella del «nucleo» positivo il nucleo è pure assunto come sede della massa dell’atomo. In un tale atomo non può esservi nessuna configurazione d’equilibrio, senza moto degli elettroni. (Non è assegnato nulla che determini un valore della dimensione, una «lunghezza» [come invece vi è nell’atomo di Thomson]). Consideriamo quindi in primo luogo le condizioni di stabilità di un anello di n elettroni che ruotano attorno ad una carica positiva puntiforme di grandezza ne.
Un’analisi analoga a quella usata da Sir J. J. Thomson, nella sua teoria della costituzione dell’atomo, mostra molto facilmente, che un anello come quello considerato non possiede alcuna stabilità nell’ordinario significato meccanico [infatti la stabilità nel modello atomico di J. J. Thomson è materialmente fondata sulla circostanza che la forza attrattiva aumenta al crescere della distanza dal centro; perciò l’aggiunta di elettroni all’interno dell’anello aumenta la stabilità (nel suo modello), perché questi rendono ancora maggiore la rapidità con cui la forza aumenta; come si vede subito, nulla di simile altera la stabilità nel modello atomico del prof. Rutherford (se gli elettroni non sono esattamente nel centro dell’anello, ma disposti per esempio in anelli attorno ad esso, la loro presenza abbasserà piuttosto la stabilità (perché ogni ulteriore elettrone scherma l’effetto della carica positiva del nucleo e quindi diminuisce la forza da esso esercitata sugli elettroni dell’anello esterno)], e il problema della stabilità deve quindi essere trattato da un punto di vista molto diverso. [ … ]
[A.2] Nello studio della configurazione degli elettroni negli atomi incontriamo subito la difficoltà (connessa con l’instabilità menzionata) che un anello, se sono dati solo la forza della carica centrale e il numero degli elettroni nell’anello, può ruotare con un numero infinitamente grande di tempi di rotazione diversi, a seconda del diverso raggio assunto per l’anello; e pare non esservi nulla (a motivo della stabilità) che consenta di discriminare in base a considerazioni meccaniche tra i diversi raggi e tempi di vibrazione. Nell’ulteriore ricerca introdurremo ed useremo pertanto un’ipotesi, da cui possiamo determinare le quantità in questione. L’ipotesi è: che esista per ogni anello stabile (ogni anello realizzato negli atomi naturali) un rapporto definito tra l’energia cinetica di un elettrone nell’anello e il tempo di rotazione [in realtà come è chiaro dal seguito, è il rapporto tra energia cinetica e frequenza di rotazione ad essere costante: è l’ipotesi fondamentale che si ritrova poi nelle tre memorie del ’13]. Quest’ipotesi, per la quale non si farà nessun tentativo di fondazione meccanica (poiché questa appare senza speranza), è assunta come la sola che sembra offrire una possibilità di spiegare l’insieme dei risultati sperimentali che si raccolgono e sembra confermare concezioni del meccanismo della radiazione come quelle proposte da Planck ed Einstein. [ … ]
Vedremo tra un poco qual è l’ipotesi che Bohr vuole proporre, qui egli ci fa sapere indirettamente che nella sua costruzione teorica i dati della spettroscopia non sono presi in considerazione. Egli non era infatti uno spettroscopista essendosi occupato d’altro nei suoi primi lavori. Confrontando però questo memorandum con i lavori che pubblicherà da qui a poco, vi è certamente stato un qualche suggerimento (lo stesso Rutherford ?) che lo ha spinto a studiare ed a tener conto dei risultati della spettroscopia tra i quali i recentissimi dell’astronomo Nicholson che con la spettroscopia applicata alla costituzione della corona solare e con un’ipotesi simile a quella che vedremo essere di Bohr era riuscito a rendere conto con elevatissima precisione delle linee spettrali osservate. E Nicholson, nel suo lavoro del 1911-12, che Planck conobbe alla fine del 18912, aveva scritto:
Se la costante di Planck h è significativa per l’atomo, come ha supposto Sommerfeld, allora questo può significare che il momento angolare può crescere o diminuire solo per quantità discrete allorché gli elettroni abbandonano l’atomo o vi ritornano. Si vede senz’altro che questo punto di vista presenta minori difficoltà che non l’interpretazione usuale che implica una costituzione atomica della stessa energia.
Vi era inoltre un altro fatto della fine del 1911 e lo conosciamo da una lettera che egli scrisse al suo amico C.W. Oseen, fisico teorico svedese. Egli era particolarmente entusiasta delle scoperte del fisico P. Weiss sul magnetismo perché mostravano l’esistenza di unità fondamentali di magnetismo (atomi di magnetismo) e questo andava a sostegno delle idee che si andava costruendo: se infatti le proprietà magnetiche della materia dipendevano dal moto degli elettroni in orbite elettroniche, e se si avevano unità fondamentali di magnetismo, ciò voleva dire che i momenti angolari degli elettroni avevano valori determinati.
In ogni caso anche a Manchester Bohr non era entusiasta del lavoro sperimentale sulla radiazione α che gli aveva assegnato Rutherford. Egli aveva uno spiccato interesse per gli elettroni in una sorta di elaborazione successiva del suo lavoro di dottorato. Da una lettera al fratello del giugno 1912 sappiamo che era accaduto qualcosa che raccordava le radiazioni α con gli elettroni e quindi motivava Bohr al lavoro con Rutherford. Un articolo del fisico C.G. Darwin, nipote del più famoso Darwin, trattava dell’assorbimento delle particelle α da parte della materia. In questo lavoro si trattava tale fenomeno come se si dovesse considerare solo l’azione del nucleo degli atomi della materia attraversata da tali particelle. Bohr riteneva ciò non corretto distinguendo il problema dell’assorbimento da quello della diffusione. E mentre nel caso della diffusione era lecito trascurare il contributo degli elettroni atomici rispetto alle forze che erano in gioco tra particella e nucleo, nel caso dell’assorbimento non si potevano trascurare le forze di legame degli elettroni con il nucleo. Fu una questione del genere che spinse Bohr ad approfondire il problema dell’assorbimento di particelle α da parte della materia per studiare meglio il ruolo degli elettroni e per scrivere un qualcosa che sistemasse l’articolo di Darwin (tra l’altro stava per finire la borsa e, dovendo tornare in Danimarca era preoccupato per il suo futuro all’Università perché aveva poche pubblicazioni). Nel fare questa operazione però Bohr dovette iniziare ad occuparsi di un qualcosa che prima non lo aveva interessato: il modello atomico di Rutherford (modello nucleare), che era la naturale strada per capire cosa facessero gli elettroni nel caso di assorbimento di particelle α da parte della materia (e questo modello era preferibile a quello di Thomson anche perché con esso era più semplice costruire la tavola periodica degli elementi e spiegare vari aspetti della fenomenologia nota tra cui la distinzione che permetteva tra fenomeni chimici e radioattivi). Ed in poco tempo egli trovò un’espressione per la perdita di energia della particella α per urto con un elettrone atomico che teneva conto del tempo della collisione e dell’energia che aveva l’elettrone soggetto alla forza di legame. Tale espressione era in buon accordo con i risultati sperimentali sull’assorbimento e questo, che era un grande risultato, lo emozionò tanto che, tornato a Copenhagen, quando fece la pubblica relazione del suo lavoro in Gran Bretagna, disse (settembre 1912):
Se in conclusione devo descrivere in poche parole la differenza caratteristica tra le conoscenze che si ottengono per mezzo dello studio della diffusione e dell’assorbimento dei raggi alfa, potrei forse dire che il primo fenomeno (la diffusione dei raggi) ci fa partecipi di conoscenze sul comportamento statico degli atomi, in quanto ci mostra la grandezza e la natura dei campi di forza nell’interno degli atomi e con ciò il numero e la carica delle particelle in essi presenti; mentre il secondo fenomeno (l’assorbimento dei raggi) ci fornisce informazioni sul comportamento dinamico degli atomi, poiché l’assorbimento – in quanto dipendente dal movimento degli elettroni – ci dà conto dei loro tempi di oscillazione.
Quindi Bohr era già passato a studiare il comportamento degli elettroni in un atomo e le loro frequenze di oscillazione.
Nel memorandum dell’estate 1912, subito dopo il brano riportato e sempre con il fine di risolvere il problema della stabilità dell’atomo, Bohr comunicava qual era la sua ipotesi:
Usando l’ipotesi particolare E = k.v [Bohr non menziona la costante di Planck h; in realtà è k = 1/2 h], possiamo dedurre che l’energia di un sistema che contiene un anello di n elettroni soggetti ad una forza centrale (e2/r2).X è uguale a ~n·X2.A dove A vale approssimativamente 1,3.10-11erg ed NA = 1,9.105 cal (N numero di molecole in l mole del gas).
Quindi Bohr aveva già assunto i quanti come base su cui costruire la sua struttura atomica e
L’ipotesi menzionata sembra pienamente corroborata dai fatti sperimentali; si può mostrare che essa offre una spiegazione di:
1. la legge periodica del volumi atomici degli elementi;
2. la legge di Widdington sulla relazione tra la velocità necessaria per eccitare i raggi Rontgen caratteristici di un elemento, e il peso atomico di quell’elemento;
3. (approssimativamente) la legge di Bragg dell’assorbimento dei raggi a da parte di elementi diversi;
4. sembra spiegare la stabilità e il calore di combinazione di alcuni dei singoli composti. [ … ]
Sembrava che le cose fossero tutte al loro posto ma proprio le osservazioni di Nicholson e uno studio accurato degli spettri (con la scoperta della formula di Balmer che fu molto importante inserita nei ragionamenti che portava avanti) lo convinsero di alcuni difetti del memorandum, particolarmente quello di aver considerato il solo livello fondamentale dell’atomo senza tener conto degli stati (come diremmo oggi) eccitati. Furono proprio gli spettri ed il raccordare i dati di Nicholson, riferiti ad atomi altamente eccitati, con le sue elaborazioni a far fare a Bohr il passo decisivo verso la quantizzazione dell’atomo.
Fu nel marzo del 1913 che Bohr inviò a Rutherford una bozza simile all’articolo che pubblicherà poi in luglio dove era quasi tutto fatto con la completa quantizzazione dell’atomo proprio attraverso gli spettri.
E nel luglio del 1913 vide la luce il primo dei tre articoli di Bohr sulla struttura atomica(6). Tutti e tre con lo stesso titolo, Sulla costituzione degli atomi e delle molecole, il secondo con sottotitolo Sistemi contenenti un singolo nucleo ed il terzo con il sottotitolo Sistemi contenenti parecchi nuclei.
Dopo aver parlato delle varie difficoltà che si incontrano adottando l’atomo di Rutherford, soprattutto in relazione alla sua instabilità sia elettromagnetica che meccanica, Bohr avanza due ipotesi fondamentali da cui parte l’elaborazione del suo lavoro:
Vogliamo ora mostrare che le difficoltà in questione scompaiono se si tratta il problema dal punto di vista del presente lavoro. Prima di procedere, è forse utile riassumere le idee che stanno alla base delle formule scritte. I postulati fondamentali sono i seguenti:
1) l’equilibrio dinamico dei sistemi negli stati stazionari può venire trattato con la meccanica ordinaria, mentre ciò non è possibile per le transizioni del sistema tra due diversi stati stazionari;
2) quest’ultimo processo è accompagnato dall’emissione di una radiazione omogenea, per la quale la relazione tra la frequenza e l’energia è quella data dalla teoria di Planck.
La prima ipotesi si presenta come del tutto naturale, in quanto si sa che la meccanica ordinaria non può avere alcuna validità assoluta, ma può servire soltanto a calcolare certi valori medi. D’altro canto, nel calcolo dell’equilibrio dinamico di uno stato stazionario, in cui non si verifica alcuno spostamento relativo delle particelle, non occorre distinguere tra i moti effettivi e i loro valori medi. La seconda ipotesi è in evidente contrasto con l’elettrodinamica ordinaria, ma sembra necessaria per l’interpretazione dei fatti osservati.
Essenzialmente Bohr basò il suo modello atomico su questi due postulati non giustificati ma enunciati per rendere conto dei fatti sperimentali. Questi postulati, conseguenza diretta dell’applicazione dei quanti alla struttura atomica, affermano, come si intende meglio leggendo il seguito, che in un atomo gli elettroni non possono assumere qualsiasi valore dell’energia ma solo certi valori definiti (si usa dire che in un atomo l’energia è quantizzata). Ciò significa qualcosa di molto importante: solo certe orbite elettroniche possono essere occupate dagli elettroni che ruotano intorno al nucleo e ad ogni orbita corrisponde un determinato valore dell’energia.
Vediamo quanto qui detto formalizzando. Supponiamo di considerare un elettrone che ruoti intorno al nucleo su una determinata orbita; sia r il raggio dell’orbita che stiamo considerando e q = mv la quantità di moto dell’elettrone su questa orbita, di modo che il momento della quantità di moto, meglio, il momento angolare dell’elettrone rispetto al nucleo sarà p = mvr; ebbene, questo momento angolare non può assumere tutti i valori possibili, ma solo alcuni determinati, multipli interi di una data quantità elementare; vale cioè la relazione:
mvr = n(h/2p)
là dove n è un numero intero positivo chiamato numero quantico principale ed h è la costante di Planck.
Il secondo postulato, in particolare, afferma e riconosce che l’elettrone orbitale non può emettere alcuna energia a meno che non cambi orbita (cioè livello energetico); questo passaggio non può avvenire, quindi, gradualmente, ma si ha un vero e proprio salto energetico. Quando, per un qualche motivo, un elettrone salta da una orbita ad energia più alta (livello energetico iniziale: i) ad una energia più bassa (livello energetico finale: f), la sua perdita di energia è emessa sotto forma di quanto di luce. Si ha così:
Ei – Ef = h ν .
dove Ei è l’energia corrispondente all’orbita ad energia più alta, Ef quella corrispondente all’orbita ad energia più bassa ed hn è il quanto di luce della prima teoria dei quanti di Planck. La relazione scritta significa che un elettrone nel passare da una certa orbita ad una ad energia più bassa perde energia, e questa perdita di energia (per la legge di conservazione) la si ritrova sotto forma di emissione di radiazione (emissione di un quanto di radiazione). Nel caso il salto avvenga in senso contrario a quello descritto fin qui si ha assorbimento di un quanto di radiazione hn dall’esterno. [La prova sperimentale dell’esistenza degli stati quantici fu fornita dall’esperienza di Franck ed Hertz nel 1913].
Cerchiamo di ricostruire con un qualche dettaglio i conti di Bohr in modo più semplice ed oggi più comprensibile, abbandonando quindi la ricostruzione delle elaborazioni di Bohr attraverso le sue memorie.
In un atomo l’elettrone orbita circolarmente intorno al nucleo. La forza centripeta (Fcentripoeta = Fc) che mantiene l’elettrone nell’orbita circolare è fornita dalla forza di attrazione elettrostatica (Felettrostatica = Fe) che il nucleo esercita sull’elettrone; deve allora risultare:
Fc = Fe
La forza centripeta è data da:

A questo punto subentra la condizione di Bohr di quantizzazione del momento angolare (che però non è propriamente di Bohr ma solo di una ricostruzione a posteriori):






Introducendo una nuova unità per l’energia, l’elettronvolt ( 1 eV = energia che acquista un elettrone nel passare attraverso la differenza di potenziale di 1 volt):
1 eV = 1,6.10-12erg => 1 erg = 6.1011eV
si ha che quella costante vale 13,6 eV. La (9) può quindi scriversi:

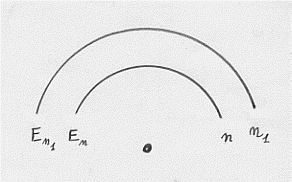
La relazione (10), trovata da Bohr, spiegava bene le righe spettrali osservate la prima volta nel 1906 e relative ad n = 1. Appunto in quell’anno Lyman osservò, con uno spettroscopio per radiazione ultravioletta (UV), uno spettro di radiazione, emesso dall’idrogeno, costituito da tante righe che andavano addensandosi intorno alla lunghezza d’onda di 908 Å (che corrisponde ad n1 = ∞), come mostrato in figura:
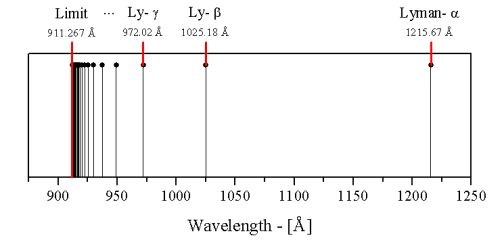
Già nel 1885 erano state osservate le righe spettrali dell’idrogeno situate nella regione del visibile (da 4.000 Å a 7.000 Å) e relative ad n = 2 (si veda figura):

Quindi tutte le altre situate in altre regioni dello spettro. In definitiva, per quel che riguarda il visibile si ritrova la formula che empiricamente aveva dato Balmer. E merito di Bohr fu proprio l’aver dato un significato a quella costante R che avevamo incontrato in quella formula. Inoltre la formula di Bohr era in grado di prevedere altri spettri a frequenze diverse e tutto questo fu confermato sperimentalmente (con una qualche deviazione al crescere di Z, come vedremo). Nella figure che seguono sono riportate tutte le serie spettrali dell’idrogeno:


I due postulati di Bohr forniscono un nuovo modello di atomo che è simile a quello di Rutherford (nucleo centrale carico positivamente in cui era concentrata l’intera massa dell’atomo intorno al quale, su orbite concentriche, ruotavano gli elettroni, in numero pari al numero atomico e tale da rendere neutro l’atomo) con la fondamentale differenza che le leggi che governavano tale struttura non erano ricavabili dalla o riconducibili all’elettrodinamica classica ma fondate su una serie di postulati che affermavano che nell’atomo non si applicava la fisica classica. In particolare, ora non tutte le orbite risultavano permesse all’elettrone (quantizzazione dell’energia o dei livelli energetici). In tal modo l’edificio atomico risultava stabile anche se con qualche difficoltà teorica.
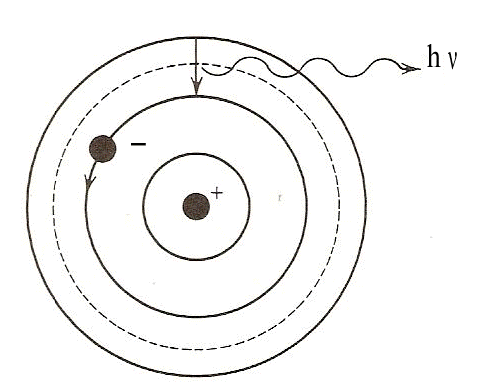
L’atomo di Bohr per l’atomo di idrogeno. E’ schematizzato un elettrone che da un orbita più elevata (stato eccitato) passa ad una più bassa con l’emissione di energia sotto forma di un quanto hν (l’orbita ancora più bassa corrisponderebbe allo stato fondamentale) La circonferenza tratteggiata sta ad indicare un’orbita non permessa, sulla quale un elettrone non può trovarsi.
Si possono riassumere, come l’ha fatto Whittaker, le novità introdotte da Bohr nel modo seguente:
1) Gli atomi producono linee spettrali uno alla volta non essendo responsabili simultaneamente dell’intero spettro.
2) Un singolo elettrone è responsabile della produzione di una linea spettrale.
3) L’atomo di Rutherford fornisce una base soddisfacente per il calcolo delle frequenze dello spettro.
4) La produzione di spettri è un processo quantistico.
5) Un dato atomo può esistere in differenti stati stazionari; in tali stati l’atomo non emette radiazioni.
6) Il momento angolare è quantizzato in unità h.
7) Se si produce una linea spettrale, risultano interessati due stati stazionari ed i termini spettrali possono essere identificati attraverso le energie degli stati stazionari.
8) Sia in emissione che in assorbimento è interessato un quanto di luce e la sua frequenza è determinata dalla relazione E = hν di Planck-Einstein.
9) E’ impossibile visualizzare o spiegare classicamente il comportamento dell’atomo quando avviene la transizione.
PROBLEMI E SUCCESSI: SOMMERFELD
La teoria di Bohr fu accolta con più scetticismo che altro. I due postulati alla sua base si contraddicevano tra loro: da una parte si richiamava la fisica classica per descrivere il moto dell’elettrone, dall’altra la si negava quando di parlava di acquisti o perdite di energia. Inoltre la sua base sperimentale e i fenomeni che spiegava erano ristretti. Era trattato un nucleo ed un solo elettrone (o idrogeno o elio ionizzato), non si sapeva proprio cosa sarebbe accaduto all’aumentare del numero degli elettroni, quando il problema da due corpi sarebbe diventato ad n corpi. In particolare quando le orbite da circolari sarebbero diventate ellittiche come sarebbe dovuto accadere nel caso di atomi a più elettroni (si trattava di ammettere che gli elettroni avessero più di un grado di libertà). Vi era inoltre un altro fenomeno, apparentemente di importanza minore che non trovava spiegazione nella teoria di Bohr, la cosiddetta struttura fine degli spettri, il fatto cioè che, osservando in modo accurato alcune linee spettrali esse risultavano costituite da due o tre linee che viste grossolanamente sembravano appunto una linea sola.
Un contributo fondamentale a questi problemi venne dal fisico tedesco Arnold Sommerfeld (1868-1951) nel 1916(7), che si ispirò ad alcune ricerche teoriche sul significato della costante h nello spazio delle fasi(8), fatte dal fisico austriaco Paul Ehrenfest (1880-1933) nel 1913.
Ehrenfest aveva trovato che nelle orbite circolari degli stati stazionari nella teoria di Bohr dell’atomo di idrogeno, se q denota l’angolo che la linea che congiunge l’elettrone al nucleo fa con una linea fissata, allora la quantità di moto p corrispondente alle coordinate q è il momento angolare dell’elettrone intorno al nucleo e, per stati stazionari, esso deve essere multiplo di h. Ciò corrisponde a dire che ∫pdq = nh.
Sommerfeld generalizzò ciò affermando che in certe condizioni, in un sistema con diversi gradi di libertà, se q1, q2, …. sono le coordinate e p1, p2, …. sono le corrispondenti quantità di moto, allora gli stati stazionari del sistema sono tali che ∫p1dq1, ∫p2dq2, ….. sono multipli di h quando le integrazioni sono estese su periodi che corrispondono alle coordinate. Questa generalizzazione permetteva di quantizzare l’energia in moti centrali periodici, quelli che interessano i movimenti elettronici in un atomo. E poiché il sistema di coordinate è uguale al numero di gradi di libertà del sistema Sommerfeld superava così la limitazione di Bohr ad orbite circolari passando ad orbite ellittiche. Infatti la quantizzazione del momento angolare introdotta da Bohr limitava i gradi di libertà di un elettrone costringendolo ad un raggio R di una determinata orbita. Sommerfeld suppose che l’elettrone, muovendosi nello spazio ha tre gradi di libertà e non uno solo. E le orbite di Sommerfeld, come accennato, risultavano quantizzate. La quantizzazione era rappresentata da un numero intero chiamato numero quantico. Bohr aveva introdotto il numero quantico n (n = 1, 2, 3, ……, ∞) che ci diceva in quale orbita si trovava l’elettrone. Con la quantizzazione delle orbite ellittiche di Sommerfeld (1915), mentre restava immutato il numero n (che continua ad indicare in che orbita ci si trova e quindi in che livello energetico), occorreva introdurre un numero quantico, a (che distingue le serie spettrali l’una dall’altra), per indicare l’eccentricità dell’orbita (in genere si fornisce il numero ℓ= a – 1 che rappresenta il momento angolare in unità h) che ha una stretta relazione con il momento angolare dell’elettrone. Più in dettaglio, dato un livello energetico n, gli ℓ dicono quanti sottolivelli alla stessa energia ha quel livello. Se n = 1 non si hanno sottolivelli, se n = 2 si ha un solo sottolivello, …

Le orbite di Bohr-Sommerfeld (per un dato n vi sono vari ℓ ). Il numero n è chiamato numero quantico principale e determina energia ed asse maggiore delle orbite. Il numero quantico a ≤ n fornisce l’eccentricità dell’orbita. Il numero a – 1 = ℓ fornisce il momento angolare in unità h. Il numero ℓ è chiamato numero quantico azimutale e può valere: ℓ = 0, 1, 2, …., n – 1.
Insomma, si tratta di importanti aggiustamenti all’atomo di Bohr sempre fatti con un ibrido di teoria classica e numeri magici che debbono rendere conto di una quantizzazione forzata. Infatti, ad uno studio più accurato, anche quella stessa energia di cui dicevova corretto perché, per un dato n, gli elettroni che viaggiano su orbite ad ℓ più basso, hanno energia maggiore in quanto passano più vicini al nucleo e debbono avere maggiore velocità (con l’effetto relativistico dell’aumento della loro massa). L’effetto di ciò è il moto di precessione del perielio (fenomeno previsto in Relatività Generale da Einstein nel 1919 ed osservato nel sistema solare per il pianeta Mercurio) che origina quel movimento a rosetta illustrato nella figura seguente.

Moto in un campo di forza centrale
Questa sistemazione rendeva conto del fatto che, in corrispondenza di una data linea (e quindi di una stessa energia) di uno spettro, ad un’osservazione più sofisticata, corrispondevano due o tre linee (quasi) sovrapposte. Ebbene la comparsa dei livelli con i sottolivelli alla stessa energia spiegava bene le osservazioni di doppietti e tripletti negli spettri. Mentre la correzione relativistica spiegava il sorgere di altre linee, quelle appunto di struttura fine.

Spettro con indicate (in modo esagerato) le separazioni delle linee (solo per qualcuna) per effetto relativistico. Si può vedere che in luogo della linea Hα della serie di Balmer vi sono ora ben sei linee che non sono visibili se non con una strumentazione avanzata.
E la sistemazione non era finita(9) perché vi era un altro fenomeno da dover prendere in considerazione e che veniva fuori, pur non ben compreso, da elaborazioni successive (1920) di Sommerfeld(10). Risultava che anche l’inclinazione delle orbite, rispetto ad un piano di riferimento, non poteva essere qualunque ma ubbidire ad un’altra quantizzazione di tipo spaziale. Questo risultato

era teorico e mancavano riscontri sperimentali per cui fu inizialmente lasciato da parte. Solo più tardi, con le esperienze di Otto Stern (1888-1969) e Walther Gerlach (1889-1979), l’elaborazione teorica risulterà confermata (questo numero quantico è chiamato numero quantico magnetico e si indica con m. Essopuò assumere tutti i valori interi seguenti m = 0, ±1, ±2, … , ± ℓ ).
VERIFICHE SPERIMENTALI: FRANCK ED HERTZ; STERN E GERLACH
La prima verifica sperimentale relativa all’atomo di Bohr fu realizzata dai due fisici tedeschi James Franck (1882-1964) e Gustav Hertz (1887-1975) in varie esperienze a partire dal 1911 fino a quella decisiva del 1914(11).
Franck ed Hertz, inizialmente, si muovevano non per verificare la correttezza delle ipotesi di Bohr ma di quelle di Johannes Stark (1874-1957) che nel 1908 aveva avanzato l’ipotesi che le righe dello spettro fossero causate dalla ionizzazione provocata da un potenziale V = hν(12). Alla fine, però, la loro esperienza andò a sostegno delle ipotesi di Bohr.
Nella loro esperienza i due utilizzarono un particolare tubo in cui un filamento di platino scaldato ad elevata temperatura emetteva elettroni, successivamente accelerati con opportune differenze di potenziale V e fatti collidere con bersagli costituiti da atomi di gas e di vapori.
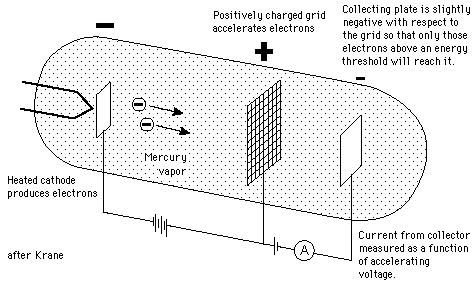
Aumentando V la corrente di elettroni che arriva all’anodo aumenta di conseguenza ma fino ad un certo valore massimo, dopo di ché si abbassa bruscamente. Aumentando ancora V si arriva ad un nuovo massimo per la corrente di elettroni, dopo di ché vi è ancora una brusca discesa. Si può seguire con lo stesso sistema e si hanno sempre i medesimi effetti.
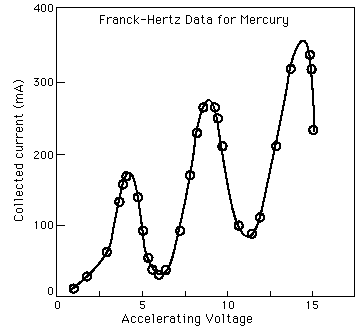
Franck ed Hertz interpretarono il fenomeno come una prova della correttezza di quanto sosteneva Stark: raggiunta l’energia di ionizzazione, gli elettroni, gli elettroni trasferiscono tutta la loro energia agli elettroni dell’atomo, determinando la conseguente caduta della corrente all’anodo. L’interpretazione di Bohr nel 1915 fu differente ed andò nel senso che quell’esperienza mostrava la correttezza delle sue ipotesi: gli elettroni accelerati non provocavano ionizzazione ma eccitavano gli atomi del catodo dal loro stato fondamentale ad uno stato eccitato. Se mediante urti di elettroni si fornisce energia ad un atomo, esso può solo ammettere quelle energie che corrispondono ad un salto quantico. E’ perciò che bombardando l’atomo con elettroni a bassa energia, minore cioè alla prima energia di eccitazione di un atomo, non si avrà alcun acquisto di energia da parte dell’atomo (a parte ciò che conosciamo come energia cinetica che diventa energia termica). Se però l’energia trasportata dagli elettroni che urtano è maggiore o uguale al primo salto quantico (mantenendosi però inferiore al secondo), allora l’atomo acquisterà energia con transizione di elettroni dal livello fondamentale al primo livello di eccitazione (e questo corrisponde al primo picco dell’esperienza di Franck ed Hertz ma anche alla prima linea della serie spettrale. Questo ragionamento si può ripetere per picchi e linee successive. E, in accordo con quanto la teoria di Bohr sosteneva, il salto energetico da un’orbita ad una più elevata prevede l’emissione di quanti di luce (che sono poi le linee spettrali in emissione).
Una verifica sperimentale diversa, di un fenomeno cioè che si accompagna all’ammissione di quantizzazione dell’atomo, e mi riferisco alla verifica dell’esistenza del quanto magnetico predetto da Sommerfeld, fu fatta come accennato da Stern e Gerlach tra il 1921 ed il 1922(13).
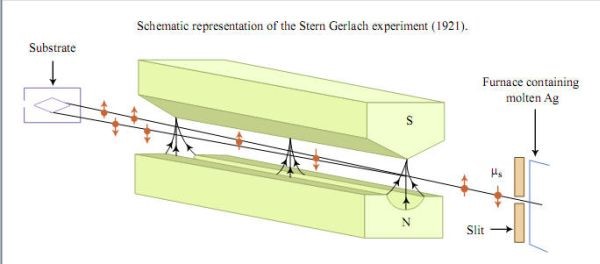
Un fascio di atomi di argento veniva prodotto in una fornace ad elevata temperatura. Dopo essere passati attraverso una fenditura, tali atomi attraversavano un campo magnetico non omogeneo ed andavano a finire su uno schermo che permetteva di fotografare le tracce qui lasciate. L’esperienza è semplice concettualmente ma difficilissima e costosissima da realizzare. Si trattava di verificare sullo schermo se, sotto l’azione del campo magnetico H, vi erano deflessioni continue degli atomi (sullo schermo sarebbe apparsa una striscia uniforme) o solo alcune deflessioni finite da imputare alla quantizzazione (sullo schermo sarebbero apparse alcune tracce separate, ognuna relativa alla quantizzazione spaziale del gruppo di atomi che la componeva). L’atomo con momento magnetico è come un piccolissimo magnete con dimensioni comunque finite. Se sistemiamo questo magnete elementare in un campo magnetico omogeneo, si muoverà secondo una linea retta dentro il campo. Ma se il campo non è omogeneo, le forze che agiscono sui due poli del magnetino non sono le stesse, come nel caso precedente, ed accelerano il magnete elementare o nel verso del campo o in quello opposto con la conseguenza che la sua traiettoria non sarà più rettilinea ed ogni singolo atomo subirà una deviazione proporzionale all’intensità e direzione del suo momento magnetico. Queste tracce si possono rendere visibili su uno schermo. Se vale la teoria classica il fascio di elettroni che arriva sullo schermo deve risultare ampliato, visto che i momenti magnetici degli atomi che fluiscono nel campo magnetico possono assumere tutte le direzioni rispetto al campo medesimo. Ma se vale la quantizzazione spaziale, non sono possibili tutte le posizioni ma solo un certo numero discreto di esse. Il fascio sullo schermo deve quindi scomporsi in un numero finito di fasci discreti determinato dal numero quantico magnetico (un numero diverso per atomi di differenti elementi). I risultati trovati furono quelli rappresentati nelle seguenti prime due due fotografie (la terza essendo stata costruita per far vedere cosa si sarebbe visto nel caso di validità dell’ipotesi classica):
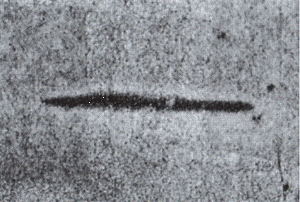
Fascio di elettroni in assenza di campo magnetico esterno.

Fascio di elettroni che ha attraversato un campo magnetico non omogeneo nell’ipotesi quantistica.

Fascio di elettroni che ha attraversato un campo magnetico non omogeneo nell’ipotesi classica.
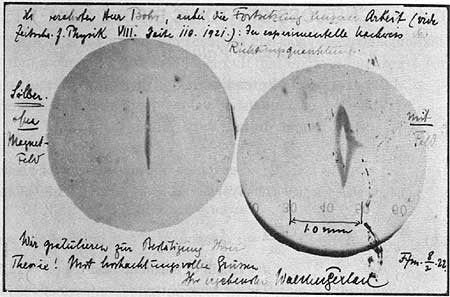
Cartolina che Gerlach inviò a Bohr facendogli i complimenti per la correttezza della sua teoria. Fra l’altro si dice: E’ qui riportata la prova sperimentale della quantizzazione spaziale. Questo è un risultato sorprendente. Senza campo magnetico non c’è splitting. Se c’è campo magnetico c’è splitting. Il momento magnetico è quantizzato.
RUTHERFORD SCOPRE IL PROTONE
Rutherford, nel 1911, aveva capito che all’interno di un atomo deve esservi una carica positiva concentrata che poi assunse il nome di nucleo. Ma di tale nucleo si sapeva molto poco. Che lì era concentrata tutta la massa atomica e che era dotato di carica positiva come le particelle α che già Rutherforda aveva capito essere dei nuclei di elio. Sempre impegnato con le sue ricerche di avanguardia, Rutherford proseguiva indagando sullo scattering delle particelle α con la materia e, nel 1919, fece quest’altra fondamentale scoperta. Questa volta l’apparato sperimentale era quello mostrato in figura.

Siamo durante la Prima Guerra Mondiale e Mardsen, il collaboratore ed amico di Rutherford era tornato in Australia. Prima di andarsene, nel 1917, nell’eseguire esperienze di bombardamento di aria con particelle α, notò che si originavano particelle che avevano un percorso particolarmente lungo, maggiore di quello delle particelle α stesse, ed in apparente contrasto con la conservazione dell’energia. Una delle possibilità era che queste particelle fossero nuclei di idrogeno perché presentavano la stessa fenomenologia di quando si bombardava direttamente idrogeno con particelle α. E’ qui che intervenne un Rutherford privo di collaboratori a causa della guerra. Egli con estrema pazienza si mise ad indagare la natura di quelle particelle soprattutto per quel fino ad allora trascurato ed apparente contrasto con la conservazione dell’energia. Nel giugno del 1919 pubblicò la memoria(14) in 4 parti, Urti di particelle α con atomi leggeri, che raccontava la sua scoperta. Egli iniziò con lo stabilire che le particelle con così lunghe traiettorie erano originate dal bombardamento con raggi α degli atomi di azoto presenti nell’aria. Rutherford spiegò il fenomeno introducendo la legge del decadimento radioattivo: gli atomi di azoto decadono con emissione di energia: Dobbiamo concludere che l’atomo di azoto si disintegra sotto l’azione delle violente forze prodotte in un urto con una particella alfa veloce e che l’atomo di idrogeno [atomo H] che viene liberato era parte costituente del nucleo d’azoto. E’ il riconoscimento dell’esistenza della disintegrazione nucleare del fatto che è possibile passare da un elemento ad un altro intervenendo sui nuclei degli atomi. E questo fatto è davvero strabiliante. Ma dietro il risultato più eclatante ve ne è un altro. Riporto la descrizione dell’esperienza che fa Bellone:
Nella prima memoria Rutherford esaminava il caso in cui l’idrogeno era bombardato da proiettili α emessi da una sorgente di radio C collocata in D nella figura. Il gas era introdotto nella scatola A (un contenitore a sezione rettangolare, con dimensioni pari a 18 cm di lunghezza e 6 cm e 2 cm in sezione) e si operavano conteggi su uno schermo F, dopo aver inserito tra lo schermo e il foro S una lamina metallica capace di assorbire le particelle α. All’esterno si sistemava infine un campo magnetico abbastanza intenso da far subire forti deflessioni alla radiazione β che, altrimenti, avrebbe prodotto troppa luminosità sullo schermo impedendo un efficace conteggio degli eventi da controllare.
I conteggi rivelavano immediatamente una situazione anomala, poiché si registrava un numero di scintillazioni dovute ad «atomi H» superiore a quello che la teoria esistente prevedeva. Si trattava allora di ricavare maggiori informazioni e di misurare la massa e la velocità degli oggetti messi in moto dai proiettili α. Nella seconda memoria Rutherford esponeva i risultati ottenuti facendo sì che un fascio di «atomi H» passasse attraverso un campo magnetico noto. Confrontando i dati con quelli relativi ad un fascio di particelle α, si aveva che gli «atomi H» dovevano essere considerati come oggetti che trasportavano una carica positiva, con un rapporto e/m conforme a quello che ci si doveva attendere se gli oggetti in questione erano proprio «atomi d’idrogeno con una carica positiva» elementare. Nella terza memoria si analizzavano gli effetti provocati da collisioni tra particelle α e atomi di ossigeno e di azoto, e, nella quarta, si giungeva alla conclusione che i prodotti della collisione tra particelle α e 1’azoto «non sono atomi d’azoto ma, probabilmente, atomi d’idrogeno, oppure atomi con massa 2. Se questo fosse il caso, allora dovremmo concludere che l’atomo d’azoto si disintegra per le intense forze che si sviluppano in una collisione ravvicinata con una veloce particella α, e che l’atomo di idrogeno che si libera formava una parte costituente del nucleo dell’azoto». E ciò faceva sperare che per mezzo di proiettili molto veloci – corpuscoli a o altri corpuscoli – diventasse possibile frantumare la struttura nucleare di altri atomi leggeri.
In pochi mesi di sperimentazione, Rutherford ottenne dati sulla produzione di «atomi H» per collisione tra α e altri atomi leggeri, quali il boro, il fluoro, il sodio e l’alluminio, e, in un articolo scritto insieme a James Chadwick (1891-1974) nel 1921, suggerì che nell’atomo, attorno ad un «nucleo centrale», ruotassero dei «satelliti» identificabili come «nuclei H»(15).
Il nuovo oggetto scoperto da Rutherford, il nucleo dell’atomo di idrogeno, che egli stesso, alla riunione annuale della British Association che nel 1920 si tenne a Cardiff, suggerì di chiamare protone, faceva ovviamente sorgere una classe di problemi di difficile enunciazione. Già nella Bakerian Lecture del 1920 Rutherford aveva anche ipotizzato l’esistenza di una microstruttura con carica elettrica zero. Essa, vista come particella, era intesa come un «nucleo neutro», formato da un protone strettamente unito ad un elettrone e battezzato con il nome di neutrone. Un neutrone, ad esempio, non essendo portatore di carica elettrica, avrebbe potuto con grande facilità penetrare in un nucleo pesante. Era ragionevole, comunque, cercare una simile particella servendosi di apparati di laboratorio come i tubi di scarica, nei quali si avevano grandi quantità di «nuclei d’idrogeno» e di elettroni, e dove, di conseguenza, era probabile che un protone acquistasse un elettrone strettamente legato e si trasformasse in un neutrone ad alta velocità. Muovendosi lungo le linee di ragionamento su indicate, nel 1921 J.L. Glasson pubblicava i risultati negativi di una ricerca dell’ipotetico neutrone(16): un intero decennio avrebbe dovuto trascorrere prima che, nel 1932, Chadwick potesse dare alle stampe un memorabile articolo intitolato The existence of a neutron, e, in quel decennio, moltissime cose dovevano però accadere, sia sul piano teorico, sia su quello sperimentale.
BOHR E IL PRINCIPIO DI CORRISPONDENZA
Abbiamo visto che le due condizioni di Bohr sono tra loro in contraddizione. Come può fare un grande fisico, un fisico veramente grande, ad assumerle senza il terrore di rovinare la sua reputazione per tutta la vita ? Occorre che costui sia proprio grande come le premesse e sia convinto delle cose che sostiene in modo quasi fideistico. Oppure si può fare una sorta di compromesso nell’ammettere gradualmente senza tagliar ei ponti con le cose che si dovrebbero abbandonare. Segrè ci avvicina in questo modo alle problematiche che dovevano essere al fondo di ciò che Bohr faceva e ci dice ciò che Einstein, un grande intenditore di azzardi, diceva di lui, della follia delle sue ipotesi:
«Che queste basi mal sicure e contraddittorie bastassero a un uomo coll’istinto e acutezza unici di Bohr, a scoprire le leggi fondamentali delle righe spettrali, delle orbite elettroniche negli atomi e perfino la loro importanza per la chimica, mi sembrò allora un miraacolo e tale mi sembra ancor oggi».
Lo stesso Bohr diceva del suo modo di operare quanto segue e ci spiega bene come stanno le cose:
«Assumeremo che le condizioni da usare per stabilire le energie negli stati stazionari siano tali che le frequenze ν, al limite quando il moto in stati stazionari successivi differisce molto poco, tenda a coincidere colle frequenze che sono da attendersi in base alla teoria classica ordinaria per il moto in queste orbite stazionarie».
Bohr ha quindi detto che occorre passare in modo graduale, con continuità, attraverso casi limite, dai casi classici a quelli quantistici. Ha cioè detto che occorre muoversi con circospezione e che il suo modo di operare non voleva essere distruttivo di ciò che c’era prima ma solo un modo per far capire come passare dal macroscopico al microscopico per piccoli passi. E’ un modo, dice Segrè, di rappresentare il principio di corrispondenza dovuto a Bohr, principio che non è formulabile in modo rigoroso ma solo per esempi come questo. Esso compare per la prima volta nella trilogia di Bohr Sulla teoria quantistica degli spettridi righe del 1918(17) pubblicato nelle Memorie dell’Accademia Danese. Cerco di dire qualcosa in più.
Di fronte ai dati dell’esperienza, le leggi della fisica classica hanno saputo far fronte in modo brillante a tutte le questioni relative al moto ed ai processi che lo vedono interessato sia macroscopici che microscopici. Quest’ultimo aggettivo deve essere pensato in relazione alla teoria cinetica. Se ora si introduce una nuova meccanica occorre dare per buono il fatto che essa dovrà almeno dare gli stessi risultati della vecchia. Si deve quindi esigere da essa che, nei casi limite di grandi masse e di orbite di grandi dimensioni, la nuova meccanica divenga la vecchia.
Sull’argomento vi è una stimolante discussione di Tagliaferri della quale riporto la parte introduttiva:
Affinché la teoria quantistica – così arbitraria nei suoi fondamenti – non fosse incompatibile con l’ormai codificata rappresentazione di tanta «realtà» sperimentale, bisognava dunque che essa in riconosciuti casi limite conducesse a risultati eguali a quelli dedotti o deducibili con i procedimenti non quantistici. […]
Fino al 1917 il ragionamento della corrispondenza era di fatto un’applicazione di analisi matematica, che come tale non richiedeva nuove assunzioni fisiche. Ma le novità del 1916-17, ossia la quantizzazione delle strutture atomiche in tre dimensioni, l’introduzione della meccanica hamiltoniana per trattare i sistemi molteplicemente periodici, la concezione delle probabilità di transizione tra stati stazionari, allargarono in breve tempo gli orizzonti della quantistica. Bohr reagì prontamente: sviluppò il ragionamento della corrispondenza (sia pure sacrificandone in parte il rigore matematico) in un procedimento euristico di vasta portata, che in seguito si meritò con buon diritto la qualifica di «principio». Così esso si affiancò a quello dell’invarianza adiabatica nella funzione di fornire criteri di guida all’empirico avanzamento della vecchia teoria dei quanti.
Mentre infatti il principio di invarianza adiabatica assicurò l’applicabilità formale della meccanica ordinaria alla teoria dei quanti nei problemi relativi alla determinazione degli stati stazionari, quello di «corrispondenza» assolse analoga funzione nei riguardi della determinazione delle caratteristiche della radiazione emessa nelle transizioni tra stati stazionari (in particolare, per l’avvio a soluzione del problema delle intensità delle righe spettroscopiche). Sebbene – giova ripeterlo – il principio di corrispondenza abbia avuto solo un carattere formale, la sua importanza sia pratica che concettuale è stata profonda nella vecchia teoria dei quanti; inoltre esso ha contribuito in maniera decisiva alla fondazione della meccanica quantistica.

Bohr con Einstein nel 1927
IL SEGUITO …
Non c’è seguito che io possa trattare compiutamente arrivato a questo punto. Avrete notato come la storia si infittisce e si intreccia a molteplici attori, molti dei quali ho tra l’altro trascurato. Inoltre nascono complicazioni matematiche notevoli che non mi permettono più di essere abbastanza discorsivo. Diventa estremamente complesso seguire tutti gli infiniti rivoli di tale storia almeno a partire dagli anni Venti del Novecento.

Il 6° Congresso Solvay del 1930. Vi sono: (in prima fila da sinistra a destra) Théophile de Donder, Pieter Zeeman, Pierre Ernest Weiss, Arnold Sommerfeld, Marie Curie, Paul Langevin, Albert Einstein, Owen Willans Richardson, Blas Cabrera, Niels Bohr, Wander Johannes de Haas. (In piedi, da sinistra a destra) Edouard Herzen, Émile Henriot, Jules Émile Verschaffelt, Charles Manneback, A. Cotton, J. Errera, Otto Stern, Auguste Piccard, Walther Gerlach, Charles Galton Darwin, Paul Dirac, E. Bauer, Pyotr Leonidovich Kapitsa, Léon Brillouin, Hendrik Anthony Kramers, Peter Debye, Wolfgang Pauli, J. Dorfman, John Hasbrouck van Vleck, Enrico Fermi, Werner Heisenberg.

Bohr, in primo piano con delle carte nella mano, al fianco di Guglielmo Marconi che è a sua volta a fianco di Maria Curie, a Roma, al congresso di fisica nucleare del 1931.

Bohr con Marconi
Per ciò che riguarda Bohr, egli avrà una brillantissima carriera e farà ancora moltissimi lavori. Nel 1916 gli sarà data la cattedra di Fisica Teorica all’Università di Copenhagen. Nel 1918, come accennato, esce la prima parte della trilogia Sulla teoria quantistica della radiazione. Nel 1922 esce un suo articolo sulla teoria del sistema periodico degli elementi e, nello stesso anno, riceve il premio Nobel per la fisica. Nel 1924 è uno dei coautori (insieme a Kramers e Slater) della proposta nota come BKS, una sorta di programma di lavoro in fisica quantistica. Nel 1927, a settembre, è uno tra gli eminenti fisici al Congresso di Como dove presenta la prima formulazione del Principio di Complementarità. E’ obbligatorio notare come la fisica torni in Italia grazie al lavoro di Enrico Fermi e della Scuola di Roma. A novembre del 1927 vi è il 5° Congresso Solvay dove inizia uno scontro memorabile con Einstein sui fondamenti della Meccanica Quantistica e sul significato da dare ad essa. Einstein sarà perdente e si taglierà per sempre il filo che doveva legare fisica e filosofia. Nel 1933 affronta con Rosenfeld il problema della misura in Elettrodinamica quantistica. Nel 1933 vi è un altro suo lavoro fondamentale che ci ricorda un poco i suoi esordi in idrodinamica; propone il modello a goccia per il nucleo atomico. Nel 1940 siamo tragicamente di nuovo in guerra e l’esercito di Hitler invade la Danimarca. Bohr inizia una fuga che lo porterà prima in Svezia, quindi in Inghilterra ed infine negli Stati Uniti. L’ascesa di Hitler in Germania ha significato (tra l’altro) la totale distruzione della più grande concentrazione mai avuta al mondo di fisici di livello eccelso, quella tedesca, con la simultanea nascita del dominio scientifico nordamericano che metteranno su, anche se provvisoriamente un’analoga concentrazione di cervelli a Los Alamos.

Niels Bohr con Enrico Fermi a Los Alamos
Sulla fuga di Bohr verso gli USA vi è qualcosa da raccontare.
Tramite gli scienziati che conosceva molto bene, alcuni suoi amici come Frisch e Lise Meitner, ed un articolo apparso su Nature nel febbraio del 1939, Bohr venne a sapere di una reazione nucleare, chiamata fissione, realizzata in Germania da Otto Hahn e Fritz Strassman. La caratteristica principale di tale reazione era la liberazione di un’enorme quantità di energia. Lo stesso Hahn usava per descriverla il temine zerplatzen (esplosione). Jungk racconta che quando Frisch, di ritorno dalla Svezia dove aveva avuto scambi d’idee con Lise Meitner, ne parlò con Bohr a Copenhagen, questi si colpì la fronte ed esclamò: “Come abbiamo potuto non rendercene conto per tanto tempo ?“. E da allora iniziò una sorta di incubo per tutti gli scienziati atomici antifascisti che comprendevano cosa accadeva e cosa sarebbe potuto accadere. Sotto questa spinta di terrore fu coinvolto anche Einstein che scrisse la famosa lettera a Roosevelt della quale si pentì molto amaramente per l’uso che gli americani fecero della bomba. Per parte sua Bohr cercò di saperne il più possibile. Ebbe un incontro con Heisenberg nel quale tentò di capire se gli scienziati restati in Germania avrebbero collaborato a portare avanti le ricerche sulla fissione. Heisenberg non disse né si né no ma che se il governo avesse voluto, sarebbe bastato solo un poco di impegno … Ciò lo spaventò e gli fece perdere la fiducia sui colleghi restati in Germania. I tedeschi sequestrarono tutto l’uranio dei laboratori di ricerca, anche a Copenhagen. Bohr riuscì ad avere una bottiglia di acqua pesante, un materiale da utilizzare in processi atomici, che proveniva da alcuni laboratori che i tedeschi avevano messo su in Norvegia. Quando partì verso gli USA portò con sé questa bottiglia. Ma seguiamo quanto racconta Jungk sul Bohr in territorio nordamericano.
Particolarmente difficile fu per Niels Bohr attenersi alle norme dell’osservanza del segreto. Da quando era fuggito dalla Danimarca, veniva trattato non più come un essere umano ma come una preziosissima arma segreta, che in nessun modo doveva cadere nelle mani del nemico. Già sul « Mosquito » che lo portò a volo oltre il Mar del Nord, quel «carico» così pericolosamente intelligente fu sistemato proprio sull’orlo dello sportello da cui si sganciavano le bombe, per poterlo – e immediatamente in caso di attacco tedesco – far cadere in acqua con una spinta. Quella volta Bohr arrivò a Londra più morto che vivo, giacché, tutto concentrato nello sforzo fisico, aveva dimenticato il consiglio del pilota di mettersi la maschera dell’ossigeno, e così ad alta quota era svenuto.
Quando Bohr atterrò a New York in compagnia di suo figlio Aage, due funzionari del servizio segreto inglese gli si misero alle calcagna. All’insaputa di questi sorveglianti, altri due agenti speciali del Manhattan Project presero Bohr sotto la loro sorveglianza, e per colmo dei colmi lo seguivano ancora due detectives dell’Fbi americano. Niels Bohr, l’amico della libertà e della franchezza, non gradiva affatto questa sorveglianza ad opera di una mezza dozzina di cerberi, e cercava di sottrarvisi ogni volta che poteva. Ed effettivamente non era un compito facile tenerlo sott’occhio senza farsi notare, poiché egli attraversava sempre le strade di New York nei punti in cui il passaggio era vietato ai pedoni, costringendo così ben sei tutori della legge a peccare assieme a lui contro le norme del traffico.
Bohr non riusciva ad abituarsi, ora che era negli Usa, ad esser chiamato «Nicholaus Baker» per motivi di sicurezza. Un giorno, i funzionari che lo sorvegliavano lo avevano ancora una volta ammonito in proposito, quand’ecco che sull’ascensore di un grattacielo egli incontrò la moglie del suo vecchio collega von Halban, che però nel frattempo – cosa che lui non sapeva – aveva divorziato. «Lei non è la signora von Halban? » domandò ossequiosamente. Al che arrivò secca la risposta: «Lei si sbaglia, io ora mi chiamo Placzek ». Poi la signora si voltò, ed esclamò sorpresa: «Ma Lei è il professor Bohr». Al che Bohr, portando un dito alla bocca, rispose sorridendo: «Lei si sbaglia, io ora mi chiamo Baker».
Quando Bohr arrivò per la prima volta a Las Alamos, Groves, che lo accompagnava, lo aveva già istruito in treno per ben dodici ore su tutto ciò che da quel momento avrebbe potuto e non avrebbe potuto dire. Bohr non aveva fatto che annuire col capo. Ma Groves ancora una volta restò deluso. «Cinque minuti dopo il suo arrivo, Bohr raccontò tutto quello che mi aveva appena promesso di non dire», riferì il generale qualche anno dopo su questa gemma della sua collezione di crackpots.
Solo nel 1947 Bohr tornerà in Danimarca. Nel 1952 sarà il primo direttore del gruppo teorico del CERN che nasce sotto l’impulso fondamentale di Auger ed Amaldi. Si spense nel novembre del 1962.

Bohr con Einstein
NOTE
(1) Poincarè, invece, in una lettera immediatamente posteriore al Congresso, ebbe a scrivere di Einstein (mostrando quanto dicevo qualche riga più su nel testo, cioè che si era convertito):
Einstein è uno dei pensatori più originali ch’io abbia mai conosciuto. Nonostante la sua gioventù, ha già raggiunto un posto onorevole tra i massimi scienziati d’oggi. In lui dobbiamo particolarmente ammirare la facilità con la quale si adatta a nuovi concetti, e sa dedurne le conclusioni. Egli non rimane legato ai principi classici, e quando gli si presenta un problema di fisica, ne considera rapidamente tutte le possibilità. Ciò porta subito nella sua mente alla predizione di nuovi fenomeni che potrebbero un giorno essere verificati dall’esperimento. Non intendo dire che tutte le sue previsioni supereranno la prova dell’esperienza, quando gli esperimenti si renderanno possibili. Poiché egli cerca in tutte le direzioni, ci si deve, all’opposto, aspettare che la maggioranza dei sentieri da lui seguiti risultino dei vicoli ciechi. Ma si deve sperare, al contempo, che una di queste direzioni da lui indicate possa essere quella giusta, e ciò sarebbe abbastanza. Questo è precisamente il modo in cui si dovrebbe procedere. Il ruolo del fisico matematico è quello di porre interrogativi e soltanto l’esperimento può rispondere a essi.
(2) R.A. Millikan, A new modification of the cloud method of determining the elementary electrical charge and the most probable value of that charge, Phys. Mag. XIX, 6 (1910), p. 209.
Ehrenhaft F., Über die Kleinsten Messbaren Elektrizitätsmengen, Phys. Zeit., 10(1910), p. 308.
R.A. Millikan, On the Elementary Electric charge and the Avagadro Constant, Phys. Rev. II, 2 (1913), p. 109.
(3) A. E. Haas, Jahrb. d. Rad. u. El., 7, p. 261 (1910).
(4) Nella nota 10 di pag. 295, Baracca, Russo e Ruffo dicono: Occorre notare qui che si tratta di una instabilità meccanica e non elettromagnetica, come di solito viene ripetuto. Si dice cioè che essendo gli elettroni che ruotano intorno al nucleo delle cariche elettriche accelerate, essi devono perdere energia per irraggiamento e quindi cadere rapidamente nel nucleo. In realtà, se intorno al nucleo ruotano molti elettroni si possono realizzare delle configurazioni per cui l’irraggiamento è trascurabile (si pensi al caso limite di una corrente continua circolante in un anello, la quale non irradia). L’equilibrio che si realizza è però instabile meccanicamente in quanto basta una piccola perturbazione del moto degli elettroni per distruggerlo in modo irreversibile. Ciò non avviene al contrario nel caso del modello «a panettone» [di Thomson] in quanto cambia la legge di forza che lega gli elettroni all’atomo (cfr. Heilbron, J.J. Thomson and the Bohr Atom, su Physics Today, Aprile 1977).
In realtà occorre tenere conto di ambedue gli effetti, sia quello elettrodinamico che quello meccanico.
(5) L’energia cinetica T = 1/2 mv2 dell’elettrone (di massa m) e la sua frequenza di rotazione ν sono legate dalla relazione T = kν, dove k è una costante; cioè mv2/ν = 2k. Se τ è il periodo di rotazione (τ = 1/ν), si ha allora mv(vτ) = 2k e, essendo ντ pari alla lunghezza r della circonferenza che costituisce l’orbita dell’elettrone si ha infine 2mrv = 2k. Se si confronta questa con la regola di quantizzazione per il livello fondamentale formulata da Bohr nella trilogia del 1913 (2 mrv = h) si conclude che k = 1/2 h.
(6) Niels Bohr, On the Constitution of Atoms and Molecules, Philosophical Magazine 26 (Series 6): pp. 1-25, 1913.
Niels Bohr, On the Constitution of Atoms and Molecules, Philosophical Magazine 26 (Series 6): p. 476, 1913.
Niels Bohr, On the Constitution of Atoms and Molecules, Philosophical Magazine 26 (Series 6): p. 857, 1913.
(7) A. Sommerfeld, Annalen der Physick, 51, p. 1, 1916. Cose analoghe, nello stesso tempo, erano state indipendentemente ricavate da William Wilson, Philosophical Magazine, 29, p. 795, 1915 e 31, p. 156, 1916.
(8) In somma sintesi, lo spazio delle fasi, in coordinate cartesiane, è uno spazio che ha su uno degli assi coordinati le quantità di moto q di un sistema in moto e sull’altro asse le coordinate spaziali dello stesso sistema. In coordinate qualunque, la definizione più generale di spazio delle fasi è quello spazio in cui si rappresenta il moto di un sistema. Tale spazio è formato dalle 2n coordinate generalizzate del sistema in studio (sistema di coordinate uguali al numero dei gradi di libertà del sistema) qn e dai momenti coniugati del medesimo sistema (o velocità generalizzate di esso) pi. Si tratta di un metodo matematico elaborato da Hamilton per rendere più semplice lo studio di sistemi complessi.
Riporto il disegno (uno dei pochi realizzabili perché in due dimensioni) dello spazio delle fasi per un semplice oscillatore armonico. Si tratta di ellissi che, se trattiamo l’oscillatore con i quanti e quindi con h, risultano quantizzate, ciascuna delle quali con area ∫pdq = nh.

In accordo con l’espressione per l’area ora data, l’area della prima ellisse è h, della seconda è 2h, della terza 3h, e così via. Ed anche l’area tra due ellissi consecutive è h. L’oscillatore quantizzato, che è rappresentato nel grafico con un punto, se acquist
a energia ed acquista un quanto di energia hν salta da una ellisse a quella superiore (e viceversa se perde energia). Avverto però che la traiettoria dell’oscillatore nello spazio delle fasi non deve essere confusa con una traiettoria ordinaria in uno spazio ordinario.
(9) La teoria di Bohr si può ulteriormente migliorare tenendo conto che quando si ha a che fare con un oggetto che ruota intorno ad un altro oggetto, bisogna considerare i due oggetti che ruotano intorno al loro centro di gravità. Ciò vuol dire che in qualche modo bisogna tener conto anche della massa del nucleo e, in definitiva, occorre sostituire ad m che compare nelle formule viste la cosiddetta massa. ridetta (m) data da:
dove M è la massa del nucleo.
(10) A. Sommerfeld, Annalen der Physick, 63, p. 221, 1920.
(11) J. Franck, G. Hertz, On the Excitation of the 2536 Å Mercury Resonance Line by Electron Collision, Verh. Dtsch. Ges. Berlin, 16, 457, 512, 1914. Osservo a parte che Gustav Hertz, premio Nobel per la fisica nel 1925, era il nipote del più famoso Heinrich Hertz.
(12) J. Stark, Phys. Zs., 9, pp. 85, 889, 1908.
(13) Walther Gerlach & Otto Stern, Das magnetische Moment des Silberatoms, Zeitschrift für Physik, 9, 353-355, 1922.
Otto Stern, Ein Weg zur experimentellen Pruefung der Richtungsquantelung im Magnetfeld, Zeitschr. f. Physik, 7, 249-253, 1921.
W. Gerlach, Zeitschr. f. Physik, 8, 110, 1921.
Walther Gerlach & Otto Stern, Der experimentelle Nachweis der Richtungsquantelung im Magnetfeld, Zeitschr. f. Physik, 9, 349-352, 1922.
(14) Ernest Rutherford, Collision of alpha Particles with Light Atoms; An Anomalous Effect in Nitrogen, Philosophical Magazine, 37, No. 222, pp. 537-87, 1919.
(15) J. Chadwick, E. Rutherford, The artificial disintegration of light elements, Nature, 107, p. 41, 10 marzo 1921.
J. Chadwick, E. Rutherford, Phil. Mag., 42, 809, 1921.
J. Chadwick, E. Rutherford, Phil. Mag., 44, 417, 1922.
(16) J.L. Glasson, Attempts to Detect the Presence of Neutrons in a Discharge Tube, Philosophical Magazine, Sixth Series, 42:596, 1921.
(17) Niels Bohr, On the quantum theory of line spectra, Voll. 1 e 2, København: Z.F. Host, 1918. La discussione del Principio di Corrispondenza è nella Parte I, Cap. 5, n. 3.
L’argomento fu poi ripreso nel 1920 in
Niels Bohr, Zeits. f. Phys., 2, p. 423.
(18) N. Bohr, H.A. Kramers, e J.C. Slater, Phil. Mag., 47, 785-802, 1924.
BIBLIOGRAFIA
(1) AA. VV. – Scienziati e Tecnologi dalle origini al 1875 – EST Mondadori 1975
(2) Emilio Segrè – Personaggi e scoperte nella fisica contemporanea – EST Mondadori 1983
(3) E. Whittaker – A History of Theories of Aether and Electicity – Nelson and Sons 1952
(4) Articoli di Enrico Bellone in: Paolo Rossi (diretta da) – Storia della scienza – UTET 1988
(5) Max Born – Atomic Physics – Blackie & Son, London 1962
(6) Max Born – La sintesi einsteniana – Boringhieri 1969
(7) Guido Tagliaferri – Storia della fisica quantistica – Franco Angeli 1985
(8) Mario Gliozzi – Storia della fisica – in: N. Abbagnano (diretta da) – Storia delle Scienze, UTET 1965
(9) René Taton (diretta da) – Storia generale delle scienze – Casini 1965
(10) John L. Heilbron – I dilemmi di Max Planck – Bollati Boringhieri 1988
(11) Piero Caldirola – Lezioni di fisica teorica – Viscontea, Milano, dopo 1950
(12) Samuel Tolansky – Introduzione alla fisica atomica – Boringhieri 1966
(13) Giuseppe Bruzzaniti – Dal segno al nucleo – Bollati Boringhieri 1993
(14) A. Baracca, S. Ruffo, A. Russo – Scienza e industria 1848 – 1915 – Laterza 1979
(15) Enrico Persico – Gli atomi e la loro energia – Zanichelli 1970
(16) Jean Perrin – Les atomes – Gallimard 1970
(17) D. ter Haar – The Old Quantum Theory – Pergamon Press 1967.
(18) Robert Jungk – Gli apprendisti stregoni. Storia degli scienziati atomici – Einaudi 1958.
(19) http://nobelprize.org/nobel_prizes/physics/laureates/1922/bohr-bio.html
(20) Banesh Hoffmann – Albert Einstein – Bompiani 1977
(21) Niels Bohr – Teoria dell’atomo e conoscenza umana – Boringhieri 1061.
(22) Giulio Peruzzi – Niels Bohr – I grandi della scienza, Le scienze n° 23, Novembre 2001.
Categorie:Senza categoria
Rispondi