di Roberto Renzetti
BECQUEREL SCOPRE LA RADIOATTIVITA’
Il 20 gennaio del 1896 i due medici Oudin e Barthélemy presentarono all’Accademia delle Scienze di Parigi le foto delle radiografie fatte da Röntgen ed il fisico matematico Henri Poincaré (1854-1912) discusse i primi dettagli dei lavori dello stesso Röntgen. Poincaré si soffermò particolarmente sul fatto che i raggi X nascevano nell’urto dei raggi catodici sulla parte terminale del tubo quella che diventa fluorescente con i raggi catodici. Egli avanzò una prima ipotesi che i due fenomeni, la fluorescenza e la creazione di raggi X in quella parte di vetro fossero tra loro collegati. Oggi sappiamo che questa ipotesi non era corretta ma essa stimolò il desiderio di fare ricerche in proposito.

Henri Poincaré
Tra i più interessati vi era un antico condiscepolo di Poincaré alla Scuola Politecnica di Parigi, socio dell’Accademia e professore di fisica presso il Museo di Storia Naturale, Henri Becquerel (1852-1908). In lui si fece subito strada il pensiero che discendeva dall’ipotesi fatta da Poincaré: è possibile che altre sostanze per il solo fatto di essere fluorescenti o fosforescenti abbiano la caratteristica di emettere raggi X o radiazioni simili ? La cosa aveva per lui grande interesse perché era figlio di Edmond Becquerel (1820-1891) che aveva dedicato la vita allo studio delle azioni chimiche della luce, della fluorescenza nei composti dell’uranio. E subito iniziò una ricerca in tali direzione, a partire da alcune sostanze che aveva in abbondanza nel suo laboratorio e cioè di alcuni composti del potassio e dell’uranio (uranile osolfato doppio di uranio e potassio).

Henri Becquerel
Nella prima esperienza che fece iniziò con l’originare la fosforescenza dell’uranile esponendone una quantità alla luce del sole ed accertandosi di ciò mediante una lastra fotografica. Espose quindi per 4 ore alla radiazione solare una lastra fotografica protetta con molta cura con spessi fogli di carta nera per evitare che fosse impressa dalla luce. Sopra questa lastra sistemò un frammento di uranile. La fosforescenza di questo materiale avrebbe dovuto impressionare la lastra fotografica. Passate le 4 ore ritirò il tutto e controllò la lastra fotografica che presentava impressionato il profilo del frammento che era stato sistemato su di essa sotto forma di una macchia scura. Era un immediato successo che sembrava mostrare la correttezza dell’ipotesi fatta: la fosforescenza di un dato materiale attraversava fogli di carta nera, non attraversati dalla luce, ed impressionava una lastra fotografica, proprio come i raggi X. Il 24 febbraio 1896 Becquerel annunciò la sua scoperta(1).
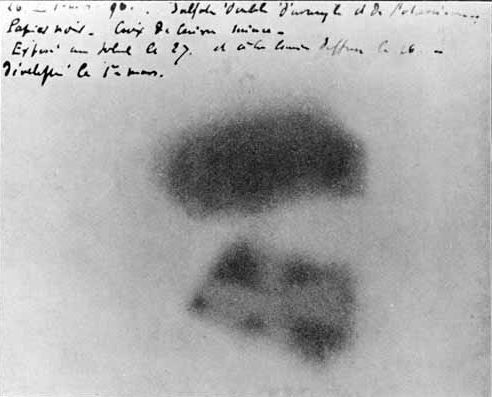
Una lastra fotografica impressionata dal minerale di uranio
L’idea era di fare altre esperienze per il 26 ed il 27 febbraio ma, poiché il cielo era coperto di nubi, rimandò i suoi lavori. Nel frattempo, dispose alcuni minerali di uranio che aveva sul tavolo da lavoro dentro un cassetto della sua scrivania, cassetto nel quale erano conservate anche le lastre fotografiche rigorosamente protette da involti di carta nera. Nel cassetto non entrava luce ed i minerali di uranio erano poggiati sulle lastre fotografiche. Quando finalmente ricomparve il sole, Becquerel estrasse le lastre ed il minerale di uranio per fare le sue esperienze. Ebbe cura di controllare lo stato delle lastre e le trovò rovinate, completamente inutilizzabili per le macchie scure che presentavano, simili a quelle disegnate nel primo esperimento. Eppure questo minerale di uranio non era stato esposto alla luce per provocarne la fosforescenza … Volle accertarsi che non vi fossero stati difetti di alcun tipo nella cura dei materiali e ripeté quanto accaduto come esperienza controllata. Sistemò un sale di uranio non esposto alla luce sopra una lastra fotografica protetta dalla luce e mise il tutto per qualche giorno dentro un recipiente buio. Il risultato fu molto chiaro: senza che si fosse prodotta fosforescenza o fluorescenza mediante luce, la lastra era impressionata con la silhouette del metallo che era stato sistemato su di essa. Una sola conclusione era possibile: quel materiale emetteva una qualche radiazione diversa da quella X(2). Più oltre, nello stesso anno, lo stesso Becquerel arrivò ad una conclusione di grande importanza: quella radiazione proviene dall’uranio indipendentemente dal suo stato di composizione chimica (ciò vuol dire che la radioattività è una proprietà atomica e non molecolare) ed essa è emessa con continuità. Maria Skłodowska Curie (1867-1934), nel suo Traité de radioactivité del 1910, così racconta le cose:
L’origine dei lavori di Becquerel si riallaccia alle ricerche perseguite fin dalla scoperta dei raggi Röntgen sugli effetti fotografici delle sostanze fosforescenti e fluorescenti.
I primi tubi produttori di raggi Röntgen erano dei tubi senza anticatodo metallico. La sorgente di raggi Röntgen si trovava nella parete di vetro colpita dai raggi catodici; al tempo stesso questa parete era vivamente fluorescente. Ci si poteva allora chiedere se l’emissione di raggi Röntgen non accompagnasse necessariamente la produzione della fluorescenza, qualunque fosse la causa di quest’ultima. Questa idea è stata annunciata fin dall’inizio da Henri Poincaré.
Poco tempo dopo diversi sperimentatori segnalarono la possibilità di ottenere delle impressioni fotografiche attraverso carta nera mediante solfuro di zinco fluorescente, solfuro di calcio esposto alla luce e blenda esagonale artificiale fluorescente. Le esperienze ora citate non hanno potuto essere riprodotte malgrado numerose prove fatte a tale scopo. Non si può quindi considerare affatto provato che il solfuro di zinco e il solfuro di calcio siano capaci di emettere, sotto l’azione della luce, delle radiazioni invisibili che attraversano la carta nera ed agiscono sulle lastre fotografiche.
A. Becquerel ha fatto delle esperienze analoghe sui sali di uranio, alcuni dei quali sono fluorescenti. Egli ottenne delle impressioni fotografiche attraverso carta nera con solfato doppio di uranile e di potassio. Becquerel credette all’inizio che questo sale, che è fluorescente, si comportasse come il solfuro di zinco ed il solfuro di calcio nelle esperienze che erano da poco state descritte al riguardo. Ma il seguito delle esperienze mostrò che il fenomeno osservato non era affatto legato alla fluorescenza. Non è necessario che il sale venga illuminato; per di più l’uranio e tutti i suoi composti, fluorescenti o meno, agiscono allo stesso modo, e l’uranio metallico è il più attivo. Becquerel trovò poi che i composti di uranio, posti nell’oscurità completa, continuano ad impressionare le lastre fotografiche attraverso la carta nera durante anni. Becquerel ammise che l’uranio ed i suoi composti emettessero dei raggi particolari: i raggi uranici.
Era la scoperta della radioattività che impegnò subito i fisici in tutti i laboratori del mondo con un susseguirsi frenetico di scoperte. Becquerel per parte sua continuò i suoi studi mostrando che i raggi uranici rendono conduttrice l’aria che sta intorno ad essi.
PRIME RICERCHE DEI CONIUGI CURIE
Nel 1898 la fisica chimica polacca Maria Skłodowska Curie con suo marito il fisico francese Pierre Curie (1856-1906) in Francia e Schmidt in Germania, incuriositi dall’ultimo fenomeno scoperto da Becquerel, si misero a studiare quegli strani fenomeni.

Strumento inizialmente utilizzato da Maria Curie per misurare la ionizzazione dell’aria prodotta dai raggi uranici. L’elettroscopio, caricato precedentemente, si scarica se tra i piatti di un condensatore poniamo una sostanza radioattiva che, ionizzando l’aria, la rende conduttrice. La scarica dell’elettroscopio è tanto più rapida quanto più intensa è la radiazione ionizzante.
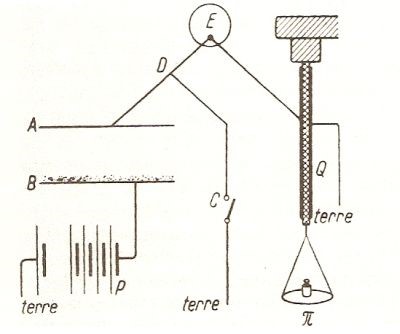
Strumento realizzato da Pierre Curie insieme al fratello Jacques per misurare correnti molto deboli. E’ simile al precedente ma qui si utilizza un sistema più perfezionato e preciso per misurare la corrente sviluppata dalla sostanza radioattiva disposta sul piatto B del condensatore alimentato da una batteria P di pile. Si tratta di un elettrometro a quarzo. L’elettrometro è quello indicato con E, π rappresenta i pesi disposti sul piattello, mentre Q è un quarzo piezoelettrico la cui fenomenologia era stata scoperta proprio dai fratelli Curie nel 1880 (in breve: alcuni cristalli, tra cui il quarzo, si deformano elasticamente se sottoposti ad un campo elettrico). Nelle esperienze di Curie le placche erano del diametro di 8 cm e distanti tra loro 3cm. Veniva utilizzata una tensione V di circa 100 volt che forniva una corrente I dell’ordine di 10-12A.

Pierre e Maria Curie nel loro laboratorio mentre usano l’elettrometro piezoelettrico.

L’elettrometro piezoelettrico dei Curie
Con uno elettrometro a quarzo piezoelettrico scoprirono che la radioattività è proporzionale alla quantità di uranio e non alla combinazione chimica in cui si trova. Fu proprio la sensibilità dello strumento che permise loro questa scoperta che eliminò molti errori in proposito tra cui anche quello iniziale di Rutherford che credeva essere più radioattivo l’uranio in polvere che quello solido. Nelle loro ricerche Pierre e Maria Curie trovarono che il torio ha le stesse proprietà dell’uranio (aprile 1898(3)). Tra il luglio ed il dicembre del 1898, ancora Maria e Pierre Curie riuscirono a separare dalla pechblenda (un minerale che contiene uranio) due nuovi elementi, ambedue radioattivi, il polonio (nome dato a questo elemento in onore del Paese natale di Maria Curie)(4) e (con Gustave Bémont)(5) il radio (poiché questo elemento aveva intense proprietà di emettere radiazioni, fu chiamato, da Maria Curie, radio). Per fare ciò analizzarono vari campioni di uranio trovando che alcuni erano molto più radioattivi di altri. A questo punto dovettero procedere a metodi di separazione ed analisi chimica del minerale di cui disponevano per osservare in quale parte di esso fosse concentrata la maggiore radioattività osservata (nasceva un nuovo campo di indagine che prende il nome di radiochimica).
Queste ricerche ne originarono moltissime altre a catena (chimica dei radioelementi) e molti altri elementi radioattivi vennero scoperti, tra i quali merita ricordare che A. Debierne nel 1899 riuscì ad isolare l’attinio. In poco tempo si scoprirono e si organizzarono provvisoriamente tre famiglie radioattive che riporto nella tabella seguente (nella quale vi sono riportate alcune proprietà che ancora non ho discusso ).
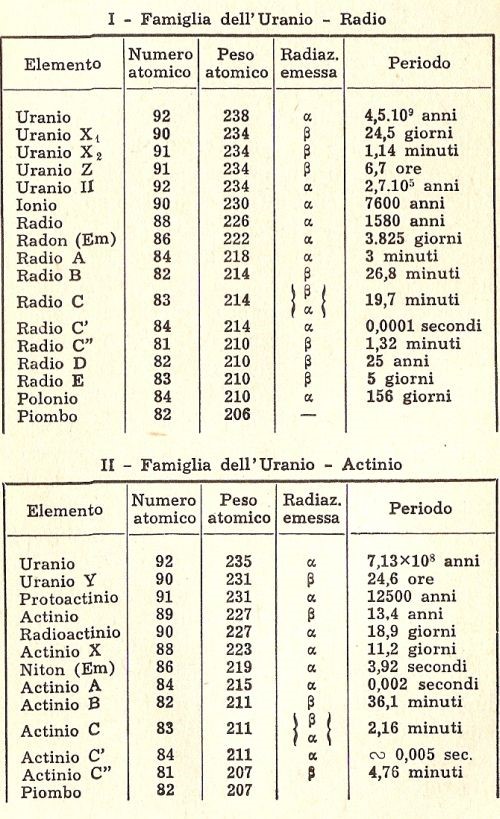
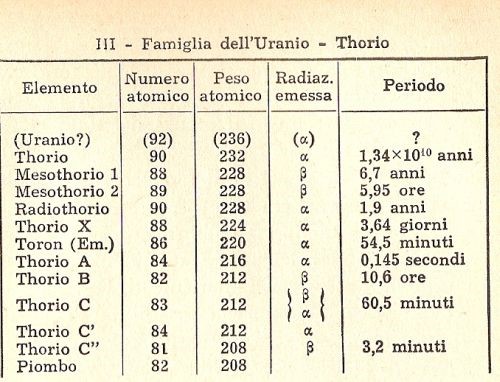
L’INTERVENTO DI RUTHERFORD
Dirigendo lo sguardo altrove, nei Laboratori Cavendish, diretti all’epoca da J.J. Thomson, il giovane fisico chimico Ernest Rutherford (1871-1937), arrivato dalla Nuova Zelanda, nel 1895, iniziò a studiare la radiazione di Becquerel. Nel 1898, quando già si era trasferito ad insegnare a Montreal, insieme ad Owens scoprì il thoron, un gas emesso dal torio (che oggi sappiamo essere un isotopo del radon). Nel 1899 scoprì che la radiazione di Becquerel era formata da due componenti con comportamenti differenti che egli chiamò raggi α (alfa) e raggi β (beta). La prima era assorbita da un foglio di carta o da una sottile foglia metallica mentre la seconda penetrava invece in spessori considerevolmente più grandi (ad esempio: poco meno di mezzo centimetro di alluminio)(6). In questa ricerca Rutherford si muoveva in analogia con quanto si faceva per scoprire la capacità di penetrazione dei raggi X cercando alcune caratteristiche della nuova radiazione. L’apparato utilizzato era del tipo che inizialmente usavano i coniugi Curie, con un buon elettrometro in luogo dell’elettroscopio, poiché Rutherford ancora non sapeva dell’esistenza dell’elettrometro a quarzo piezoelettrico. Egli misurava la

Vari strumenti di misura utilizzati da Rutherford
ionizzazione dell’aria di un materiale radioattivo disposto su una placca sistemando successivamente su di esso schermi di materiali diversi e di spessori diversi. In tal modo scoprì subito che la schermatura indeboliva la ionizzazione e cioè la radiazione. Ma veniva fuori qualcosa di inatteso che lo convinse che le radiazioni che studiava erano complesse. Quando disponeva infatti successive foglioline di alluminio con lo spessore di 0,0005 centimetri osservava che per i primi tre fogli l’intensità della radiazione diminuisce secondo l’usuale legge di assorbimento e che, dopo il quarto spessore, l’intensità della radiazione diminuisce di molto poco aggiungendo altri fogli. Rutherford commentava la cosa così: Questi esperimenti mostrano che la radiazione dell’uranio è complessa e che sono presenti almeno due tipi distinti di radiazione – un tipo che è assorbito con grande facilità e che per convenienza verrà chiamato radiazione α, ed un altro con carattere più penetrante che sarà chiamato radiazione β (e che sarà riconosciuto da Rutherford come una specie di raggi catodici). Egli tentò anche di fornire una legge empirica per l’assorbimento di radiazione che risultava di tipo esponenziale decrescente.
In questo periodo Rutherford si mise anche a ripensare allo strano comportamento del torio, studiato in precedenza con Owens ed a fare delle misure sulla sua radioattività(7). Vi fu un fatto casuale che spinse in avanti queste ricerche: l’apertura ed una chiusura di una porta del laboratorio che provocava uno spostamento d’aria che faceva diminuire la velocità di scarica dell’elettrometro che fungeva da strumento di misura. Rutherford si convinse che i fenomeni presentati dai composti del torio hanno una completa spiegazione se supponiamo che, oltre all’ordinaria radiazione, un gran numero di particelle radioattive vengono emesse dalla massa della sostanza attiva. Questa emanazione può passare attraverso spessori considerevoli di carta […] Questa emanazione diminuisce gradualmente il suo potere radioattivo. Studiando il comportamento di tale emanazione scoprì che essa durava solo un certo tempo: essa decadeva nel tempo secondo una legge esponenziale:
i(t) = I.e-λt
con i(t) che rappresentava la corrente misurata all’istante t, I la corrente iniziale e λ una costante.
Scriveva Rutherford che i composti del torio, sotto certe condizioni, hanno la capacità di produrre una radioattività temporanea in tutte le sostanze solide poste nei loro dintorni. Si tratta del fenomeno che successivamente (1900) sarà chiamato da Rutherford radioattività eccitata e che egli interpretò come la deposizione di particelle radioattive provenienti dai composti del torio.
Nello stesso periodo i coniugi Curie pubblicarono un lavoro(8) in cui veniva segnalata la proprietà del radio di provocare una radioattività temporanea nei corpi posti nelle sue vicinanze. Il fenomeno fu da loro chiamato «radioattività indotta». Questo fatto era significativo perché, quando E. Dorn scoprì che anche il radio aveva una sua emanazione, stabiliva un effetto analogo per differenti sostanze radioattive.
Nel 1899, Geiser, Becquerel, Meyer e Schweilder, mostrarono indipendentemente che i raggi beta, quella specie di raggi catodici, sono deflessi da un campo magnetico e quindi che sono composti da corpuscoli negativi. A questo proposito Kaufmann mostrò che il rapporto tra carica e massa per i raggi beta è approssimativamente lo stesso trovato per i raggi catodici.
La deviabilità dei raggi β ebbe molte conferme sperimentali in poco tempo. Lo fece Becquerel nel 1899 per i raggi emessi dal polonio e dal radio(9). Un poco più tardi anche Pierre Curie verificò la deviabilità aggiungendo che tale deviabilità era solo riferibile alla radiazione più penetrante del polonio del radio e cioè ai raggi β(10). Un mese dopo, ancora Becquerel, mostrava con esperienze fatte sia con campi elettrici che con campi magnetici che i raggi β erano costituiti da particelle che presentavano lo stesso rapporto carica-massa trovato da Thomson per l’elettrone(11).
Nel 1900 il fisico francese Paul Ulrich Villard (1860-1934) mostrò che vi è un terzo tipo di radiazione emessa dalle sostanze radioattive. Si tratta di raggi estremamente penetranti che non sono deflessi da campi magnetici. Sono simili ai raggi X ma con frequenza maggiore. Li chiamò raggi γ (gamma)(12).
Rutherford aveva nel frattempo iniziato una collaborazione con Frederick Soddy (1877-1956) e, tra il 1902 ed il 1903, i due ricercatori capirono le successive trasformazioni delle sostanze radioattive ed introdussero il concetto di decadimento(13). La prima cosa che venne accertata fu la natura atomica della radioattività. Conseguenza di ciò è che gli atomi delle sostanze radioattive perdendo un qualcosa non potevano essere stabili nel tempo e vi doveva essere una qualche legge, del tutto ignota, che regolava i fenomeni all’interno dell’atomo
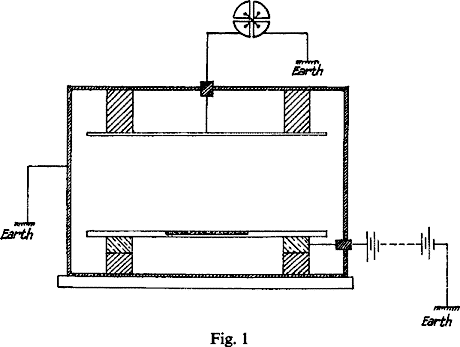
L’apparato sperimentale utilizzato da Rutherford e Soddy. Le due placche sono sistemate in un ambiente sotto vuoto. L’elettrometro è collegato alla placca superiore.
medesimo. Vi era poi la vicenda di raggi deviabili dai campi magnetici (le radiazioni β) e quelli non deviabili (la radiazione α) che complicava lo studio. Inoltre, se un atomo perde un qualcosa, questa perdita deve originare anche cambiamenti di natura chimica nelle sostanze radioattive, con processi del tutto diversi da quelli noti nella chimica ordinaria, e quindi si devono progressivamente avere nuovi tipi di materia. Nella loro memoria leggiamo:
Si mostra che la radioattività è accompagnata da mutazioni chimiche nelle quali vengono continuamente prodotti dei nuovi tipi di materia. Questi prodotti di reazione sono in un primo tempo radioattivi e la loro radioattività diminuisce regolarmente a partire dal momento della formazione. La continua produzione di essi mantiene la radioattività della materia che li genera ad un valore definito d’equilibrio. Si trae la conclusione che queste mutazioni chimiche debbono essere di carattere subatomico.
Trovarono poi che, separando dal torio (Th) un suo costituente radioattivo, il ThX, con le stesse caratteristiche del torio, si otteneva una strana situazione così descritta nella memoria:
Il costituente materiale che è responsabile della radioattività, una volta separato dal torio che lo produce, si comporta analogamente agli altri tipi di radioattività già citati. La sua attività decade geometricamente nel tempo e l’andamento del decadimento è indipendente dalle condizioni molecolari. La radioattività normale è tuttavia mantenuta ad un valore costante da un mutamento chimico che produce nuovo materiale radioattivo ad un ritmo che è ancora indipendente dalle suddette condizioni. L’energia necessaria per mantenere le radiazioni va valutata nell’ipotesi che l’energia del sistema dopo il mutamento sia minore ci quella precedente prima del mutamento stesso.
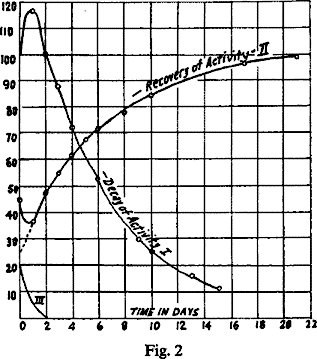
Ciò che osservavano Rutherford e Soddy. Mentre l’attività del ThX, estratto dal Th, decresce (decay of activity), la radioattività del Th, che aveva perso attività al momento dell’estrazione del ThX, la riconquista (recovery of activity), di modo che la somma delle due attività resta costante.
Fatte le misure, risultava che
l’attività del ThX diminuisce approssimativamente secondo una progressione geometrica al passare del tempo. Se I0 rappresenta l’attività iniziale ed It l’attività dopo il tempo t, si ha:
(1) It/I0 = e–lt ,
dove l è una costante ed e la base dei logaritmi naturali.
Mentre l’attività del torio, da cui era stato separato il ThX, passava da un minimo ad un massimo ed il suo valore può essere approssimativamente espresso dalla relazione:
(2) It/I0 = 1- e–lt
dove I0 rappresenta la quantità di radioattività recuperata quando si giunge al massimo ed It l’attività recuperata dopo il tempo t, con λ che è la stessa costante di prima [nota come costante di disintegrazione].
La memoria si concludeva con queste parole:
La radioattività è una nuova proprietà della materia capace di esatte determinazioni quantitative […] I risultati qui presentati mostrano che la radioattività può anche essere usata per ottenere cambiamenti chimici che avvengono nella materia.
Nel 1903 fu pubblicata una memoria(14) del solo Rutherford in cui intanto si osservava che la questione lasciata in sospeso della deviabilità o meno di alcuni raggi era legata solo all’intensità dei campi magnetici. Utilizzando infatti campi magnetici intensi anche le particelle α subivano deviazioni. Questa scoperta sgombrando il campo da interpretazioni che volevano tali particelle emesse da
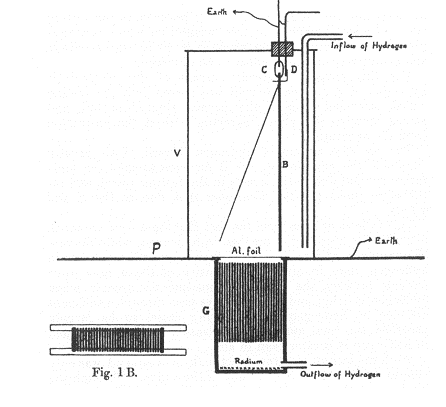
Apparato utilizzato da Rutherford per mostrare che anche le particelle α subivano deviazioni se i campi magnetici erano sufficientemente intensi. Le radiazioni provenienti da un sottile strato di radio passavano attraverso il sistema di fenditure realizzato disponendo, parallelamente l’una all’altra, un determinato numero di lastre d’ottone. Passando poi attraverso un sottile foglio di alluminio (spesso 0,00034 cm) entravano nella camera di ionizzazione V. La ionizzazione prodotta era misurata determinando la velocità di scarica dell’elettroscopio B. Il flusso di idrogeno, che dal recipiente V passava attraverso il foglio di alluminio poroso nel recipiente G, aveva un duplice scopo: per un verso serviva a portar via l’emanazione del radio, per l’altro verso serviva ad aumentare la corrente di ionizzazione dovuta ai raggi α e a diminuire quella dovuta ai raggi β e γ. Ciò era dovuto al fatto che i raggi α erano poco assorbiti dall’idrogeno rispetto all’aria, mentre i raggi β e γ producevano, in idrogeno, una quantità molto minore di ioni rispetto a quella prodotta in aria. L’esperienza, nelle sue linee generali, consisteva nel misurare la corrente di ionizzazione con e senza l’applicazione di un forte campo magnetico, perpendicolare al piano del disegno e parallelo al piano delle fenditure. La valutazione degli effetti di ionizzazione, non determinati dai raggi α, era eseguita ripetendo la stessa esperienza, quando la sorgente radioattiva era ricoperta da un foglio di mica in modo da assorbire tutte le radiazioni α.
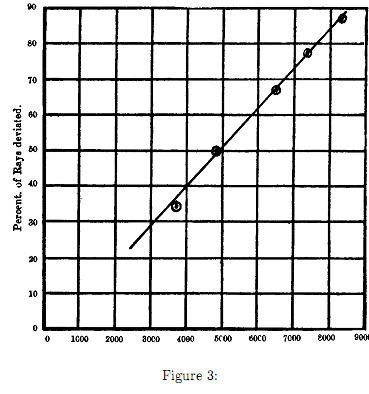
I risultati delle misure mostrano che la percentuale di raggi deviati (in ordinate) è approssimativamente proporzionale al campo applicato (in ascisse ed in unità CGS).
reazioni secondarie provocate dai raggi β, aprì la strada a conclusioni di notevole portata poiché si ebbe l’immediata deduzione che l’inizio della successione di mutamenti chimici nei corpi radioattivi è provocato dall’emissione di raggi α, e cioè dall’espulsione di una massa carica e pesante da parte dell’atomo. E questa deduzione ne comportava subito un’altra che metteva subito in gioco la struttura atomica: Il potere dei corpi radioattivi di espellere spontaneamente grandi masse con velocità enormi conforta l’opinione che gli atomi di queste sostanze siano costituiti, almeno in parte, da sistemi rotanti od oscillanti di corpi pesanti e carichi, grandi rispetto all’elettrone. L’improvvisa uscita di queste masse dalle loro orbite può essere dovuta all’azione di forze interne o esterne di cui oggi non abbiamo alcuna conoscenza. Ancora, a catena, Rutherford afferma, a fine memoria, che i corpi radioattivi, quando perdono particelle α devono diminuire di peso (come recentemente osservato da Heydweiler). In proposito scrivevano i due ricercatori: Arriviamo alla conclusione che la radioattività è insieme un fenomeno atomico ed un fenomeno che si accompagna al cambiamento della natura chimica delle sostanze in cui nuovi tipi di sostanze sono create […] L’idea universalmente accettata della stabilità dell’atomo chimico è basata solamente sulla conoscenza che abbiamo delle forze a nostra disposizione […] Non sembra irragionevole pensare che la radioattività ci possa fornire i mezzi per ottenere informazioni dei processi che avvengono all’interno dell’atomo chimico.
Come osserva Bellone, si profilava un’immagine della radioattività secondo la quale l’uranio ed il torio emettevano esclusivamente particelle α, mentre l’uranio X ed il torio X emettevano rispettivamente particelle β ed α + β. Di fronte a tante complicazioni pian piano si apriva qualche spiraglio, se non altro nel senso di suggerire ulteriori esperienze.
Nel 1903 Rutherford e Soddy pubblicarono un’altra memoria(15) che chiariva molti punti problematici restati in sospeso. Dopo aver studiato con precisione il comportamento della particelle α, passarono a misurarne alcune caratteristiche trovando che il rapporto della loro carica rispetto alla loro massa (q/m) aveva un valore che faceva pensare che la loro massa fosse dello stesso ordine di grandezza di quella dell’atomo di idrogeno. Oltre a ciò risultava che quasi tutto il fenomeno della radioattività dipendeva da esse che risultavano essere espulse per prime dai materiali radioattivi e solo successivamente seguite da particelle β. La conclusione più importante che trassero dai loro lavori sperimentali fu che alla luce di questa evidenza c’è ogni ragione per supporre che l’espulsione di una particella carica non accompagni semplicemente la mutazione, ma che questa espulsione sia la reale mutazione la responsabile cioè di cambiamenti chimici nella materia. E poiché la radioattività è una proprietà specifica dell’elemento, il sistema mutante deve essere l’atomo chimico e, poiché un solo sistema è implicato nella produzione di un nuovo sistema e di una particella pesante carica, nel mutamento radioattivo l’atomo chimico deve subire una disintegrazione. L’atomo chimico perdeva cioè parti che lo caratterizzavano come un dato elemento per renderlo d’altro tipo. Si perdevano prima delle particelle α e subito dopo delle particelle β. Ed il termine trasformazione, utilizzato dal 1902 e fino ad allora in modo non definito, acquisiva ora il significato preciso di disintegrazione, qualcosa all’interno di un atomo ancora tutto da definire si rompeva per originare nuovi elementi chimici.
A questo punto non restava che passare a dati quantitativi, partendo dalle questioni energetiche che si ponevano.
L’energia cinetica delle particelle α era calcolabile attraverso la relazione:
½ m v2 = ½ (m/e) e v2 = 5.1014 e ~ 10-5 erg
Tenendo conto che un grammo di radio conteneva intorno a 1020 atomi, esso emetteva una radiazione dell’ordine di 1015 erg o circa 2.107 grammocalorie. E questo per una sola emissione mentre si sapeva che vi erano almeno 5 successive fasi di emissione per cui era lecito valutare in circa 1010 grammocalorie l’energia irradiata da un grammo di radio nelle sue successive emissioni. Rutherford e Soddy concludevano affermando che l’energia latente nell’atomo deve essere enorme in confronto a quella che si libera nell’usuale mutamento chimico(16).
Poiché ogni fase di emissione durava un tempo tale da non permettere lo studio dell’eventuale elemento che si fosse formato, essa fu ribattezzata da Rutherford e Soddy metabolon.
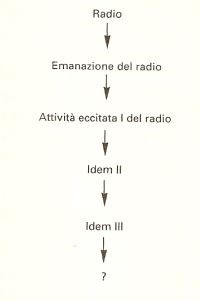
Il radio e le sue successive fasi di emissione, ciascuna delle quali chiamata metabolon.
Nella memoria compariva anche un esplicito riferimento alla formula oggi nota come decadimento radioattivo:
N(t) = N0.e -λt
dove N0 è il numero di atomi radioattivi inizialmente presenti, N(t) è il numero di atomi radioattivi presenti al tempo t e λ è la solita costante di disintegrazione. E questa legge può essere presentata in forma differenziale, dN = – λN.dt, scrivendo che il numero di atomi dN che si trasforma durante il tempo dt è proporzionale al numero N di atomi presenti. Viene quindi fuori quella regola di base per la radioattività: ogni atomo radioattivo ha una probabilità costante nel tempo di decadere in un tempo dt e tale probabilità dipende dalla sostanza considerata.
Le molte esperienze fatte mostravano una continua presenza di elio, sia se venivano riscaldate le sostanze radioattive, sia come gas proveniente dal bromuro di radio o dal radio medesimo. Inoltre la misura fatta del rapporto q/m per le particelle α mostrava un valore vicino a quello trovato per gli atomi di elio ionizzati. Questi dati convinsero Rutherford che le particelle α fossero atomi di elio ionizzati(17) (anche se ne mancava la prova definitiva)(18) ed a tal proposito è utile leggere il commento di Bellone:
La definizione del significato di «radiazione α» subiva così un complesso di ristrutturazioni la cui dinamica era condizionata dal rilevamento di dati empirici e da argomenti di prima approssimazione aventi lo scopo di stabilire valori numerici per grandezze quali e/m, v ed m. Nel volgere di pochi mesi le indagini di Rutherford avevano spostato i confini e le interne correlazioni dell’ area semantica del termine raggio α: da una forma di radiazione pensata in termini di forte assorbimento, di non deviabilità in campo elettromagnetico e di fenomenologia secondaria rispetto all’emissione di elettroni, si era giunti a una descrizione che faceva riferimento a particelle pesanti, portatrici di carica positiva, deviabili in campo elettromagnetico, atte a spiegare la maggior parte dell’energia emessa dalla materia in decadimento spontaneo, privilegiate rispetto agli elettroni, radicate nel fondo stesso dei mutamenti schematizzabili in termini di metaboloni, e, infine, caratterizzate da parametri analoghi a quelli dell’elio.
Fu lo stesso Rutherford a fare il punto della situazione nel 1904 quando fu invitato dalla Royal Society di Londra a tenere la prestigiosa Bakerian Lecture. Il titolo che egli dette alla sua lezione fu The Succession of Changes in Radioactive Bodies (La successione dei mutamenti nei corpi radioattivi)(19). Essa era suddivisa nei 13 capitoli seguenti:
l) nomenclatura;
2) velocità di disintegrazione della attività eccitata dal torio e uranio per differenti tempi di esposizione all’emanazione e per tipi di radiazioni differenti;
3) teoria matematica delle disintegrazioni successive;
4) applicazione della teoria al torio, attinio e radio;
5) questioni relative alla lentezza delle trasformazioni del radio;
6) radioattività apparente della materia ordinaria dovuta in parte a deposito attivo dell’atmosfera;
7) paragone nelle trasformazioni successive in U, Th, Ac. Tabella dei prodotti radioattivi;
8) discussione delle trasformazioni ‘senza radiazione’;
9) radiazioni emesse dai prodotti attivi. Significato dell’apparizione di raggi β e γ negli ultimi elementi della serie;
10) differenza tra trasformazione chimica e trasformazione radioattiva;
11) discussione di esperienze per misurare la carica della particella alfa;
12) entità dei cambiamenti che avvengono nei radioelementi;
13) origine degli elementi radioattivi.
Come già accennato la trattazione di Rutherford degli argomenti suddetti era il sunto delle conoscenze che si avevano sulla radioattività che erano illustrate con disegni del tipo seguente, ancora non completi nella nomenclatura ma certamente utili a capire il tipo di radiazione che veniva emessa. Inoltre, Rutherford era già in grado di fornire, oltre a varie proprietà fisico-chimiche dei materiali ottenuti dai decadimenti, i tempi di dimezzamento (tempo necessario a che l’attività si riduca a metà del suo valore iniziale) ed i valori della costante di disintegrazione λ (che dal primitivo significato di frazione di atomi che si disintegrano ogni secondo era passato al suo inverso 1/λ come vita media della corrispondente sostanza radioattiva) di molte delle sostanze radioattive che prendeva in considerazione (vedi la tabella Famiglia dell’uranio presentata qualche pagina più su dove il tempo di dimezzamento è chiamato periodo).

Decadimenti come presentati da Rutherford nel 1904
Era un fondamentale punto di arrivo che permise di capire molte cose e dove intervenire per capirne altre. Inoltre era propositivo di vari programmi di ricerca che partirono immediatamente. Tra di essi particolare rilievo ebbe quello che va sotto il nome di radiochimica della quale non mi occupo in questa sede.
Iniziavano molti anni di intense ricerche che servirono a sistematizzare e chiarire una mole di problemi e concetti. Molte cose le ho discusse nel precedente articolo nel quale mi sono occupato di Rutherford, dell’indirizzo di studio puntato sulle traiettorie delle particelle α, sullo scattering, della ricerca di modelli atomici che diventavano indispensabili come momenti di comprensione più generale di quanto si scopriva in radioattività.
Prima di chiudere questo paragrafo serve parlare di una delle scoperte più importanti fatte nell’ambito della radioattività, quella del concetto di isotopia, termine introdotto da Soddy nel 1913(20). Scriveva Soddy:
Che la carica intratomica di un elemento sia determinata dal suo posto nella tavola periodica piuttosto che dal suo peso atomico, come ha sostenuto A. van der Broek, ha una grande possibilità di verifica dopo la recente generalizzazione dei radioelementi e della tavola periodica. La successiva espulsione di una particella α e due β in ognuna delle tre trasformazioni radioattive riporta la carica intratomica dell’elemento indietro al suo valore iniziale, e l’elemento torna indietro al suo posto originale nella tavola, benché la sua massa atomica si sia ridotta di 4 unità. Abbiamo recentemente ottenuto qualche prova del punto di vista di van der Broek che la carica intratomica del nucleo di un atomo non è meramente una carica positiva, come nel tentativo di teoria di Rutherford, ma è la differenza tra una carica positiva ed una più piccola carica negativa […]
La stessa somma algebrica delle cariche positive e negative nel nucleo, quando la somma aritmetica è differente, fornisce quelli che io chiamo isotopi o elementi isotopici, perché essi occupano lo stesso posto nella tavola periodica. Essi sono chimicamente identici e, salvo solo qualche piccola proprietà che dipende direttamente dalla massa atomica, anche fisicamente identici.
Con questo concetto veniva messo un grande ordine in una serie di definizioni dubbie e contraddittorie. Da questo momento veniva riconosciuto il suggerimento di van der Broek ed il peso atomico veniva sostituito con la carica intratomica. Le proprietà chimiche dell’elemento erano stabilite non più dal peso atomico ma dal numero atomico che è poi il valore della carica centrale dell’atomo.
Altri lavori in proposito si ebbero da parte di Crookes, Hahn, Baltwood ed altri.
LA PAUSA DELLA PRIMA GUERRA MONDIALE
[Da John Cornwell, Gli scienziati di Hitler, Garzanti 2006]
La prima guerra mondiale venne soprannominata dalle generazioni successive di scienziati «la guerra dei chimici», un appellativo ampiamente meritato dal lavoro di Fritz Haber e dei suoi colleghi, che misero a punto i gas venefici. La fisica ebbe tuttavia un ruolo in chiaro scuro in una guerra nella quale i cannoni erano ancora 1’arma principale sulla terra e sul mare, e il problema più importante era indirizzare correttamente i proiettili a prescindere dalle condizioni atmosferiche, dal fumo, dalla distanza, dall’oscurità e dal moto ondoso dei mari in tempesta. Per calcolare la posizione di un cannone nemico, e di altri bersagli che emettevano segnali osservabili, i combattenti della prima guerra mondiale avevano impiegato le leggi fisiche dell’acustica, dell’ ottica, dell’ elettromagnetismo e della sismica. Gli scienziati impegnati nella ricerca di base su entrambi i fronti, quello alleato e quello degli imperi centrali, si misero anch’essi a lavorare alla tecnologia militare, dimostrando così quanto fosse labile e temporanea – durante la guerra – la separazione tra scienza pura e scienza applicata. Max Born di Gottinga studiò l’influenza del vento e dell’ altitudine sulla propagazione del suono. Max Wien di Jena lavorò sulle comunicazioni radio degli aerei. Arnold Sommerfeld di Monaco, pur essendo un celebre esperto di fisica teorica, studiò l’intercettazione delle comunicazioni telefoniche del nemico; le sue «cimici» elettroniche amplificate erano in grado di rilevare i segnali di una linea telefonica a un chilometro di distanza.
Gli scienziati britannici troppo anziani per combattere vennero coinvolti anch’essi nell’attività bellica, mentre i più giovani andarono entusiasticamente in trincea, dove in molti persero la vita. Ricordiamo in particolare Henry G.J. Moseley, il brillante allievo prediletto di Rutherford, ucciso da un cecchino nei Dardanelli. I fisici britannici […] si occupavano da tempo del problema di controllare il tiro dei cannoni (attraverso un apparecchiatura di misurazione della distanza) sulle navi da guerra, nonostante i pregiudizi dell’ ammiragliato. William Henry Bragg, padre di Lawrence e coinventore con il figlio della cristallografia a raggi X, lavorò sulla propagazione del suono per individuare i cannoni nemici, mentre Ralph Fowler (che poi divenne genero di Rutherford) studiò l’uso degli strumenti ottici presso il British Munitions Invention Department, per migliorare il controllo del tiro sui cannoni antiaerei. Frederick Lindemann (il futuro lord Cherwell, consigliere scientifico di Winston Churchill), lavorò a Farnborough sui sensori a raggi infrarossi come possibile sistema di allarme aereo precoce. Nel frattempo, a Manchester, Ernest Rutherford stava cercando la maniera di localizzaare gli U-boot.
Gli scienziati britannici avevano capito l’importanza della scienza e della tecnologia a fini bellici già nelle fasi iniziali della prima guerra mondiale. Sul numero del 17 giugno 1915, il direttore di «Nature» invitava il governo a utilizzare meglio «le centinaia di uomini di scienza del paese, le cui energie e conoscenze esperte non vengono utilizzate efficacemente. […] L’organizzazione dell’intelletto scientifico del paese è essenziale, ma non si è ancora fatto quasi nulla in questa direzione». Come i loro omologhi tedeschi, alcuni grandi scienziati britannici si erano dedicati a un lavoro di supporto all’attività bellica non necessariamente compatibile con il talento e con l’expertise di cui erano portatori; Rutherford, diventato famoso con la prima guerra mondiale per i suoi tentativi di comprendere l’atomo, era convinto che l’acustica fosse l’unico mezzo per rilevare la presenza dei sommergibili. Lui e il suo team si concentrarono sullo sviluppo degli «idrofoni» e di altri marchingegni per l’ascolto, tra cui l’utilizzo del quarzo piezoelettrico (cristalli che generano impulsi elettronici quando vengono urtati o compressi dalle onde sonore) per localizzare i suoni ad alta frequenza. Questa tecnologia anticipava la tecnica di rilevazione del sonar, o ecoscandaglio. Nell’ultimo anno di guerra Rutherford si era fatto un’idea abbastanza precisa delle possibilità offerte dalla fisica atomica. Si racconta che quando gli rinfacciarono la mancata partecipazione a una riunione di esperti sulle tecnologie antisommergibili, Rutherford – noto per il tono elevato della sua voce – abbia risposto: parlate piano, per favore. Ho fatto degli esperimenti da cui si desume che l’atomo si può disintegrare artificialmente. Se è vero, è ben più importante di una guerra». Successivamente dichiarò, curiosamente, che la scienza atomica non avrebbe mai prodotto energia in grandi quantità. Rutherford, Bragg e J,J. Thomson (il fisico di Cambridge che scoprì l’elettrone) facevano parte dell’ Admiralty Board of Invention and Research; ma la marina era restia a discutere di strategia e di tattica con dei civili, per cui molte opportunità andarono perdute.
Alla fine della grande guerra, ben pochi esponenti del governo e delle forze armate dovevano ancora convincersi che la fisica era essenziale per le armi e per la tecnologia della difesa, e che occorrevano ingenti finanziamenti da parte del governo se si voleva che la scienza avesse un ruolo di primo piano nella pianificazione del futuro. Nel 1918 la fisica a uso militare era ormai consolidata, ma pochi avrebbero potuto immaginare in che misura quella disciplina avrebbe dominato le armi e le innovazioni dei sistemi difensivi nella seconda guerra mondiale, specie per quanto riguarda l’individuazione degli aerei in volo notturno. Questa situazione è descritta vividamente dallo scrittore Russell McCormmach nel romanzo Pensieri notturni di un fisico classico. Riflettendo su questi argomenti nel pieno della prima guerra mondiale, Victor Jacob, protagonista del romanzo, arriva alla seguente conclusione: «Se, Dio ne guardi, ci sarà un’altra guerra, il mondo userà la fisica moderna. Ma questa guerra era combattuta con la fisica classica, in tutto e per tutto».
AVVICINAMENTO AL NUCLEO ATOMICO
Nei primi anni del Novecento J.J. Thomson volse la sua attenzione ai raggi canale scoperti da Eugene Goldstein (1850-1930) nel 1886.
Egli, studiando i raggi catodici, pensò di fare dei buchi sul catodo di un tubo a vuoto per vederne l’effetto.
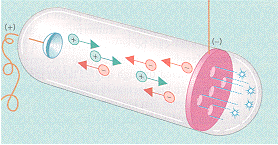
In queste condizioni Goldstein osservò un altro tipo di radiazione che si aggiungeva a quella ordinaria dei raggi catodici che andava dal catodo verso l’anodo(21). Questa nuova radiazione (chiamata kanalstrahlen o raggi canale o raggi positivi) passava attraverso i buchi (i canali) del catodo per andare ad urtare l’involucro di vetro del tubo catodico dietro il catodo medesimo. Questi raggi viaggiano quindi in direzione opposta ai raggi catodici e devono quindi trasportare una carica opposta che deve essere positiva. E le proprietà di tali raggi furono mostrate da Wien nel 1897(22). Egli trovò, tramite l’azione di campi magnetici ed elettrici, che essi hanno carica positiva ed un rapporto tra carica e massa molto più grande di quello dei raggi catodici. Per avere misure precise su questo, per le difficoltà che nascono dal fatto che tali raggi ionizzano fortemente l’aria residua nel tubo, occorrerà aspettare le misure che J.J. Thomson inizierà a realizzare a partire dal 1907(23).

Le misure di e/m per i raggi positivi di Thomson si realizzarono con l’apparato di figura seguente, che è una modifica dell’originale di Goldstein mostrato nella figura precedente.
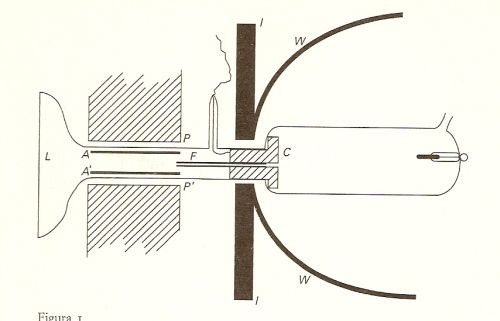

Nella prima figura in alto è mostrato lo schema dell’apparecchio utilizzato da Thomson. Era costituito da un tubo a scarica con il catodo C forato e contenente un sottile tubo F la cui funzione era sostanzialmente quella di collimare i raggi positivi. I segmenti A, A’ e le aree tratteggiate P, P’ rappresentano, rispettivamente, le piastre di un condensatore e i poli di un magnete cui era affidato il compito di deviare i raggi prodotti. I e W rappresentano la struttura di ferro che aveva la funzione di schermare elettrostaticamente il tubo a scarica. L, infine, indica lo schermo su cui incidevano i raggi positivi. La foto in basso fu ottenuta dallo stesso Thomson con un sistema fotografico da lui stesso elaborato
Si può immaginare che la foto di figura abbia sovrapposto un sistema di assi cartesiani con l’asse delle ascisse parallelo ai campi elettrico e magnetico e l’asse delle ordinate perpendicolare a tali campi. Lo spostamento sull’asse x, dovuto al solo campo elettrico sarà x = A.(e/m).(1/v2) mentre lo spostamento sull’asse y dvuto al solo campo magnetico sarà y = B.(e/m).(1/v) [con e, m, v:carica, massa e velocità delle particelle del fascio ed A e B: costanti che dipendono dalle intensità dei campi e dalla posizione della lastra fotografica]. Dalle precedenti equazioni eliminando e/m, si trova: y/x = (B/A).v che è l’equazione di una retta rappresentante le particelle che hanno velocità costante e differente e/m. Eliminando invece v, si trova: y2/x = (B2/A)(e/m) che è l’equazione di una parabola rappresentante le particelle che hanno un valore costante di e/m ma differente velocità. Con queste informazioni si possono determinare, come fece Thomson, le tracce sulle lastre fotografiche. Egli scriveva:
Le parabole sono determinate dal valore di e/m, così un atomo con una singola carica produrrà la stessa parabola di una molecola biatomica con una carica doppia.
Le parabole non sono complete ma solo archi che si dipartono da una distanza finita dalla verticale, questa distanza è […] inversamente proporzionale alla massima energia cinetica posseduta dalla particelle. Questa massima energia cinetica è dovuta alla carica cha passa dal potenziale dell’anodo a quello del catodo nel tubo di scarica. Consideriamo ora le particelle che hanno due cariche: esse acquistano nel tubo un’energia cinetica doppia rispetto a quella che ha carica singola. Alcune di queste particelle con carica doppia perderanno una carica passando attraverso il lungo tubo stretto situato nel catodo, ed emergeranno come particelle con una sola carica; esse possiederanno comunque energia cinetica doppia rispetto a quelle che sono stabilmente a carica singola. In tal modo il fascio di particelle emergenti dal tubo con carica singola sarà costituito da due tipi di esse, uno dei quali con energia doppia rispetto all’altro; le particelle che hanno energia cinetica doppia urteranno la lastra più vicine alla verticale che le altre ed in tal modo prolungheranno la normale lunghezza dell’arco di parabola che invece caratterizza le particelle con una singola carica.
Se l’atomo acquista più di due cariche tale prolungamento sarà maggiore […]
Usando questo metodo per distinguere tra sistemi con carica singola o multipla troviamo che le particelle che producono le parabole sulle lastre fotografiche possono essere divise nei seguenti tipi:
- Atomi elettrizzati positivamente con una carica.
- Molecole elettrizzate positivamente con una carica.
- Atomi elettrizzati positivamente con carica multipla.
- Atomi elettrizzati negativamente.
- Molecole elettrizzate negativamente.

L’apparato per lo studio dei raggi positivi realizzato da Thomson con la collaborazione di Aston nel 1909, quando Aston andò a lavorare nei laboratori di Cambridge.
LO SPETTROGRAFO DI MASSA
Le ricerche di Thomson, comunque, si muovevano nell’ambito di un programma che intendeva studiare a fondo la natura dell’elettricità. L’interesse per la struttura della materia era marginale ma queste ricerche mossero altri a seguire altre strade. In particolare è interessante notare, con Bruzzaniti, che nella Bakerian Lecture che Thomson tenne nel 1913 si ponevano alcune questioni la cui soluzione dette un forte impulso ai lavori di Aston. Nella memoria che riportava la Bakerian Lecture, Thomson scriveva:
La prima applicazione di tale metodo consiste nel rivelare i gas rari nell’atmosfera. Sir J. Dewar mi ha gentilmente fornito due campioni di gas ottenuti da residui di aria liquida; i campioni sono stati trattati in modo tale che uno contenga solo elementi pesanti e l’altro solo elementi leggeri (…). Volgendo ora l’attenzione alle fotografie degli elementi leggeri si possono osservare le linee dell’elio, del neon (molto forte), dell’argon e, in aggiunta, una linea corrispondente a un peso atomico pari a 22 che non può essere identificata con la linea dovuta a qualunque gas noto (…). L’origine di queste linee presenta molti punti interessanti: non c’è alcun composto gassoso noto degli elementi conosciuti che ha questo peso molecolare (…). Se noi accettiamo la tavola periodica di Mendeleev non c’è alcun posto per un nuovo elemento con questo peso atomico. Il fatto che questa linea, nel campione in osservazione sia brillante quando la linea del neon è straordinariamente brillante, mentre è invisibile nell’altro campione in cui la linea del neon è comparativamente debole, suggerisce che esso possa essere un composto di neon e idrogeno NeH2 benché sino ad ora non sia stata trovata alcuna evidenza diretta della combinazione di questi gas inerti. (…) C’è comunque la possibilità di un’interpretazione troppo rigida del sistema periodico di Mendeleev, nel senso che in un intorno del peso atomico del neon potrebbe esistere un gruppo di due o più elementi con proprietà simili, proprio come in un’altra parte della tavola periodica abbiamo il gruppo ferro, nichel e cobalto. Dall’intensità relativa della linea 22 e della linea del neon, possiamo concludere che la quantità del gas che dà la linea 22 è soltanto una piccola frazione della quantità di neon.
La tavola periodica confrontata con le osservazioni sperimentali mostrava un problema alla riga 22. Le parabole dei raggi positivi di Thomson mostravano che dovevano esistere due tipi di neon. La massa del neon ordinario è circa 20,2. Le tracce sulle lastre ne facevano risultare anche uno di massa 22 con parabole di intensità molto più debole, indicando ciò che il neon con maggiore massa era relativamente più raro (si veda la fotografia fatta da Thomson in basso a destra dove sono indicati i due isotopi del neon). Thomson lo aveva capito e descriveva con chiarezza il problema e Francis William Aston (1877-1945) risolse la questione comunicandola alla British Association nel 1913(24). In tale occasione diceva Aston:
Sir Thomson ha recentemente richiamato l’attenzione su alcuni risultati ottenuti con il metodo dei raggi positivi che implicano la probabile esistenza di un elemento di peso atomico pari a 22. Questo punto è stato ulteriormente analizzato e l’evidenza ottenuta mostra che il neon atmosferico non è omogeneo, ma consiste in una mistura di due elementi il cui peso atomico è approssimativamente 19,9 e 22,1 rispettivamente. Una parziale separazione è stata eseguita attraverso diffusione frazionata ( … ). I due elementi appaiono identici in tutte le proprietà eccetto che nel peso atomico.
Aston si propose di risolvere il problema dell’anomalia della riga 22 ma, i venti di guerra gli impedirono di lavorare su quel problema in quell’anno e dovette rimandare al 1919 quando scrisse una memoria con Lindemann(25).
Cerchiamo però di capire meglio quali sono i termini del problema discutendo un poco il comportamento di un fascetto di raggi positivi in campi elettrici e magnetici. Se sul percorso di tali raggi agisce un campo elettrico, esso costringerà il fascetto ad una traiettoria parabolica. Anche un campo magnetico provocherà una deviazione in accordo con la regola di Fleming della mano sinistra. E ciò perché, come ho già detto, in un campo elettrico la deviazione è inversamente proporzionale al quadrato della velocità mentre in un campo magnetico la deviazione è inversamente proporzionale alla semplice velocità. Per fissare le idee supponiamo che il campo magnetico, agente in corrispondenza dei riquadri tratteggiati di figure, abbia il polo nord davanti allo schermo ed il polo sud dietro di esso. Sappiamo già che gli elettroni hanno tutti stessa carica e stessa massa quindi stessa carica specifica. Ma con i raggi positivi abbiamo le cariche specifiche più diverse (la carica va generalmente da 1 a 4 ma la massa può andare da 1 a qualche migliaio). E’ necessario separare allora gli effetti della velocità da quelli della massa e per farlo occorre agire sui campi elettrici e magnetici in modo da focalizzare il fascetto in un punto della lastra. In tale situazione e con il campo elettrico agente come disegnato, si avranno le deviazioni e la focalizzazione mostrate in figura seguente per differenti velocità delle particelle, con uguale carica e massa, presenti nel fascetto.
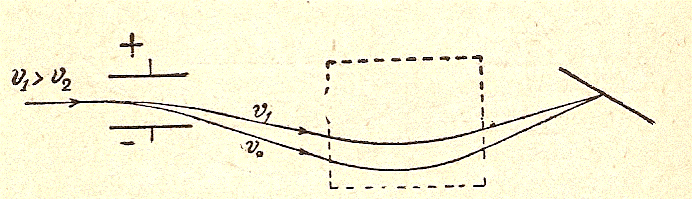
Si può operare sui campi elettrici e magnetici in modo da ottenere ciò che si ritiene utile a partire dalle dipendenze che vi sono nelle ralazioni che abbiamo visto. Così nella figura seguente il fascetto originale ha uguale carica e velocità ma diversa massa.
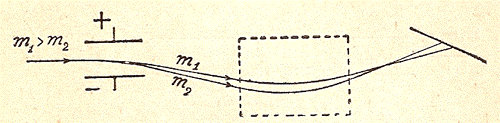
Nella figura seguente il fascetto ha uguale massa e velocità ma diversa carica.
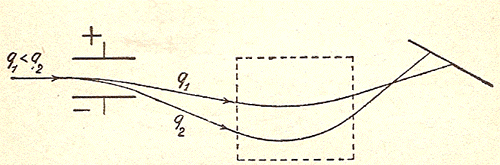
Nella figura seguente, quella che serve prendere in considerazione, le particelle hanno uguali carica ma diverse masse e velocità.
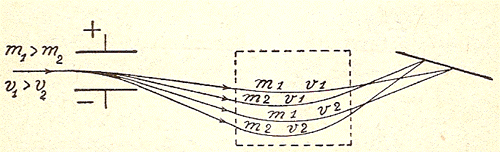
Nella pratica occorreranno molte più accortezze e le difficoltà cresceranno perché, ad esempio, aumenteranno le velocità comprese tra i due valori dati.
Torno ora alla memoria di Aston e Lindemann. I due ricercatori partirono da un confronto dei diversi metodi di separazione degli isotopi (distillazione, diffusione, densità, raggi positivi) e si resero conto delle enormi difficoltà che ciascun metodo presentava. In particolare quello dei raggi positivi, attraverso le parabole di Thomson, non era preciso per la cattiva definizione e la bassa intensità delle parabole. Fu Aston che si mise a lavorare sul metodo dei raggi positivi modificandolo opportunamente fino ad ottenere, mediante focalizzazioni che risolvevano le difficoltà annunciate del metodo delle parabole, ciò che oggi è noto come spettrografo di massa. Quando le velocità risultano focalizzate si aumenta il potere risolutivo dello strumento con la conseguenza che si possono separare le tracce fotografiche di ioni aventi masse poco diverse tra loro fino ad 1/600 dell’una rispetto all’altra e con errori inferiori allo 0,01%, qualcosa di sensazionale rispetto ai metodi chimici.
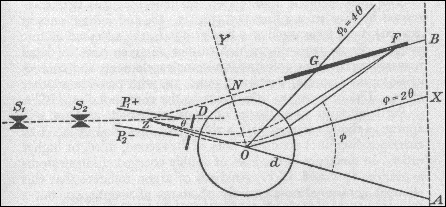
Lo schema di funzionamento dello spettrografo di massa di Aston che egli stesso pubblicò su Nature (105, p. 617, 1920).
Il disegno dell’apparato realizzato da Aston e lo strumento originale sono riportati nelle figure seguenti.
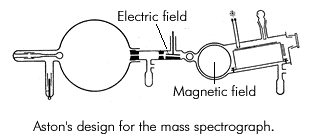


Lo spettrografo di Aston nel suo laboratorio.

Aston lavora alla separazione del neon dal meta-neon (come egli stesso aveva chiamato l’isotopo del neon cercato).
Le difficoltà che Aton aveva annunciato nel primo lavoro del 1919 vennero superate ed in una memoria del 1920(26) egli comunicò il buon esito dei suoi lavori annunciando l’esistenza del neon con peso atomico 20 e di quello con peso atomico 22, nelle proporzioni del 90% e 10%. Inoltre il suo spettrografo permetteva l’immediata individuazione degli isotopi dei più svariati elementi. La memoria di Aston si concludeva con queste parole:
La più importante generalizzazione prodotta da questi esperimenti è il fatto notevole che tutte le masse atomiche di elementi e composti fin qui misurate sono, all’interno degli errori sperimentali, dei numeri interi. È ancora prematuro sostenere che questa relazione sia vera per tutti gli elementi, ma il numero e la varietà di quelli esaminati rende ciò estremamente probabile (…). Cosi si può ora supporre che un atomo elementare di massa m possa essere cambiato in uno di massa m + 1 aggiungendo una particella positiva e un elettrone. Se entrambe penetrano nel nucleo si ottiene un isotopo, poiché la carica nucleare è inalterata. Se entra soltanto la particella positiva si ha un elemento avente numero atomico più alto. Nel caso in cui entrambe queste forme diano una configurazione stabile, i due elementi saranno isobari.
ROTTURA DEL NUCLEO
Rutherford, nel 1911, aveva capito che all’interno di un atomo deve esservi una carica positiva concentrata che poi assunse il nome di nucleo. Ma di tale nucleo si sapeva molto poco. Che lì era concentrata tutta la massa atomica e che era dotato di carica positiva come le particelle α che già Rutherford aveva capito essere dei nuclei di elio. Sempre impegnato con le sue ricerche di avanguardia, Rutherford proseguiva indagando sullo scattering delle particelle α con la materia e, nel 1919, fece quest’altra fondamentale scoperta. Questa volta l’apparato sperimentale era quello mostrato in figura.
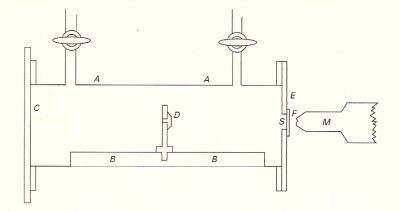
Molto schematicamente, il dispositivo utilizzato da Rutherford consisteva di una scatola rettangolare, lunga 18 cm, alta 6 cm e profonda 2 cm, contenente al suo interno una guida BB’ su cui poteva scorrere un supporto che sosteneva un disco D sul quale era deposta la sorgente di raggi α. li contenitore metallico, grazie a due rubinetti, poteva essere riempito con un determinato gas. Esso era posto tra le espansioni polari di un forte elettromagnete in modo da eliminare i raggi β che altrimenti avrebbero causato un’intensa luminosità sullo schermo di solfuro di zinco posto in F. Sul disco E era ricavata una stretta fenditura. La distanza tra la fenditura e lo schermo era di circa due millimetri, in maniera da poter inserire strati di potere assorbente noto su! percorso delle particelle diffuse e determinarne la distribuzione in funzione del loro percorso [da Bruzzaniti].
Siamo durante la Prima Guerra Mondiale e Mardsen, il collaboratore ed amico di Rutherford era tornato in Australia. Prima di andarsene, nel 1917, nell’eseguire esperienze di bombardamento di aria con particelle α, notò che si originavano particelle che avevano un percorso particolarmente lungo, maggiore di quello delle particelle α stesse, ed in apparente contrasto con la conservazione dell’energia. Una delle possibilità era che queste particelle fossero nuclei di idrogeno perché presentavano la stessa fenomenologia di quando si bombardava direttamente idrogeno con particelle α. E’ qui che intervenne un Rutherford privo di collaboratori a causa della guerra. Egli con estrema pazienza si mise ad indagare la natura di quelle particelle soprattutto per quel fino ad allora trascurato ed apparente contrasto con la conservazione dell’energia. Nel giugno del 1919 pubblicò la memoria(27) in 4 parti, Urti di particelle α con atomi leggeri, che raccontava la sua scoperta. Egli iniziò con lo stabilire che le particelle con così lunghe traiettorie erano originate dal bombardamento con raggi α degli atomi di azoto presenti nell’aria. Rutherford spiegò il fenomeno introducendo la legge del decadimento radioattivo: gli atomi di azoto decadono con emissione di energia. E la quarta parte del lavoro di Rutherford si chiudeva con queste parole: Dobbiamo concludere che l’atomo di azoto si disintegra sotto l’azione delle violente forze prodotte in un urto con una particella alfa veloce e che l’atomo di idrogeno [atomo H] che viene liberato era parte costituente del nucleo d’azoto. E’ il riconoscimento dell’esistenza della disintegrazione nucleare del fatto che è possibile passare da un elemento ad un altro intervenendo sui nuclei degli atomi. E questo fatto è davvero strabiliante. Rutherford concludeva così la sua memoria:
Dai risultati fin qui ottenuti è difficile non concludere che gli atomi a lungo percorso aventi origine dalla collisione di particelle α con azoto non siano atomi di azoto, ma atomi di idrogeno o atomi di massa due. Se questo è vero, dobbiamo concludere che l’atomo di azoto è disintegrato dalle intense forze sviluppate in un’intima collisione con una particella α veloce, e che l’atomo di idrogeno liberato è un costituente del nucleo di azoto (…). È interessante notare che mentre la maggior parte degli atomi leggeri hanno pesi atomici rappresentabili dall’ espressione 4 n o 4 n + 3, dove n è un numero intero, l’azoto è il solo atomo il cui peso atomico è espresso da 4 n + 2 (…) il nucleo di azoto è [dunque] formato da tre nuclei di elio, ciascuno di massa 4 e da due nuclei di idrogeno o da un nucleo di massa.
Si iniziavano cioè a fare ipotesi sulla costituzione nucleare e Rutherford, dopo aver chiamato protone il nucleo dell’atomo di idrogeno, ipotizzò addirittura una specie di neutrone (una sorta di atomo di idrogeno con l’elettrone caduto sul nucleo), una microstruttura con carica elettrica zero, vista come particella, ed intesa come «nucleo neutro». In un articolo scritto insieme a James Chadwick (1891-1974) nel 1921, suggerì che nell’atomo, attorno ad un «nucleo centrale», ruotassero dei «satelliti» identificabili come «nuclei H»(28). Nel 1921 J. L. Glasson pubblicava però i risultati negativi di una ricerca dell’ipotetico neutrone(29) e tali risultati non potevano portare ad altro perché ottenuti con la strumentazione che era stata fino ad allora efficacissima, i tubi a scarica, ma per particelle cariche .
CENNO AL SEGUITO DELLA STORIA FINO A FERMI ED ALLA SCUOLA DI ROMA
Gli anni che seguirono furono anni di elaborazioni fondamentali nella fisica. Le ricerche in campo nucleare si fecero sempre più feconde di risultati per arrivare ad una maggiore comprensione della struttura della materia. In ambito teorico nacque e si sviluppò la meccanica quantistica che fu alla base di nuove e fondamentali scoperte. E quanto la teoria produceva veniva ricercato in tutti i laboratori del mondo. Per quel che ci riguarda, fisica del nucleo e più in generale fisica atomica, vi sono alcune scoperte che vanno ricordate con l’avvertenza che quanto di seguito racconto è una semplificazione notevole. I contributi che vi furono furono centinaia e sarebbe di interesse capire come si arrivò ai fatti noti attraverso contributi che oggi non sono più ricordati. Ma l’economia (è il termine esatto) di questo lavoro non mi permette di entrare in dettagli.
Nel 1922-1923 il fisico statunitense A. Compton, studiando lo scattering dei raggi X con gli elettroni, deve ricorrere ai quanti di Einstein, quindi ad una interpretazione quantistica dei raggi X, per spiegare i fenomeni d’urto di fotoni X con elettroni.
Nel 1925 i due fisici olandesi Uhlenbeck e Goudsmit ipotizzano l’esistenza dello spin dell’elettrone. Questa particella ha un movimento a trottola in aggiunta agli altri movimenti atomici e tale movimento, anch’esso quantizzato, è caratterizzato da un numero quantico, il quarto, che può assumere solo due valori ± h/2π.
Nel 1925 il fisico tedesco W. Pauli postulò il Principio di esclusione secondo il quale in un atomo non possono esistere due elettroni con gli stessi 4 numeri quantici.
Il 1926 è l’anno in cui si ritorna a parlare autorevolmente di fisica italiana a 300 anni da Galileo e con la sola interruzione notevole di Alessandro Volta. In quest’anno Fermi pubblica la sua statistica per particelle dotate di spin semintero (statistica che riprenderà il britannico Dirac per inserirla nella sua meccanica quantistica e che è nota come statistica di Fermi-Dirac).
Nel 1927, per dare una spiegazione teorica alle condizioni di Bohr e Sommerfeld per l’esistenza di orbite atomiche, L. V. De Broglie associa un’onda ad ogni particella mediante la relazione p = h/λ, con p = quantità di moto dell’elettrone. Per avere spiegazioni più rigorose occorrerà attendere la soluzione dell’equazione di Schrödinger (almeno per l’atomo d’idrogeno). Subito dopo, nel 1927-1928, Davisson e Germer mostrarono sperimentalmente la natura ondulatoria degli elettroni.
Nel 1927 viene sviluppato, sulla base della meccanica quantistica, da Thomas e Fermi un metodo autoconsistente per calcolare la distribuzione della carica elettronica in un atomo.
Siamo arrivati all’inizio degli anni Trenta, quando occorre riprendere più da vicino gli eventi. A quest’epoca vi è la generale convinzione che il nucleo atomico sia costituito da elettroni e protoni e che si debbano considerare anche i fotoni. Già Rutherford, nel 1920, aveva fatto presente che il nucleo atomico risultava troppo piccolo per contenere tutti gli elettroni che gli erano assegnati dalle teorie di Prout, Aston e J.J. Thomson ed aveva avanzato quell’idea alla quale ho accennato di una particella neutra che entrasse nella costituzione di tale nucleo. Il fisico britannico James Chadwick (1891-1974) aveva iniziato una lunga serie di esperienze alla ricerca di quella particella vagamente teorizzata da Rutherford. Nel 1930 i fisici

J.J. Thomson (a sinistra) e Rutherford
tedeschi W. Bothe e H. Becker(30) fecero esperienze con sorgenti radioattive più intense ed una strumentazione più avanzata (il contatore di Geiger-Müller appena realizzato). Essi bombardarono il berillio 9 (ma anche boro e litio) con particelle
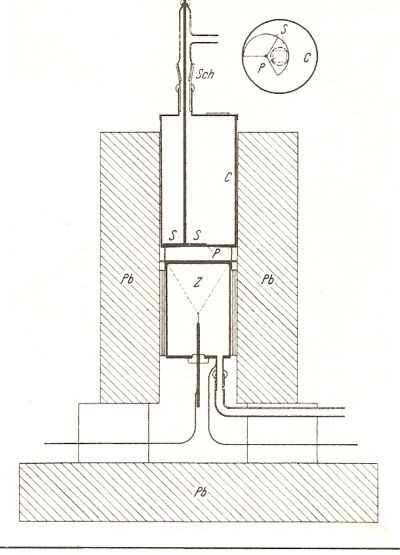
L’apparato sperimentale di Bothe e Becker (Z è il contatore Geiger-Müller)
alfa provenienti dal polonio e dal berillio uscirono radiazioni molto penetranti, molto di più dei raggi gamma emessi dal radio. Essa risultava molto più penetrante nella direzione di incidenza delle particelle alfa che non in quella opposta. Chadwick studiò il fenomeno e si convinse che il fenomeno poteva essere spiegato solo con l’ammissione di nuove particelle con caratteristiche diverse.
Intanto il fenomeno era indagato in Francia dai coniugi Frédéric Joliot ed Irene Curie (la figlia di Marie) che, subito dopo il matrimonio, cambiarono il loro cognome in Joliot-Curie. I due disponevano di una sorgente molto intensa di particelle alfa, generate da polonio, con la quale bombardavano della paraffina(31). Osservando gli effetti con una camera di ionizzazione collegata ad un elettrometro si resero conto che avevano generato una radiazione in grado di espellere protoni dalla paraffina. La cosa risultò strana perché energeticamente il bilancio non
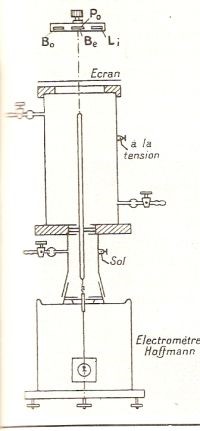
L’apparato sperimentale di Joliot-Curie
tornava. Se quelle radiazioni erano costituite da fotoni γ, questi non avrebbero mai avuto l’energia in grado di far schizzare fuori dalla materia dei protoni. Con i fotoni sono possibili effetti Compton ma questi riguardano elettroni. Un protone è circa 2000 volte più pesante e l’energia gamma, ma anche la sezione d’urto, è totalmente inefficace ad agire su protoni. I conti fatti dai Joliot-Curie, che attribuivano il fenomeno ai fotoni γ che avrebbero avuto proprietà inverosimili, fecero esclamare a Rutherford: Non ci credo! ed a Majorana: Che cretini, hanno scoperto il protone neutro e non se ne sono accorti!

Frédéric Joliot ed Irene Curie. Frédéric fu Presidente del Fronte di Liberazione Nazionale francese dal nazismo. Alla fine della guerra divenne Alto Commissario per l’Energia Atomica ma fu allontanato dall’incarico dal governo francese per la sua militanza comunista. La Francia trattò male anche Pierre e Maria Curie ai quali non concesse mai il “privilegio” di avere un laboratorio. I due morirono giovani per la contaminazione da radiazioni come accadde a molti ricercatori nel campo nucleare quando ancora non si conoscevano gli effetti disastrosi delle radiazioni.
Chadwick che seguiva con estrema attenzione l’evoluzione di tali ricerche e che, come osserva Segrè, era mentalmente preparato ad una particella neutra, ripeté le esperienze utilizzando polonio e berillio come sorgente indirizzando i proiettili alfa contro idrogeno, elio ed azoto. Con accurate misure riuscì a mostrare
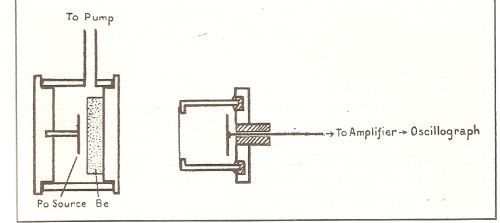
L’apparato sperimentale di Chadwick (a sinistra la sorgente di polonio e berillio, a destra la camera di ionizzazione).
che la radiazione molto penetrante che si produceva conteneva anche un tipo di particella neutra, con massa grande e simile a quella del protone, che egli chiamò neutrone(32).
A questo punto si chiarirono molte cose soprattutto relativamente all’isotopia e sembrò subito chiaro che nel nucleo dovessero esservi protoni e neutroni. Restavano però dei problemi molto grossi:
– come può un nucleo atomico emettere elettroni ?
– perché il bilancio energetico delle reazioni nucleari non torna, ogni volta che viene emessa radiazione beta (gli elettroni) sembra che dell’energia svanisca ?
– come è possibile tenere insieme in un nucleo due protoni, cioè due particelle cariche dello stesso segno che, secondo la legge di Coulomb, dovrebbero respingersi schizzando via come proiettili supersonici?
Nel 1933 Pauli ipotizzò che, a lato dell’elettrone, il nucleo emettesse anche un’altra particella non ancora rilevata (tale particella fu battezzata da Fermi: neutrino; doveva essere priva di carica e con una massa, nel caso fosse esistita, infinitesima). È il mito della conservazione dell’energia: piuttosto che rinunciare a questa certezza, i fisici preferirebbero il taglio della mano. Quali erano le caratteristiche di tale particella? Esattamente quelle che mancavano perché tornasse la conservazione, o meglio, le conservazioni (oltre all’energia, c’è la carica, la parità, la simmetria, …). Anche qui, il fatto straordinario è che questa particella, il neutrino, fu scoperta nel 1956 da Raines e Cowan (USA).
Nel 1934 fu Fermi ad entrare in argomento con un lavoro ancora storico e pietra miliare di ogni ricerca fisica: Tentativo di teoria di emissione dei raggi beta, pubblicato in tedesco da Zeitschrift für Physik ed in italiano su la Ricerca Scientifica(33) (è da notare che la prestigiosa rivista inglese Nature gli rifiutò la pubblicazione in quanto il lavoro era ritenuto “troppo astratto”). Si tratta di quella che oggi è nota come interazione debole o come interazione universale di Fermi. Nel lavoro veniva spiegato il fenomeno dell’emissione degli elettroni da parte di un nucleo con il decadimento di neutroni in protoni, elettroni e neutrini. In particolari condizioni un neutrone presente nel nucleo decade (o si disintegra) originando un protone, un elettrone ed un neutrino (oggi sappiamo che si tratta di un antineutrino). Di seguito riporto il modo con cui viene indicato il decadimento beta (n è il neutrone, p il protone, e– l’elettrone e νeil neutrino la barra sul quale lo rende antineutrino):
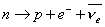
La reazione di decadimento conserva tutto ciò che la fisica nota prevede (essenzialmente: energia, carica e massa). Questo risultato di Fermi, a giudizio di tutti gli storici, sarebbe bastato a passarlo definitivamente alla storia della fisica insieme all’altro, già menzionato, della statistica di un gas di elettroni.
Questa scoperta di Fermi iniziava a far luce su alcune trasmutazioni nucleari già evidenziate ma, evidentemente, non capite dal britannico Blackett nel 1923.
I problemi sono i seguenti: che accade del nucleo di un atomo quando perde “un elettrone”? e cosa accade quando perde una particella alfa (cioè due protoni uniti a due neutroni)? Le questioni relative alle radiazioni gamma e neutroniche si porranno in seguito e saranno in gran parte risolte dalla soluzione ai due problemi posti.
La perdita di un elettrone da parte di un nucleo corrisponde ad un suo neutrone che è diventato un protone (con, appunto, l’espulsione dell’elettrone). Il numero dei protoni dell’atomo cresce di una unità. L’elemento chimico cambia natura (trasmuta) e si sale di un posto nella tavola periodica degli elementi.
L’espulsione di una particella alfa comporta, da parte di un nucleo, la perdita di due protoni. La conseguenza è che si scende di due posti nella tavola periodica e, anche qui, l’elemento chimico è un altro.
Ma il 1932 fu un anno definito formidabile, oltre al neutrone furono scoperti anche il deuterio ed il positrone (elettrone positivo). La prima scoperta è dovuta al chimico statunitense Harold Urey e si tratta del primo isotopo pesante dell’idrogeno scoperto. Il positrone fu invece trovato da un altro statunitense, dal fisico Carl D. Anderson. E’ la prima particella di antimateria che viene trovata che aprirà un campo enorme di ricerca. Essa era stata predetta teoricamente dalla teoria di Dirac e di tale predizione Anderson non sapeva nulla. Sarà merito di P.M.S. Blackett e G.P.S. Occhialini (1933) l’aver messo in relazione l’esistenza del positrone con le ipotesi di Dirac del 1930.
Tra il 1932 ed il 1933 venne formulato da Heisenberg e Majorana (a Lipsia per ragioni di studio) la teoria delle forze agenti all’interno dei nuclei, le forze quantistiche di scambio(34)che nascono da esigenze di simmetria per il fatto che le particelle costituenti il nucleo sono indistinguibili. Sulla base di questa teoria il fisico giapponese H. Yukawa nel 1935 ipotizzò una particella che avrebbe permesso lo scambio, il mesone π. Questa particella, dopo un’identificazione errata nel 1935 con i mesoni μ dei raggi cosmici, fu trovata sperimentalmente nel 1947.
Nel 1934 F. Joliot e I. Curie scoprirono la radioattività artificiale: “bombardando” con neutroni degli isotopi esistenti e stabili in natura, si ottengono degli isotopi instabili dello stesso elemento che, dopo l’emissione di uno o più tipi di radiazione ed un certo tempo, che varia da elemento ad elemento (vita media), ritornano spontaneamente ad essere isotopi stabili.
Nello stesso anno iniziava a Roma una grande e metodica serie di ricerche che avevano il fine di bombardare tutti gli elementi della tavola periodica e di studiare gli isotopi degli elementi che si ottenevano dopo la reazione nucleare. Tra i fisici del gruppo non vi era chi avesse importanti conoscenze di chimica. Per questo fu associato al gruppo stesso il chimico Oscar D’Agostino. Era lui che, dopo ogni esperimento di bombardamento, doveva studiare le proprietà chimiche dei prodotti di reazione e, alla fine, dire quali elementi si erano ottenuti.
Il metodo seguito era quello indicato più su: tra i prodotti della reazione di un dato elemento bombardato si cercavano isotopi di elementi o situati un posto successivo nella tavola periodica (nel caso in cui, bombardati da neutroni, avessero emesso radiazione beta) o elementi situati due posti più indietro nella stessa tavola periodica (se l’elemento in considerazione avesse emesso radiazione alfa). Arrivati all’ultimo elemento bombardato, l’uranio, poiché non vi erano elementi che rispondessero alle caratteristiche chimiche di ciò che si trovava due posti prima nella tavola periodica e poiché non vi era nulla dopo, Fermi pensò di aver creato due nuovi elementi il 93 ed il 94 che, proprio perché eventualmente situati al di là dell’uranio, furono detti transuranici.
Cosa era accaduto nelle reazioni nucleari con l’uranio ? Le cose non erano per nulla chiare perché si sovrapponevano svariati fenomeni:
– gli elementi radioattivi prodottisi nel bersaglio erano più di due;
– certamente l’uranio (l’isotopo 238) aveva dato origine a qualche transuranico ma era impossibile ricavarne proprietà chimiche che non si potevano conoscere;
– contemporaneamente l’uranio (l’isotopo 235, presente in percentuale dello 0,7% nel 238) aveva visto i suoi nuclei spezzarsi in due (o anche tre) pezzi più piccoli (nuclei di altri elementi, anch’essi radioattivi). Si era insomma prodotta la prima fissione nucleare ma Fermi e collaboratori non lo capirono (Amaldi successivamente parlò di “errore storico” del gruppo). Una tale non comprensione derivava dal fatto che il metodo seguito fino ad allora faceva cercare proprietà di elementi chimici “vicini” nella tavola periodica a quello bombardato. A nessuno venne in mente di cercare proprietà chimiche di elementi “lontani”. “Spaccandosi” un nucleo di uranio con 92 protoni, circa la metà di essi costituiscono un pezzo mentre la rimanente quantità di protoni costituisce l’altro pezzo. Occorreva cercare dalle parti del rodio, del palladio, dell’argento, …, insomma verso la metà della tavola periodica degli elementi: si sarebbero trovati isotopi di quegli elementi sovraccarichi di neutroni (l’uranio 235 ha 235 – 92 = 143 neutroni che prevedibilmente si suddividono più o meno al 50% per ogni prodotto di fissione) e pertanto fortemente radioattivi (la radioattività di un isotopo è tanto maggiore quanto più il numero dei neutroni sopravanza quello dei protoni nel nucleo dell’elemento). La cosa era stata capita dalla chimica tedesca Ida Noddack che scrisse un articolo e ne inviò copia a Fermi e collaboratori i quali, però, non vi fecero caso.
Ulteriori chiarimenti ed esperienze fondamentali vennero dai tedeschi Hahn e Strassman, dagli austriaci Lise Meitner e Otto Frish, dai francesi F. Joliot e I. Curie (tra il 34 ed il 39, momento in cui cadrà il silenzio su tali ricerche per la guerra che Hitler aveva scatenato).
Nell’ambito delle ricerche sul bombardamento dei vari elementi chimici un’altra scoperta fondamentale fu fatta dal gruppo Fermi. Si tratta della scoperta delle proprietà dei neutroni lenti.
Gli esperimenti di bombardamento con neutroni dei vari elementi avvenivano nel laboratorio interno all’Istituto di Fisica di Via Panisperna. Il lavoro era abbastanza ripetitivo e non tutti erano sempre presenti ad ogni fase delle successive sperimentazioni. Tutti i risultati raccolti fino all’estate del 1934 erano piuttosto grossolani. Tra i vari isotopi prodotti mediante il bombardamento con neutroni dei vari elementi chimici si era costruita una grossolana scala che prevedeva una “attività” forte, media, debole. Occorreva essere più precisi e fu così che si iniziò nell’autunno del 1934 una nuova serie di ricerche per fornire una scala di “attività” (oggi diremmo di “sezione d’urto”) più precisa. Il compito di realizzare tali misure fu affidato ad Amaldi ed all’appena arrivato giovane Pontecorvo.
Intanto occorreva costruire delle situazioni sperimentali che avessero potuto permettere la riproducibilità dei risultati ottenuti. Anche qui la geometria, la massa, i tempi, le distanze, giocavano un ruolo fondamentale. Come riferimento per le misure venne preso l’argento per il quale si disponeva di risultati molto attendibili Ma, nonostante l’estrema cura con cui ogni esperienza era progettata, vi era un qualcosa di straordinario che si presentava in corrispondenza di fattori apparentemente insignificanti. La radioattività del materiale bombardato aumentava vertiginosamente o diminuiva vistosamente se solo l’esperienza si faceva, rispettivamente, su un tavolo di legno o su un tavolo di marmo! Cosa succedeva? Tutto il gruppo fu allertato e tutti iniziarono a tentare di capire il fenomeno. Qual è la differenza principale tra un calcare (il marmo) ed il legno ? La presenza di idrogeno nel secondo. Poteva essere l’idrogeno che aveva un qualche effetto sui neutroni che andavano a bombardare il bersaglio ? Occorreva verificare tale ipotesi. Occorreva interporre un qualche materiale contenente idrogeno tra la sorgente di neutroni ed il bersaglio. Cosa contiene idrogeno ? Certamente la paraffina, ma al momento non se ne disponeva, e poi l’acqua. Nel giardino dell’Istituto vi era una fontana. Ci si recò subito lì. Seduti sul bordo della vasca si immersero con somma cura gli strumenti in acqua ed … il fenomeno divenne evidentissimo: la radioattività indotta sul bersaglio era cresciuta oltre quanto si potesse ragionevolmente immaginare. Ciò mostrava che l’ipotesi era corretta: interponendo tra sorgente e bersaglio delle sostanze idrogenate si ottiene un effetto moltiplicatore della radioattività indotta. Gli esperimenti furono ripetuti in laboratorio interponendo paraffina tra proiettili e bersaglio ed ancora si ottennero quegli stupefacenti risultati (le esperienze con paraffina sono del 22 ottobre del 1934). La sera di quel famoso 22 ottobre ci si riunì in casa Amaldi. Fermi praticamente dettava, Segrè scriveva e Rasetti, Amaldi e Pontecorvo passeggiando facevano commenti e correzioni ad alta voce. Fecero notte fonda e la domestica la mattina successiva chiese alla signora Amaldi se, per caso, i professori si fossero ubriacati. L’articolo che fu scritto, “Azione di sostanze idrogenate sulla radioattività provocata da neutroni“, fu immediatamente dato a la “Ricerca Scientifica” per la sua pubblicazione(35). Restava da capire il perché di un tale fenomeno. Fermi ed il suo gruppo lo fecero quasi subito per mezzo della fisica quantistica. Cerchiamo di descrivere sommariamente le cose.

Da sinistra: D’Agostino, Segrè, Amaldi, Rasetti, Fermi. La foto fu scattata dal più piccolo del gruppo, Pontecorvo.

Bruno Pontecorvo, dopo il 1950, già in URSS
Un neutrone è un ottimo proiettile perché riesce a penetrare le difese della materia con estrema facilità. Non essendo dotato di carica non subisce repulsioni di sorta da parte del nucleo atomico. Degli elettroni non si preoccupa: il rapporto di massa è di circa uno a 2000, quindi eventuali elettroni lungo la traiettoria vengono spazzati via. Se si usassero come proiettili gli elettroni, a parte altri inconvenienti, non si avrebbe una massa sufficiente per creare un qualche scompiglio nel nucleo. I protoni hanno una grande massa (circa uguale a quella del protone) e vengono sempre prodotti con una grande energia cinetica, e ciò vuol dire che sono dotati di grande velocità (superiore ad un km al secondo) e perciò chiamati “neutroni veloci”. Arrivati su una sostanza entrano al suo interno. Alcuni di essi passano tra nucleo e nucleo e non producono effetti. Altri vanno su di un nucleo ed in qualche modo, data la loro elevata energia, riescono ad attraversarlo senza provocare danni di un qualche tipo. Altri infine vanno a finire su dei nuclei e, venendo da questi inglobati, originano l’isotopo radioattivo. Solo pochi neutroni in definitiva arrivano in modo “utile” al bersaglio.
L’effetto delle sostanze idrogenate sui neutroni che le attraversano è di rallentarli in modo da ridurre la loro velocità a meno di un km al secondo, quando le hanno oltrepassate. È a questo punto che, rallentati, vanno sul bersaglio vero e proprio provocando effetti molto maggiori. E la cosa fu correttamente spiegata dal gruppo Fermi: la probabilità che un nucleo “catturi” un neutrone in arrivo è molto maggiore se il neutrone ha poca energia, dello stesso ordine di grandezza dell’energia propria di vibrazione del nucleo. Quando il neutrone è in “risonanza” con il nucleo (la sua “frequenza” è la stessa di quella con cui vibra il nucleo), avviene la cattura. Insomma un neutrone rallentato non ce la fa ad attraversare un nucleo che si trovasse sulla sua traiettoria, cresce quindi di molto il numero di atomi dell’isotopo radioattivo che si genera dall’elemento di partenza (aumenta la sezione d’urto e quest’ultimo concetto mostra anche la possibilità di trasformare un problema di una data natura in problema geometrico):
La notizia di questo risultato si sparse immediatamente per il mondo scientifico (fu lo stesso Rutherford che presentò la ricerca alla Royal Society di Londra) che iniziò subito, sotto questa nuova prospettiva, una nuova e lunga serie di esperimenti. Il gruppo di Roma, comunque, in 4 anni scoprì ben 50 isotopi radioattivi.
Ma siamo arrivati al 1935, inizio della fine della Scuola di Roma. Ciò che la Chiesa aveva fatto nel 1633 lo stava per ripetere il Fascismo: la distruzione di un gruppo, di una vera e propria Scuola che aveva ridato dignità alla ricerca fisica italiana riportandola alla ribalta mondiale.
A seguito delle indegne leggi razziali il gruppo si dissolse, in gran parte andando a lavorare negli USA (Pontecorvo in URSS ed Amaldi in Italia). La instancabile azione di Amaldi in Italia permise la sopravvivenza della prestigiosa scuola di fisica del gruppo Fermi portandola agli ancora prestigiosi livelli attuali.
NOTE
(1) H. Becquerel, Comptes Rendus des Séances de l’Academie des Sciences, 122, 406, 1896.
(2) H. Becquerel, Comptes Rendus, 122, 501, 1896.
H. Becquerel, Sur diverses propriétés des rayons uraniques, Comptes Rendus, 123, 855-858, 1896.
(3) Mme Sklodowska Curie, Rayons émis par les composés de l’uranium et du
thorium, Comptes Rendus, 126, 1101-1103, 1898.
(4) P. Curie e M. Curie, Sur une substance nouvelle radio-active, contenue dans la pechblende, Comptes Rendus, 127, 175-180, 1898.
(5) Curie P., Curie M., Bémont G., Sur une nouvelle substance fortemente radio-active contenue dans la pechblende, Comptes Rendus, 127, p. 1215-1218, 1898.
(6) E. Rutherford, Uranium radiation and the electrical conduction produced by it, Phil. Mag., 47, 109-163, 1899.
(7) E. Rutherford, A Radio-active Substance emitted from Thorium Compounds, Phil. Mag., 49, 1, 1900.
E. Rutherford, Radioactivity produced in Substances by the Action of Thorium Compounds, Phil. Mag., 49, 161, 1900.
(8) P. Curie e M. Curie, Sur la radioactivité provoquée par les rayons de Becquerel, Comptes Rendus, 129, p. 714, 1899.
(9) H. Becquerel, Influence d’un champ magnétique sur le rayonnement des corps radio-actifs, Comptes Rendus, 129, 996, 1899.
H. Becquerel, Sur le rayonnement des corps l’adio-actifs, Comptes Rendus, 129, 996, 1899, 1205, 1899.
(10) P. Curie, Action du champ magnétique sur les rayons de Becquerel. Rayons déviés et rayons non déviés, Comptes Rendus, 130, 73, 1900.
(11) H. Becquerel, Contribution à l’étude du rayonnement du radium, Comptes Rendus, 130, 206, 1900.
H. Becquerel, Déviation du rayonnement du radium dans un champ électrique, Comptes Rendus, 130, 809, 1900.
(12) P. Villard, Sur la réflexion et la réfraction des rayons cathodiques et des rayons déviables du radium, Comptes Rendus, 130, 1178, 1900.
(13) E. Rutherford, F. Soddy, The cause and nature of radioactivity (I), Phil. Mag., 4, 370-396, 1902.
E. Rutherford, F. Soddy, The cause and nature of radioactivity (II), Phil. Mag., 4, 569-585, 1902.
E. Rutherford, F. Soddy, The Radioactivity of Thorium Compounds – II. The Cause and Nature of Radioactivity, Journal of the Chemical Society, Transactions, 81: 837-860, 1902.
(14) E. Rutherford, Excited radioactivity and the method of its transmission, Phil. Mag., 5, 95-117, 1903.
E. Rutherford, The magnetic and electric deviation of the easily absorbed rays from Radium, Phil. Mag., 5, 177-187, 1903.
(15) E. Rutherford, F. Soddy, Radioactive change, Phil. Mag., 5, 576-591, 1903.
(16) Ancora relativamente all’energia sviluppata da materiali radioattivi, nello stesso periodo in Francia, Pierre Curie ed A. Laborde mostrarono che i sali di uranio sviluppano enormi quantità di calore. Ripetute le misure per il radio si trovò che un grammo di radio produce poco meno di 26 calorie l’ora. P. Curie, A. Laborde, Sur la chaleur dégagée spontanément par les sels de radium, Comptes Rendus, 136, 673-675, 1903.
(17) William Ramsay (1852-1916) e Frederick Soddy nel 1903 dimostrarono che il radio origina una produzione continua di elio. Era la prima volta che un elemento chimico veniva ottenuto da un altro elemento chimico. Ramsay, Soddy Experiments in Radioactivity, and the Production of Helium from Radium. Proc. Roy. Soc. 72, 204-7, 1903. Questo lavoro convinse gli scettici sulla teoria della trasmutazione degli elementi.
(18) La prova definitiva venne nel 1909 ad opera di Rutherford e Royds che nel 1909 dimostrarono che le particelle sono atomi di elio ionizzati due volte. Rutherford E., Royds T., The nature of the a particle from radioactive substances, Phil. Mag., Ser. 6, 17, 281-286, 1909.
(19) E. Rutherford, The Succession of Changes in Radioactive Bodies (Bakerian Lecture), Phil. Trans. R. Soc. A, 204, 169, 1904.
(20) F. Soddy, Intra-Atomic Charge, Nature, 92, 399, 1913.
F. Soddy, Radioactivity, Chemical Society Annual Reports 10, 262-88 1913.
(21) E. Goldstein, Berlin Sitzungber. p. 691, 1886.
(22) W. Wien, Verhandl. deut. physik. Ges. zu Berlin, 16, 165, 1897.
(23) J.J. Thomson, On Rays of Positive Electricity, Phil. Mag., 13, 561, 1907. J.J. Thomson, Positive Electricity, Phil. Mag., 18, 821, 1909.
J.J. Thomson, Rays of Positive Electricity (Bakerian lecture), Proc. Roy. Soc. A, London, 89, 1, 1913.
(24) F. W. Aston, A New Elementary Constituent of the Atmosphere, Rep. Brit. Ass. 82, 403, 1913. Il neon di Aston fu scoperto per la prima volta nel 1969 nel vento solare, in occasione delle missioni spaziali Apollo verso la Luna: Preliminary examination of lunar samples from Apollo 11, Science 165, 1211-1227, 1969.
(25) F.A. Lindemann, F. W. Aston, The Possibility of separating Isotopes, Phil. Mag., 37, 525, 1919.
Aston F.W., A Positive Ray Spectrograph, Phil. Mag., 38, p. 707, 1919.
Aston F.W., Isotopes and Atomic Weights, Nature, 105, p.617, 1920.
(26) Aston F.W., The Mass-Spectra of Chemical Elements, Phil. Mag., 39, p.611, 1920.
(27) Ernest Rutherford, Collision of alpha Particles with Light Atoms; An Anomalous Effect in Nitrogen, Philosophical Magazine, 37, No. 222, pp. 537-87, 1919.
(28) J. Chadwick, E. Rutherford, The artificial disintegration of light elements, Nature, 107, p. 41, 10 marzo 1921.
J. Chadwick, E. Rutherford, Phil. Mag., 42, 809, 1921.
J. Chadwick, E. Rutherford, Phil. Mag., 44, 417, 1922.
(29) J.L. Glasson, Attempts to Detect the Presence of Neutrons in a Discharge Tube, Philosophical Magazine, Sixth Series, 42:596, 1921.
(30) W. Bothe, H. Becker, Zeits. f. Physik, 66, 289, 1930.
W. Bothe, H. Becker, Zeits. f. Physik, 66, 307, 1930.
(31) I. Curie, F. Joliot, Émission de protons de grande vitesse par les substances hydrogénées sous l’influence des rayons γ trés pénétrants, Comptes rendus, 194, 273, 1932.
I. Curie, F. Joliot, Effet d’absorption de rayons g de très haute fréquence par
projection de noyaux légers, Comptes Rendus, 194, 708, 1932.
(32) J. Chadwick, Possible Existence of a Neutron, Nature, 129, 312, (Received Feb. 17, 1932).
J. Chadwick, The Existence of a Neutron, Proc. Roy. Soc., A, 136, p. 692-708 (Received May 10, 1932).
(33) E. Fermi, Tentativo di una teoria dell’emissione dei raggi β, Ric. Sci., 4, 491, 1933.
(34) Von W. Heisenberg, Über den Bau der Atomkerne.I., Zs.f.Phys. 78, 1, 1932. Von Ettore Majorana, zur Zeit in Leipzig, Über die Kerntheorie, Zs.f.Phys., 81, 137, 1933.
(35) E. Amaldi, B. Pontecorvo, F. Rasetti, E. Segrè, Azione di sostanze. idrogenate sulla radioattività provocata da neutroni, Ric. Sci., 5, 2, 1934.
19. Rutherford, E. and Soddy, F. Condensation of the radioactive elements. Phil. Mag., Ser. 6, 6: 561-576 (1903).
22. Rutherford, E. and Brooks, H.T. The new gas from radium. Trans. Roy. Soc. Can., Ser. 2, Sec. III, 7: 21-25 (1901).
23. Curie, M. Sklodowska. Sur le poids atomique du métal dans le chlorure de baryum radifère. Comptes Rendus, 129: 760-762 (1899).
24. Rayner-Canham, M.F. and Rayner-Canham, G.W. “Harriet Brooks. Pioneer Nuclear Scientist.” (McGill-Queen’s Univ. Press, Montreal & Kingston, 1992).
BIBLIOGRAFIA
(1) AA. VV. – Scienziati e Tecnologi dalle origini al 1875 – EST Mondadori 1975
(2) Emilio Segrè – Personaggi e scoperte nella fisica classica – EST Mondadori 1983
(3) E. Whittaker – A History of Theories of Aether and Electicity – Nelson and Sons 1952
(4) Articoli di Enrico Bellone in: Paolo Rossi (diretta da) – Storia della scienza –
(5) Mario Gliozzi – Storia della fisica – in: N. Abbagnano (diretta da) – Storia delle Scienze, UTET 1965
(6) René Taton (diretta da) – Storia generale delle scienze – Casini 1965
(7) Maurice de Broglie – Atomes, radioactivité, transmutations – Flammarion 1939
(8) Giuseppe Bruzzaniti – Dal segno al nucleo – Bollati Boringhieri 1993
(9) Robert A. Millikan – Electrons (+ and -), Protons, Photons, Neutrons, Mesotrons, and Cosmic Rays – The University of Chicago Press, 1934, 642 p.
(10) Tito Franzini – L’energia atomica – Bompiani 1951.
Categorie:Senza categoria
Rispondi