PER IL PDF:
(vai all’articolo che è in PDF su: PAGINE => DOCUMENTI)
Roberto Renzetti
NOTE BIOGRAFICHE DI SADI CARNOT
Nicolas Léonard Sadi Carnot è il primo dei due figli di Lazare Carnot(1). Il nome Sadi è un adattamento del nome del poeta persiano del 13° secolo, molto conosciuto sia in Francia che in Gran Bretagna, Saadi Musharrif ud-Din Muslih noto come Saadi, e ciò fornisce anche il senso dell’ambiente culturale aperto che vi era nella Parigi dell’epoca e della grande passione di Lazare per la letteratura e la poesia.
Sadi nacque in periodo rivoluzionario, nel 1796, quando suo padre era all’apice della sua carriera politica e dovette seguire le alterne fortune del padre. Solo un anno dopo la sua nascita vi fu il colpo di Stato del 1797 che vide Lazare esiliato per due anni. In questo periodo Sadi restò con la madre in un paesino vicino

Sadi Carnot a 10 anni
Calais. A partire dal 1807 fu Lazare che si occupò dell’educazione dei figli (Sadi aveva 11 anni ed Hippolyte 6) insegnando loro matematica, scienze, lingue e musica. E, per quanto si possa pensare il contrario, l’insegnamento fu maggiormente puntato alle lettere ed alle arti che non alle scienze, proprio per la grande vocazione letteraria di Lazare. Nel 1811 Sadi fu iscritto al Liceo Charlemagne del quartiere popolare Marais di Parigi per prepararsi alle prove di ammissione all’École Polytechnique. Nel 1812, quando aveva l’età minima di 16 anni per l’ammissione, riuscì ad entrare a l’École superando le prove proposte e trovandosi in posizione utile.

Ritratto di Sadi Carnot con la divisa dell’ École Polytechnique dipinto da Louis Léopold Boilly nel 1813, quando Carnot aveva 17 anni.
Tra gli insegnanti all’École vi era il fior fiore degli scienziati francesi dell’epoca, ed egli seguì i corsi di: Jean Nicolas Pierre Hachette (geometria descrittiva), Dominique François Jean Arago per il calcolo infinitesimale, Siméon Denise Poisson per la meccanica, Louis Jacques Thénard per la chimica e vari altri tra cui, c’è da notare, Pierre Louis Dulong (chimica) e Alexis Thérèse Petit (fisica) come ripetitori.

Jean Nicolas Pierre Hachette

Siméon Denise Poisson

François Arago

Louis Jacques Thénard

Pierre Louis Dulong
A parte una breve interruzione, in cui Sadi ed altri studenti dell’École furono arruolati nella Guardia Nazionale e combatterono per difendere senza successo il Forte di Vincennes dalla Coalizione di Stati europei che attaccava, Sadi seguì regolarmente i corsi e concluse brillantemente i suoi studi nel 1814 quando, per le sue note di studio estremamente positive, fu ammesso alla Scuola militare del Genio a Metz per frequentare i due anni di corso di ingegneria militare. Ma le vicende politiche crearono un qualche breve imbarazzo a Sadi perché, mentre era nella scuola di Metz, Napoleone riprese il potere e suo padre divenne Ministro della guerra. Ma ciò finì in breve tempo e Lazare fu esiliato a Magdeburgo, dove si recò con il figlio Hippolyte. Sadi si laureò nel 1817 con ulteriore imbarazzo nell’affrontare la carriera militare perché aveva un padre esiliato. Il lavoro che gli fu assegnato prevedeva continui spostamenti. Ebbe incarichi da ispettore di fortificazioni, di disegnatore di mappe e di redattore di rapporti. Non è trattato bene e la carriera è ferma. Nel 1818 venne bandito un concorso per entrare nel costituendo Corpo Reale di Stato Maggiore e Carnot partecipò vincendo un posto a Parigi (1819). Come addetto scientifico, aveva una paga inferiore a quella dei suoi colleghi (è tornata la monarchia !). A Parigi iniziò a frequentare vari corsi alla Sorbona, al Collegio di Francia e quelli serali al Conservatorio Nazionale d’Arti e Mestieri (considerato un covo di repubblicani e perciò tenuto sotto speciale sorveglianza). Fu in tale Conservatorio che Carnot, dal 1819, seguì le lezioni di chimica applicata dell’industriale e chimico Nicolas Clément, poi diventatogli amico, che trattavano, come vedremo, di argomenti di estremo interesse per Carnot. Ma Carnot si occupò anche di varie altre cose, le più disparate: studiò matematica, si occupò di economia politica con annessa la questione della riforma del sistema fiscale, si occupò di problemi ed organizzazione industriale, visitò fabbriche ed officine, si interessò d’arte, coltivò le sue passioni (era un bravo violinista ed ottimo ballerino) tra cui la boxe, visitò spesso il Louvre, frequentò l’Associazione Politecnica degli ex allievi dell’École Polytechnique, fondata dopo la rivoluzione del 1830 da Auguste Comte, si recò più volte al Giardino Botanico ed alla Biblioteca del Re, si divertiva agli spettacoli dell’Opéra-Comique de les italiens. Nel 1820 suo fratello Hippolyte venne da Magdeburgo a trovarlo. L’anno successivo fu lui che si recò a Magdeburgo a trovare suo padre. E’ qui che i due si scambiarono molte opinioni e conoscenze ed è qui che il padre indirizzò il figlio allo studio delle macchine, certamente idrauliche ma anche a vapore, perché, lo ricordo, di tali macchine Lazare aveva intrapreso lo studio nel 1818 in corrispondenza all’installazione della prima macchina a vapore a Magdeburgo. E Sadi aveva mostrato attenzione alle macchine a vapore e alle loro potenzialità proprio per i suoi grandi interessi per lo sviluppo industriale e per l’economia, particolarmente della Francia. Egli era anche convinto che una delle cause della sconfitta di Napoleone fosse proprio nel differente sviluppo che queste macchine avevano avuto in Inghilterra ed in Francia.
I suoi primi lavori sull’argomento delle macchine termiche sono del 1822-1823, appena ritornato a Parigi da Magdeburgo. Nel 1823, alla morte del padre Lazare, il fratello Hippolyte lasciò Magdeburgo per andare a vivere a Parigi con Sadi. Sarà l’occasione per redigere insieme l’opera fondamentale ed unica pubblicata in vita di Sadi Carnot, le Réflexions sur la puissance motrice du feu et sur les machines propres à développer cette puissance, allo scopo, come scriverà Sadi, di assicurarsi che i suoi scritti sarebbero stati compresi da persone votate ad altri studi.

Hippolyte Carnot (1801 – 1888)
Le Réflexions, sulle quali tornerò diffusamente,vedranno la luce in 600 copie, a spese dell’autore, nel maggio 1824, per i tipi del grande editore francese, Bachelier.

Il lavoro fu presentato all’Accademia delle Scienze di Parigi il 14 luglio 1824 e, successivamente, l’ingegnere Pierre-Simon Girard ne fece un resoconto alla stessa Accademia il 26 luglio, alla presenza di fisici del livello di Dulong, Laplace, Fourier e Arago. Ebbe poi la recensione favorevole (una sorta di riassunto che non coglieva alcuna delle novità presenti nel lavoro) di Girard pubblicata sulla Revue encyclopédique. Ma tutto finì qui non essendovi discussioni in proposito o ricadute particolari, tanto che presto il lavoro andò nel dimenticatoio. Come osserva Fox, quale interesse poteva suscitare nel 1824 un libro che raccomandava l’impiego delle alte pressioni e della tecnica dell’espansione ? Inoltre le condizioni che Carnot poneva per conseguire un rendimento massimo, definite su modelli ideali, risultavano del tutto irrealizzabili in pratica. E la pratica nel mondo degli ingegneri della macchine a vapore era l’unica cosa che allora avesse un senso (viceversa, gli scienziati non capivano come le macchine potessero avere un interesse scientifico). Le Réflexions furono menzionate solo in un necrologio di Adolphe Gondinet, segretario dell’Associazione Politecnica, che gli fu tributato nel 1833 dalla stessa Associazione con un qualche rimprovero per non aver usato l’analisi matematica. Edizioni successive si ebbero solo nel 1872 e nel 1878, quando tutto già era stato fatto e chiarito nell’ambito della termodinamica.
Intanto dovette riprendere la vita militare andando in giro per i compiti più svariati. Dopo molteplici incarichi ricevuti, finalmente tre anni dopo (fine 1827), riuscirà ad essere promosso capitano in seconda del Genio militare. Ma qualche mese dopo egli richiese di essere dimesso dall’esercito per motivi personali, e le dimissioni gli furono accordate nel maggio 1828. Da questo momento poté dedicarsi completamente agli studi sostentandosi con una piccola rendita proveniente da una parte dell’eredità, in origine consistente, del nonno materno.
Nel luglio 1830 vi fu un tentativo di colpo di mano contro la Costituzione da parte del Re. Seguì una sollevazione popolare che cacciò i Borboni e tentò di instaurare la Repubblica abbattendo la monarchia. Sadi partecipò con convinzione ai moti popolari perché era, con suo fratello, un convinto repubblicano molto interessato alla vita pubblica del suo Paese. Egli odiava i Borboni e con essi gli elementi reazionari della Chiesa Cattolica che faceva da sostegno a quella casa regnante. Le cose si risolsero a metà perché non si riuscì a instaurare la Repubblica ma si riuscì a mantenere una monarchia costituzionale con un ramo cadetto dei Borboni, gli Orléans. Sadi ne restò deluso perché tra i compiti che assegnava ad un eventuale governo repubblicano vi era il potenziamento dell’istruzione pubblica che, con la monarchia ed il clero, sarebbe decaduta ancora di più. La fine del sogno lo riportò ai suoi studi.
Agli inizi del 1831 un’ordinanza governativa obbligò ciascun quartiere a dotarsi di una compagnia di artiglieria e questa fu per Sadi l’occasione per ritornare ad occuparsi di cose militari infatti sarà arruolato come caporale. Ma proprio in quell’anno Sadi riprese interesse per gli studi delle macchine a vapore sollecitato dalla pubblicazione di due memorie del suo ripetitore all’École, Dulong, che trattava delle proprietà fisiche dei gas e delle relazioni esistenti tra pressione e

Sadi Carnot a 34 anni in un ritratto di Despoix
temperatura. I suoi propositi si scontrarono però con forti febbri persistenti che lo colsero a seguito di aver contratto la scarlattina, infezione che si aggiungeva ad una salute malferma. Sadi Carnot, con il fisico debilitato, fu qualche mese dopo vittima di un’epidemia di colera che, nel 1832 a soli 36 anni, lo stroncò. Lasciò uno scritto non pubblicato che, probabilmente nelle intenzioni, si sarebbe dovuto integrare con il precedente in un’opera più compiuta, Recherche d’une formule propre à représenter la puissance motrice de la vapeur d’eau(2), e delle note sparse, scritte tra il 1824 ed il 1826. In queste ultime vi sono appunti che ruotano soprattutto sui suoi dubbi relativi alla natura del calore e sul suo definitivo cambiamento a tale proposito. Essi prefigurano esperimenti che Carnot si proponeva di realizzare per studiare gli effetti termici dell’attrito nei fluidi. Alcuni di questi esperimenti erano simili a quelli che realizzerà Joule venti anni dopo. Il corpo di Sadi fu cremato ed allo stesso modo furono bruciati tutti i suoi scritti, le sue carte ed i suoi effetti personali, come si usava per chi aveva avuto malattie contagiose, solo qualche appunto si salvò.
LE TEORIE DEL CALORE
E’ utile, prima di andare oltre, dare uno sguardo alle teorie del calore che si avevano nei primi anni dell’Ottocento ed in particolare alla teoria del calore di cui si servì Sadi Carnot nelle sue Réflexions perché essa giocherà un ruolo di rilievo anche nei successivi ripensamenti dello stesso Carnot. E’ noto che la teoria, inizialmente sostenuta da Carnot, era quella del calorico che andava per la maggiore negli anni in cui egli redasse la sua opera. Ma la teoria del calorico deriva da una precedente teoria, quella del flogisto (materia ardente) sviluppata inizialmente dall’alchimista tedesco Joachin Becher (1635 – 1682). Secondo Becher, che si muove completamente in ambito aristotelico, i due costituenti la materia sono acqua e terra. La terra però può essere di tre tipi: terra mercuriale,

Joachin Becher
terra vetrosa, terra infiammabile o terra pinguis. Dalla diversa quantità con cui queste tre terre entravano a formare i corpi dipendevano le proprietà di essi e la combustibilità di un corpo era tanto maggiore quanta più terra pinguis lo componeva. Questa teoria fu sostenuta, elaborata e fatta conoscere dal medico e chimico tedesco Georg Ernst Stahl (1660 – 1734) che ebbe cura di tentare una sua razionalizzazione togliendo da essa gli elementi alchimistico-metafisici. Fu Stahl

che dette enfasi alla terra pinguis chiamandola flogisto. Esso è presente all’interno di tutti i corpi combustibili e sfugge da essi durante la combustione o la calcinazione, cambiando la loro natura (e qui vi erano molte reazioni chimiche spiegate con l’acquisto o la perdita di flogisto). Quando il flogisto, elemento imponderabile (alcuni addirittura gli assegnavano peso negativo) ed inafferrabile, non è all’interno dei corpi e quindi risulta libero, dà la sensazione di caldo. La teoria del flogisto fu anche utilizzata per spiegare alcune proprietà delle arie, quelle che oggi chiamiamo gas. Ed a seconda dei vari comportamenti rispetto al flogisto, furono classificate tre arie successivamente scoperte: accanto all’aria ordinaria, l’aria fissa (anidride carbonica), l’aria infiammabile (idrogeno) e l’aria deflogistificata (ossigeno).
Poiché la teoria non entrava in conflitto con altre teorie sulla materia ed era in linea con la filosofia di Descartes, fu accettata da tutti senza ostacoli almeno fino alla metà del XVIII secolo.
In ambito più eminentemente fisico, a partire dai primi anni del Settecento e sull’onda delle teorie corpuscolari di Newton, si diffuse la teoria che potremmo chiamare di calore come agitazione molecolare. Il primo studioso che sostenne con chiarezza che il calore è uno stato di agitazione delle molecole costituenti i corpi, fu Boyle. Dopo di lui Euler che scrisse esplicitamente (1752): che il calore consista in un certo moto delle piccole particelle dei corpi è ormai abbastanza chiaro.
Nella seconda metà del Settecento riprese però vigore la teoria che voleva il calore come una sostanza ad opera principalmente del chimico britannico Joseph Black (1728 – 1799) che considerava, con molte contraddizioni, il calore come un non precisato qualcosa di reale, assimilabile però ad una sostanza fluida composta da particelle legate alle molecole delle altre sostanze e distribuite in modo omogeneo. Tale qualcosa, chiamata calorico successivamente (1787) da Laplace e Lavoisier, può essere ceduto o assorbito dai corpi durante processi di

Joseph Balck
vario tipo. Esso, oltre a produrci la sensazione tattile di temperatura, produce il cambiamento di stato dei corpi. Ciascun corpo possiede una quantità finita di calorico e noi avvertiamo sensazioni diverse toccando i corpi a seconda del calorico che è in essi, così, ad esempio, la sua minore o maggiore concentrazione, è responsabile della diversa temperatura dei corpi e delle nostre sensazioni di caldo e freddo. Se poi strofiniamo un corpo (attrito) con le mani, aumenta la sensazione di caldo perché spremiamo del calorico dall’oggetto strofinato. Mettendo a contatto due corpi a temperature differenti, il calorico passa da quello in cui era più concentrato all’altro fino all’ equilibrio dato da una concentrazione di fluido calorico intermedia. Il calorico, inoltre, oltre ad essere in quantità costante nell’universo, si conserva nei suoi passaggi in differenti fenomeni fisici. Questa teoria era più completa di quella del flogisto e, pur non negando quella teoria, la inglobò.
Ogni buon matematico e fisico della seconda metà del Settecento si cimentò nel descrivere o inventare modelli per il calorico che comunque doveva essere considerato come imponderabile ed estremamente elastico (nel caso dei gas era il responsabile della repulsione tra molecole). La maturazione della teoria avvenne con i lavori di Laplace (1749 -1824), Poisson (1781 – 1840) e Lavoisier (1743 – 1794).
Il modello del calorico di Laplace fu sviluppato nel suo Traité de Mécanique Céleste (1799 – 1825). Nella sua descrizione meccanicistica del mondo (i fenomeni terrestri come i fenomeni celesti) trovò posto anche il calorico trattato matematicamente come gli altri fluidi (liquidi e gas). Il calore era concepito analiticamente come una funzione dello stato del corpo e la temperatura del sistema era ridotta ad un parametro della funzione di stato. Mediante il principio di conservazione del calorico e supponendo che anche se non si è in grado di conoscere il calore totale di un corpo, si può conoscere la sua variazione, definita da un differenziale esatto. Tale modello prevede che ogni molecola di una data sostanza sia circondata da un’atmosfera di calorico. La materia risulta quindi

Pierre Simon de Laplace
composta da molecole tra le quali si producono attrazioni gravitazionali e repulsioni dovute all’atmosfera di calorico che le circonda. La trattazione che ne dava Laplace, in termini di forze ed in linea con la fisica newtoniana, si serviva dell’apparato matematico delle equazioni differenziali. Ciascuna molecola di un dato corpo può poi acquistare o cedere del calorico con il risultato che le proprietà termiche del corpo variano. Il moto delle molecole provoca urti reciproci in conseguenza dei quali si origina il movimento del calorico. Scaldare un corpo vuol dire aumentare il suo contenuto di calorico che va a sistemarsi tra le sue molecole (discorso analogo per il raffreddamento). Quindi il calorico è diffuso in tutta la materia ed in grado di penetrare o uscire dai corpi entrando nella loro costituzione, originando in alcuni casi la loro disgregazione (passaggio da solido a liquido) ed in altri la loro dissoluzione (passaggio da liquido a vapore). Il termometro poi non è in grado di rilevare le atmosfere di calorico ma solo il calorico libero. Le atmosfere di calorico risultano essere il calore latente. Si apriva qui il problema della comprensione del significato fisico del concetto di temperatura. Si stabilì che essa doveva essere proporzionale alla densità del fluido calorico in un dato volume quando si fosse all’equilibrio termico.
Riguardo alla relazione esistente tra calorico e lavoro meccanico, il calorico era visto come qualcosa che permetteva la generazione di lavoro passando da un corpo ad alta temperatura ad un altro a temperatura più bassa, ma rimanendo inalterato.
L’esposizione completa ed organica della teoria del calorico fu di Lavoisier nel suo Traité élementaire de Chimie (1789). Egli confutò le idee flogistiche, stabilendo che la terra infiammabile non era contenuta nei corpi combustibili come loro principio costituente. E’ infatti il principio ossigenico (l’aria che successivamente sarà chiamata ossigeno), componente dell’aria comune, che quando si combina con un radicale qualunque libera un fluido imponderabile abbondante in natura: il calorico. Tale terra era tutt’altra cosa, quella appunto che abbiamo ora descritto. Scrive Lavoisier:
Sappiamo, in generale, che tutti i corpi esistenti in natura sono immersi nel calorico, che essi ne sono circondati e penetrati da tutte le parti, e che esso riempie tutti gli intervalli tra le loro molecole; che in certi casi il calorico si fissa dentro i corpi, entrando come costituente delle loro parti solide, ma che più spesso esso circonda le molecole, esercita su di esse una forza repulsiva e che dalla sua azione o dalla sua accumulazione più o meno grande dipende il passaggio dei corpi dallo stato solido allo stato liquido, dallo stato liquido allo stato aeriforme.
In tale lavoro però Lavoisier avanzò qualche dubbio, non confortato però da una minima ricerca sperimentale su quella vicenda che è l’imponderabilità del calorico (eppure la bilancia di Lavoisier era formidabile e gli aveva permesso di stabilire la conservazione della massa). Dice Lavoisier:
Non siamo obbligati a supporre che il calorico sia una materia reale; è sufficiente […] che esso sia una causa repulsiva qualunque, e se ne possono considerare gli effetti in modo astratto e matematico. [Citato da Sebastiani]
E questa posizione di dubbio era anche di Laplace. I due infatti scrissero insieme nella loro Mémoire sur la chaleur (Mémoires dell’Académie Royale des Sciences di Parigi, 1780) quanto segue:
I fisici non sono d’accordo sul calore. Molti di essi lo considerano come un fluido diffuso in tutta la natura ( … ). Altri lo considerano solamente come il risultato di movimenti invisibili delle molecole, gli spazi vuoti tra le molecole permettendo le vibrazioni in tutti i sensi. Questo movimento invisibile è il calore. Sulla base del principio di conservazione della forza viva, si può dare così questa definizione: il calore è la forza viva, cioè la somma dei prodotti della massa di ogni molecola per il quadrato della velocità. [Citato da Gliozzi]

Antoine Lavoisier
Insomma, siamo nella situazione di una teoria che, pur essendo utilizzata, è messa in discussione dagli stessi scienziati che più la sostengono. Ma siamo alla fine del secolo, quando, da più parti, iniziano delle critiche serrate alla teoria fluidistica del calorico (Rumford, Davy, Young, …). Osservo di passaggio che in questa Mémoire sur la chaleur, venne stabilito un principio, quello della conservazione della quantità di calorico in ogni processo.
La teoria del calorico fu feconda di vari risultati che gli stessi Laplace e Poisson conseguirono. Laplace, utilizzando il modello del calorico descritto, corresse il metodo che Newton aveva fornito per misurare la velocità del suono supponendo che la sua trasmissione non avvenisse in modo isotermo ma senza scambi di calore con il mezzo esterno (con una trasformazione adiabatica) e Poisson stabilì successivamente (1823) la legge che regola tali trasformazioni adiabatiche (PVg = costante). E poiché la correzione di Laplace era in accordo con i dati sperimentali, essa fu ritenuta come una conferma della teoria del calorico. Oltre a ciò il calorico spiegava, almeno qualitativamente, i fenomeni più comuni con i quali si aveva a che fare: calore latente, propagazione termica, riscaldamento adiabatico, calore che si sviluppa nelle reazioni chimiche, calore che si produce negli urti.
Almeno un cenno, a questo punto, occorre dare ai lavori sul trasferimento del calore nei solidi di Jean Baptiste Joseph Fourier (1768 – 1830), anche se non avrà alcuna rilevanza per le cose che riguardano le macchine a vapore.

Già Newton aveva studiato (1701) la trasmissione del calore lungo una barra di ferro avente una estremità in un braciere. Da queste sue prime osservazioni altre ne seguirono da parte di altri ricercatori. Amontons (1703) mise a scaldare sul braciere l’estremità di una lunga barra di ferro, e misurò sulla barra le distanze alle quali fondevano il vetro, il piombo, lo stagno, una lega di piombo e stagno, la cera, il sego e il burro. Questa stessa esperienza fu ripetuta da Fourier nel 1804 quando egli studiava teoricamente mediante il calcolo differenziale, la propagazione del calore nei corpi solidi. Egli non fornì però alcuna spiegazione fisica del calore scrivendo nella sua Théorie analytique de la chaleur (1822)che comunque si voglia concepire la natura di questo elemento, sia che lo si consideri come un’entità materiale distinta, che passa da una parte ad un altra dello spazio, sia che uno pensi che il calore sia una semplice trasmissione di movimento, si arriverà sempre alle stesse equazioni, perché l’ipotesi che uno avrà fatto deve rappresentare i fatti generali e semplici, dai quali vengono derivate le leggi matematiche.
Fourier ricavò le equazioni differenziali del moto del calore, avendo in mente un flusso, quello del calorico indistruttibile (stesse equazioni furonoricavate da Biot nel 1804 ma Fourier accompagnò le sue elaborazioni con dati sperimentali). Egli fece l’ipotesi fondamentale seguente: nei corpi isotropi il calore fluisce perpendicolarmente alle superfici isoterme, proporzionalmente al tasso di diminuzione della temperatura v seguendo questa perpendicolare all’istante t considerato, et proporzionalmente ad un parametro K, che in generale è funzione della temperatura. Con questa ipotesi e con il simbolismo introdotto, la quantità di calore, che durante l’istante dt fluisce attraverso un cerchio orizzontale infinitamente piccolo di superfice y, ha per valore – K (dn/dz)wdt. Fourier ricavò anche le equazioni del moto del calore lungo un prisma solido di lunghezza infinita trovando che la temperatura v deve soddisfare in ogni punto l’equazione alle derivate parziali (caso ad una dimensione):
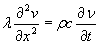
dove: ρ è la densità del materiale, c il suo calore specifico, λ la sua conducibilità termica. Fourier passa ad integrare tale equazione e, per farlo, utilizza la serie trigonometrica che ancora oggi porta il suo nome.
L’analisi di Fourier segna l’inizio della fisica matematica ed ebbe una grande influenza sullo studio dei fenomeni elettrici (metodo delle analogie).
LE RÉFLEXIONS SUR LA PUISSANCE MOTRICE DU FEU
Occorrono alcune considerazioni iniziali prima di entrare nella descrizione delle Réflexions di Carnot.
Intanto occorre dire che la teoria sulla natura del calore con la quale lavorò Carnot era quella ora descritta del calorico. In somma sintesi il calorico era un fluido imponderabile, estremamente sottile, elastico, indistruttibile ed in grado di trasferirsi da un corpo ad un altro, da quello più caldo a quello più freddo.
Altro aspetto di rilievo, nelle elaborazioni di Carnot, fu il suo rapporto, al quale ho accennato, con Nicolas Clément. Le sue lezioni, seguite da Carnot, trattavano anche di come si comporta il vapor d’acqua nell’espansione in un cilindro, in relazione al principio di espansione enunciato da Watt. Alcune conclusioni del 1816 di Jean-Baptiste Biot sembravano confermate dalle esperienze di Clément

Jean-Baptiste Biot
sembrava cioè che l’impiego del vapore ad alte pressioni, senza espansione, avesse dei vantaggi solo teorici perché, nella pratica, occorreva fare i conti con le compatibilità tecnologiche (la tenuta dei giunti nelle macchine termiche che poteva provocare esplosioni) che non permettevano di salire in pressione oltre certi valori. Clément indagò ancora e la cosa fu ulteriormente confermata. I suoi risultati furono presentati nel 1812 all’Accademia delle Scienze di Parigi in una memoria che Clément scrisse insieme al suocero Charles-Bernard Desormes, anch’egli valente chimico. Essa non fu pubblicata perché non furono apprezzate alcune considerazioni teoriche sulla temperatura che conteneva. Solo nel 1819, quando cambiarono i giudici, venne pubblicata (Desormes e Clement, Du zéro absolu et du calorifique spécifique des gaz, Journal de Physique, de Chimie et d’Histoire naturelle, 1819, 89, 321-428). In tale memoria, che trattava della misura sperimentale dei calori specifici dei gas e del rapporto tra calori specifici a pressione e volume costanti, si mostrava che vi era una maggiore economicità ad utilizzare vapore ad alta pressione con

Nicolas Clément
espansione libera dell’agente utilizzato, dopo l’interruzione dell’immissione, di quanta non ve ne fosse nell’uso del solo vapore ad alta pressione. Tale espansione era normalmente considerata isoterma ma Clément e Desormes supposero, in modo stravagante, che l’espansione, dopo l’interruzione dell’immissione, fosse adiabatica (senza scambi di calore con l’ambiente e con conseguente abbassamento di temperatura del mezzo). Inoltre occorreva lavorare con pressioni le più elevate possibili compatibilmente con la tecnologia disponibile, perché la prestazione ottenuta nell’espansione è tanto più elevata quanto maggiore è la pressione. Questi studi che Carnot conosceva, lo influenzarono molto(3) tanto che nel ciclo che egli ipotizza hanno una funzione importante proprio le espansioni con, anche qui, la stravagante novità, come vedremo, di puntare più sull’innalzamento della temperatura che su quello della pressione, rispetto alla quale era sempre stata considerata fino ad allora la potenza motrice, per realizzare l’economia di cui si discuteva. Ma non era quella della temperatura la sola stravaganza, vi era anche il considerare, con Clément, espansioni adiabatiche e non isoterme e, soprattutto, l’introduzione di un ciclo. Ciò vuol dire che Carnot si confrontava, pur in un discorso teorico, con la realtà. Per pura speculazione si può pensare ad una macchina costituita da un cilindro infinito ed un pistone. Se si immette un gas nel cilindro e si scalda indefinitamente, il pistone si muoverà per la dilatazione continua del gas. Se si continua a scaldare non vi è chi fermi il pistone. Poiché il volume del gas racchiuso nel cilindro cresce sempre si avrà un lavoro sempre positivo. Quindi non vi è necessità di ciclo e neppure di due sorgenti (come vedremo). Il fatto è che le macchine non possono essere infinite. E se sono finite, ad un elevarsi del pistone deve poi corrispondere un abbassarsi del medesimo percorrendo la via a ritroso. Ma, così facendo occorre fare un lavoro negativo e quindi serve una seconda sorgente ed in definitiva una trasformazione ciclica. Ma all’epoca di Carnot non ci si interessava del ritorno alla situazione di partenza puntando l’attenzione solo sulla fase attiva. L’idea di discutere tutte le fasi di un processo di scambio calore-lavoro mediante un ciclo è di Sadi Carnot influenzato in questo certamente dal padre Lazare (in realtà, al di là delle intenzioni, il ciclo di Carnot non si chiudeva anche se risulta evidente la sua chiusura. Tale evidenza sarà messa in luce da Clapeyron nel 1834, come vedremo).
Occorre poi aggiungere che l’approccio alle problematiche del calore e delle sue relazioni con il lavoro meccanico, non nasce in Carnot da interessi di tipo fisico, la voglia di migliorare una qualche teoria (ad esempio le leggi dei gas) o costruirne una nuova, ma dal desiderio di migliorare la prestazione, non di una particolare macchina termica, ma di tutte le macchine termiche, come aveva fatto suo padre Lazare per tutte le macchine idrauliche. E proprio questo voler rendere generale un risultato, conferisce ad esso un grande valore teorico. Come ho già detto, Carnot, che vale la pena sottolineare non era scienziato di professione, era profondamente impressionato da quanto avevano realizzato le macchine a vapore per lo sviluppo dell’economia inglese. Allo stesso modo guardava il ritardo francese in questo campo all’origine delle difficoltà economiche del Paese ed in ultima analisi responsabile della sconfitta di Napoleone. Dice Carnot nell’apertura delle Réflexions:
Levare oggi all’Inghilterra le sue macchine a vapore sarebbe come toglierle contemporaneamente il carbone ed il ferro; prosciugare tutte le sue fonti di ricchezza, privarla di tutti i suoi mezzi di prosperità; sarebbe come annientare questa potenza colossale. La distruzione della sua marina, che essa pure riguarda come la sua più salda base, le sarebbe forse meno funesta.
Da qui il suo studio combinato di economia politica, processi industriali, situazione materiale delle fabbriche ed officine, macchine per la produzione. In quest’ultimo settore l’Inghilterra aveva la supremazia ed era quindi qui che occorreva impegnarsi per tentare di recuperare il ritardo. Ed è naturale, come Carnot riconosce, che una invenzione nasca, e soprattutto si sviluppi e si perfezioni, là dove se ne sente più imperioso il bisogno. Le macchine termiche, come le idrauliche, vedevano continui e ripetuti miglioramenti, macchina per macchina, come invenzioni dei meccanici ed ingegneri che le realizzavano. Tutti tentativi ancora in gran parte condotti a caso. La macchina di Watt, ad esempio, aveva prestazioni 4 volte migliori di una macchina di Newcomen. Inoltre il confronto tra le varie macchine era reso difficoltoso dalla diversificazione del tipo di macchine e dalle prestazioni che a loro venivano richieste. Si era passati dalle macchine a vapore per liberare le miniere dall’acqua alle macchine utilizzate come pompe in genere, a quelle per sollevare il malto nelle birrerie, a quelle per distillare, a quelle per lavorare il ferro nelle fonderie. Mentre con le macchine idrauliche si erano fatti dei passi avanti proprio con i contributi di Lazare Carnot, nel primo quarto dell’Ottocento non vi era ancora alcun contributo che cogliesse gli elementi in gioco per rendere massima la prestazione di una macchina termica. Dove intervenire per ottenere il massimo di prestazione ? Sarebbe stato possibile andare avanti indefinitamente nel migliorare le prestazioni della macchine ? Può esistere un mezzo più efficiente del vapore, che sia utilizzabile in un motore termico? La prestazione dipende cioè dalla natura del mezzo ? E’ necessario che un motore termico abbia un’uscita e un ingresso di calore? Come è influenzata la prestazione della macchina dalla temperatura della sorgente dalla quale si estrae il calore? D’altra parte a quale ramo della scienza, fisica o chimica che fosse, occorreva far riferimento ? I rami più vicini a quanto gli ingegneri realizzavano empiricamente erano quelli calorimetrici, pneumatici e chimici con lo studio dei gas e dei vapori. Ma come connettere queste conoscenze con le macchine a vapore, tenendo conto che quei rami erano molto poco sviluppati all’epoca ? Una sola cosa si era capita con chiarezza, che le macchine a vapore ad alta pressione davano migliori risultati di quelle a bassa pressione. Ma non si capiva bene il perché. In questo senso era stata la macchina (ancora inglese) di Woolf a dare i migliori risultati, misurati in termini di lavoro fatto e combustibile consumato, cioè carbone. Questi risultati della macchina a vapore di Woolf attirarono su di essa l’attenzione di molti studiosi dei problemi connessi con le macchine termiche e, come ricorda Fox, vi furono molti lavori sulla teoria di queste macchine negli anni che vanno dal 1815 al 1825. A partire dal 1815 la Francia iniziò ad importare tali macchine dall’Inghilterra. Esse, proprio per il risparmio di carbone che realizzavano, ebbero grande successo (prima che si conoscessero i reali consumi ed i problemi di affidabilità e mantenibilità che presentavano) tanto che, a partire dal 1817, furono costruite in Francia su licenza. E’ quindi naturale, anche per questo motivo, che in quegli anni, in Francia, su queste macchine si concentrasse l’attenzione. Ma mentre si indagava questo o quel problema che presentava quella macchina, Carnot fece la grande operazione teorica di pensare ad una macchina termica che desse la massima prestazione possibile senza entrare in considerazioni d’ordine pratico. Si potrebbe dire che la sua trattazione fu di tipo deduttivo. Si pensa la migliore macchina e poi si realizzano quelle reali che dovranno funzionare tentando di avvicinarsi il più possibile alle prestazioni della migliore.
In ogni caso il suo approccio è divulgativo tanto che, lo ricordo, si servì del fratello Hippolyte per rendersi conto se i suoi scritti erano compresi da chi si occupava d’altro. Può sembrare strano che in un’epoca di formalizzazione spinta, nell’epoca in cui vi erano i Lagrange, gli Euler, i Laplace, i Poisson, i Fourier vi fosse chi rinunciava a tale formalizzazione per utilizzare metodi sintetici per avvicinare i possibili utenti di quanto descritto alla comprensione dell’argomento. Intanto la strada a questo metodo era stata aperta dal padre Lazare con il movimento geometrico, quindi, pur non avendo riscontri di quanto dico, deve aver influito su Sadi una considerazione di carattere generale. La Francia era il Paese dove da tempo vi era concentrato il maggior numero di scienziati che avevano elaborato tutta la fisica matematica più avanzata. Eppure, con questi apparati concettuali e teorici, si era realizzato poco nell’ambito degli avanzamenti produttivi, nelle applicazioni di quanto teoricamente elaborato. In Inghilterra, degli ingegneri, con preparazioni teoriche molto inferiori, erano riusciti ad ottenere risultati pratici di gran lunga più importanti, tanto da portare quel Paese all’avanguardia mondiale della produzione. Vi era certamente anche la questione della struttura sociale, chiusa in Francia da una monarchia assoluta ed aperta in Inghilterra da una impostazione liberale ed in tal senso Sadi era un fervente progressista. Ma, mentre nulla poteva per il cambiamento del sistema politico-sociale, almeno poteva indirizzare gli industriali e gli ingegneri verso una ricerca proficua per il Paese. Il lettore delle Réflexions doveva restare perplesso di fronte a questa opera che utilizzava appena l’algebra elementare, con qualche cenno di calcolo differenziale solo in una nota, quella nella quale egli formalizza la parte discorsiva precedentemente trattata e tenta di determinare la formula del rendimento di una macchina termica(3). Sembrava strano appunto che in un Paese in cui la ragione marciava di pari passo con l’analisi matematica, si rinunciasse a quest’ultima. Eppure Carnot aveva studiato dove quella matematica si apprendeva a livelli superiori e dove egli era stato alunno brillantissimo. Mancando la matematica ci si sarebbe potuti aspettare il ricorso a delle esperienze, così come erano realizzate all’epoca da Gay-Lussac, Petit, Dulong, Ampère, … In epoca positivista, poi ! Mancavano anche queste ed il riferimento era ad esperienze altrui ed a dati da tutti conosciuti. Oltre a ciò vi era quella stranezza di puntare alle differenze di temperatura (piuttosto che di pressione) tra caldaia e condensatore con conseguente caduta di calorico dalla temperatura più alta a quella più bassa. In definitiva il tutto si presentava come una sorta di trattatello di filosofia naturale piuttosto che come un trattato scientifico.
Il lavoro parte da una analogia molto in voga all’epoca, quella tra energia idraulica ed energia termica. L’analogia era però abbastanza vaga perché, ancora agli inizi dell’Ottocento, erano pochissime le macchine a vapore che trasferivano potenza a dei sistemi in moto rotatorio (in genere si utilizzava il moto alternativo occorrente per le pompe) e quindi il creare una similitudine tra una ruota idraulica (diventata turbina dopo gli studi di Claude Burdin del 1824) ed una ruota alimentata da vapore prevedeva aver conosciuta qualcuna di queste macchine o avere elaborato un possibile uso del vapore. Sono proprio del 1824 i primi tentativi che si fecero per accoppiare il moto rotativo ad una macchina a vapore. Un elemento che deve aver aiutato Carnot a questa analogia deve essere stato il condensatore separato di Watt, cioè la presenza nella macchina a vapore di una sorgente fredda, accanto alla caldaia che operava da sorgente calda. Inoltre tale separazione delle due sorgenti porta naturalmente a considerare una differenza di temperatura tra di esse ed al fatto che il lavoro che viene prodotto dalla macchina deve avere una relazione con tale differenza. La cosa era stata realizzata da Watt e quindi si sapeva che la macchina dava una maggiore prestazione con le due sorgenti ma Carnot intese questo come principio generale e non solo relativo alla soluzione di qualche problema in quella macchina. Altro elemento, al quale ho accennato, che colpì Carnot e che ebbe un suo ruolo nell’analogia tra energia idraulica ed energia termica, fu la maggiore prestazione fornita da macchine a vapore funzionanti ad alta pressione. A tutto ciò si deve aggiungere la concezione del calore che aveva Carnot, quella del calorico, cioè di una materia fluida, elastica, priva di peso ed indistruttibile. Siamo quindi, nei più diversi campi, ai limiti della conoscenza. Vi sono varie informazioni che hanno bisogno di trovare una sistemazione ed il modo in cui Carnot le raccoglierà, sistemerà e collegherà faranno di lui un indiscutibile innovatore.
Paradossalmente Carnot fu aiutato nell’elaborazione di quanto vedremo dal fatto che ancora non era stato scoperto il Primo Principio della Termodinamica o almeno l’equivalenza tra calore e lavoro di Joule-Mayer. Con la conservazione dell’energia sarebbe diventato imbarazzante avere del lavoro meccanico con un calorico che si conserva. Ed in ogni caso quell’equivalenza fa a pugni con la teoria del calorico. Il problema viene superato da Carnot assegnando al calorico una mera funzione di agente. Egli dice:
La produzione della “potenza motrice”(5) è dovuta, nelle macchine a vapore, non a un consumo reale di calorico, ma al suo trasferimento da un corpo più caldo ad uno più freddo cioè al ristabilimento del suo equilibrio
ed in tale concezione non sembra possano nascere difficoltà, ma piuttosto una specificazione che risulterà molto importante anche nelle elaborazioni di Kelvin e Planck(6). Dice infatti Carnot che per generare la potenza motrice non è sufficiente produrre il calore: bisogna anche disporre di un corpo freddo, senza il quale il calore sarebbe inutile. […] Ovunque esista una differenza di temperatura, ovunque si possa avere ristabilimento dell’equilibrio del calorico, si può avere anche produzione di forza motrice. […] Inversamente, ovunque si possa consumare questa potenza, è possibile generare una differenza di temperatura introducendo, con quest’ultima frase, da subito, uno dei temi più importanti che vedremo più oltre, quello della reversibilità del suo ciclo.
E’ a questo punto che Carnot si riallaccia ad una delle questioni più dibattute da vari anni e che aveva già trovato suo padre Lazare con una posizione netta: il rifiuto del moto perpetuo. E’ il considerare insieme sia il processo di produzione di potenza motrice a partire dal calore, sia la produzione di calore a partire dalla potenza motrice nel processo inverso, che gli permette di mostrare l’impossibilità di tale moto. Il ragionamento è semplice. Per generare forza motrice occorre trasferire una certa quantità di calore dalla sorgente calda A alla sorgente fredda B mediante le seguenti operazioni: si sottrae calorico da A per produrre vapore alla temperatura di A; si fa espandere tale vapore in un cilindro munito di pistone in modo che la sua temperatura si abbassi fino al valore della temperatura di B; si fa condensare il vapore mettendolo a contatto con B e lo si comprime fino a sua completa liquefazione. Ora invertiamo il processo. Generiamo vapore con il calorico ed alla temperatura di B, lo comprimiamo in modo da fargli acquisire la temperatura di A, infine lo condensiamo a contatto con A continuando a comprimerlo fino a sua completa liquefazione. Fatte queste premesse, Carnot conclude dicendo:
Con la nostra prima serie di operazioni, avevamo avuto contemporaneamente produzione di potenza motrice e passaggio di calorico da A a B; con la serie inversa, consumo di forza motrice e ritorno di calorico da B ad A. Ma se in entrambi i casi si è operato sulla stessa quantità di vapore e non si è avuta perdita alcuna di potenza motrice e di calorico, la quantità di potenza motrice prodotta nel primo caso sarà uguale a quella che verrà consumata nel secondo, e la quantità di calorico passata nel primo caso da A a B sarà uguale a quella che nel secondo passerà, in senso inverso, da B ad A. Si potrebbero allora ripetere indefinitamente coppie di operazioni successive di questo genere senza ottenere, nel complesso, né produzione di potenza motrice, né passaggio di calorico da un corpo all’altro.
Ora, se esistessero mezzi per impiegare il calore in modo più vantaggioso, se cioè fosse possibile, con un qualche metodo a disposizione, far produrre al calorico una quantità di potenza motrice superiore a quella da noi realizzata con la prima serie di operazioni, basterebbe sottrarre una parte di questa potenza per far risalire, con il metodo appena indicato, il calorico dal corpo B (refrigerante) al corpo A (focolare), insomma per ristabilire lo stato di cose iniziale e porsi in tal modo nella condizione di ripetere una operazione del tutto simile alla prima e via di seguito. Si otterrebbe così non soltanto il moto perpetuo, ma una creazione indefinita di forza motrice senza consumo né di calorico né di qualsivoglia altro agente. Ora, una tale creazione è assolutamente contraria alle nostre attuali concezioni e a tutte le leggi della meccanica e della buona fisica; è una ipotesi inammissibile. Si deve dunque concludere che il massimo di potenza motrice risultante dall’impiego del vapore è anche il massimo di potenza motrice realizzabile con qualsivoglia altro mezzo.
Carnot dà questa sua impossibilità di moto perpetuo come premessa alla sua elaborazione ma ci ritornerà più oltre in modo più rigoroso e dirimente proprio quando illustrerà la sua macchina termica con il suo ciclo. Ma già qui si può leggere che la macchina ché fornisce la massima prestazione è quella reversibile.
Ma torniamo ora all’analogia annunciata e seguiamola riferendoci alle figure seguenti, la prima delle quali è relativa all’acqua che, trasportando l’acqua, produce
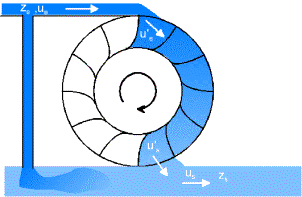
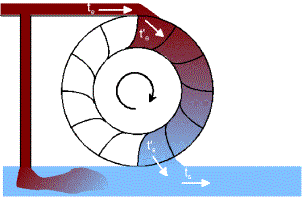
il lavoro meccanico di una ruota idraulica alimentata da sopra, acqua che cade per gravità dalla quota più alta a quella più bassa, la seconda ad una ruota (che nell’analogia di Carnot è il vapore che trasporta il calorico) fatta girare dal passaggio di calorico dalla sorgente calda alla sorgente fredda. Si deve considerare, a questo punto, il fatto che il calorico si conserva quando produce effetti meccanici, come l’acqua in una ruota idraulica, tanta ne entra quanta ne esce.
Nella macchina idraulica la potenza dipende dalla quantità d’acqua e dall’altezza di caduta. Nella macchina termica la potenza dipende dalla quantità di calorico e dalla differenza di temperatura tra i corpi attraverso cui il calorico si muove.
Nella macchina idraulica il lavoro teorico massimo, che si ha quando l’acqua agisce senza urti e senza attriti, è dato dall’equazione di Bernouilli(7):
W = m . Δ(c2/2+gz)
dove c è la velocità dell’acqua che si suppone identica prima e dopo la caduta, m è la massa d’acqua che cade, g è l’accelerazione di gravità e z è la quota. Attraverso la ruota quindi transita una quantità d’acqua data da una quota ad un’altra ed in questo passaggio si produce un lavoro.
Secondo Carnot la stessa cosa avviene nelle macchine termiche nelle quali il vapore gioca il ruolo della ruota ed il calorico quello dell’acqua: come accennato, il lavoro si origina dal passaggio del fluido calorico, mediante il vapore, dalla sorgente calda (la caldaia a temperatura t1) a quella fredda (il condensatore a temperatura t2). E come nella ruota idraulica le differenze di velocità tra ruota ed acqua originano perdite di energia meccanica, nella macchina a vapore ogni trasferimento di calorico tra le due sorgenti ed il vapore, provocherà una diminuzione dell’effetto meccanico.
Sia nel caso dell’acqua che del calorico vi sono situazioni in cui non si genera lavoro meccanico. Il trasporto diretto di calorico (come quando, dice Carnot, si riscaldano i bagni turchi mediante iniezione di vapore), corrisponde allo scorrere dell’acqua in un condotto ed in ambedue i casi non si produce lavoro meccanico.
Da ciò si deducono due cose:
– quando la temperatura della sorgente calda te è diversa da quella della sorgente fredda ts, il trasporto di calorico può produrre un effetto meccanico
– ogni scambio diretto (senza effetto utile) di calorico tra due mezzi a diverse temperature provoca una perdita rispetto al lavoro massimo ottenibile
– quindi si ha solo spreco di calorico quando esso passa da una sorgente calda ad una fredda senza produzione di lavoro meccanico
– in conseguenza il lavoro massimo si avrà quando il vapore che fa funzionare la macchina ha la stessa temperatura della caldaia quando il vapore è nella caldaia prima dell’espansione ed ha la stessa temperatura del condensatore al termine dell’operazione t’1 = t1 e t’2 = t2. Se quelle temperature non sono uguali tra loro, vuol dire che si è persa forza motrice e vi deve essere stato un flusso di calore inutilizzato.
La macchina termica pensata da Carnot è la più semplice possibile e non presenta alcuna complicazione di tipo tecnico, proprio per andare al nocciolo dei problemi senza perdersi in rivoli che distraggono.
Tale macchina doveva lavorare ciclicamente assorbendo calore da una sorgente calda per trasformarlo in effetto meccanico. Carnot capì che era impossibile realizzare un ciclo di tale fatta senza disporre di due sorgenti: una calda (da cui si preleva del calore) ed una fredda (verso cui si scarica del calore). Iniziò quindi ad ideare il miglior ciclo possibile immaginando di disporre dei seguenti strumenti ideali:
– un cilindro dentro cui scorre un pistone. Il cilindro (escludendo la sua base) deve essere perfettamente adiabatico (non deve scambiare calore con l’esterno: DQ = 0). Anche il pistone deve godere della medesima proprietà;
– una sorgente calda illimitata ed a temperatura costante t2 che possa aderire al fondo conduttore del cilindro;
– una sorgente fredda illimitata ed a temperatura costante t1che possa aderire al fondo conduttore del cilindro;
– un tappo perfettamente adiabatico in grado di aderire perfettamente al fondo conduttore del cilindro;
– tra cilindro e pistone vi è una sostanza(8) che funge da fluido operativo (può essere qualunque: solido, liquido o gas, purché sia in grado di espandersi e contrarsi). Per le sue elaborazioni Carnot si serve di aria. Dice Carnot:
Abbiamo scelto 1’aria come mezzo per realizzare la potenza motrice del calore; ma è evidente che il ragionamento vale per tutte le altre sostanze gassose, e anzi per ogni altro corpo capace di subire variazioni di temperatura per effetto di successive contrazioni e dilatazioni, proprietà comune a tutti i corpi della natura, o almeno a tutti quelli atti a sviluppare la potenza motrice del calore. Così siamo condotti a enunciare il seguente principio:
La potenza motrice del calore è indipendente dagli agenti approntati per realizzarla; la sua quantità è unicamente determinata dalle temperature dei corpi tra i quali si ha in ultima analisi il passaggio del calorico.
Carnot opera successivamente in quattro fasi che descriviamo con le sue parole e le sue figure:
Consideriamo un fluido elastico, per esempio l’aria, contenuto in un recipiente cilindrico abcd (fig. 1), munito di un diaframma mobile o pistone cd; siano inoltre due corpi A, B, ciascuno mantenuto a temperatura costante, quella di A più elevata di quella di B; immaginiamo quindi la serie di operazioni qui di seguito descritte:
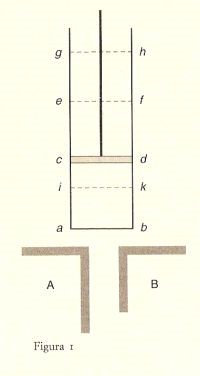
1) Contatto tra A e l’aria racchiusa nel recipiente abcd, o la parete di questo recipiente, parete che supporremo trasmettere facilmente il calorico. L’aria viene a trovarsi mediante questo contatto alla stessa temperatura di A; la posizione del pistone è a questo punto cd.
1′) Il pistone sale gradualmente e assume la posizione ef. Prosegue il contatto tra A e l’aria, che si trova in tal modo mantenuta a temperatura costante durante la rarefazione. A fornisce il calorico necessario ad assicurare questa costanza.
Questa, in due tempi, è la prima fase: l’aria di cui si serve Carnot viene fatta espandere dalla sorgente calda mettendo in contatto con essa il cilindro. Questa espansione avviene alla temperatura della sorgente calda A. Si tratta di una trasformazione isoterma.
2) A viene allontanato, e l’aria non è più a contatto con alcuna sorgente di calorico; il pistone continua però a muoversi e passa da ef a gh. L’aria si rarefà senza ricevere calorico, e la sua temperatura si abbassa. Immaginiamo che in questo modo essa diminuisca sino a diventare uguale a quella di B: il pistone allora si arresta e occupa la posizione gh.
Questa è la seconda fase che avviene con il fluido isolato dall’ambiente esterno con il quale quindi non può scambiare calore. Poiché per inerzia segue l’espansione, la temperatura del fluido-aria si abbassa fino a diventare uguale a quella della sorgente fredda B. Si tratta di una trasformazione adiabatica.
3) L’aria è posta a contatto con B, e viene compressa dal ritorno del pistone, che si riporta da gh a cd. La sua temperatura resta però costante, in virtù del suo contatto con B, cui cede calorico.
Questa è la terza fase che prevede l’inizio del ritorno verso dove era cominciato il ciclo. L’aria viene ora compressa dall’esterno dopo che il cilindro è stato messo in contatto con la sorgente fredda B. La sorgente fredda B garantisce una trasformazione a temperatura costante. Abbiamo quindi una trasformazione isoterma. Viene scaricato del calore alla sorgente fredda.
4) B viene allontanato e si continua la compressione dell’aria che, trovandosi ora isolata, subisce un incremento di temperatura. La compressione viene protratta fin quando 1’aria raggiunge la temperatura di A. Il pistone passa nel frattempo da ed a ik.
Questa è la quarta fase che prevede: l’allontanamento della sorgente fredda; la sua sostituzione con un isolante; la compressione dell’aria che avviene quindi senza scambi di calore con l’ambiente esterno e con il conseguente abbassamento della sua temperatura. Abbiamo quindi una trasformazione adiabatica.
Si ritorna così alla situazione iniziale e l’aria viene di nuovo messa in contatto con A dando inizio ad un nuovo ciclo(9).
Come già aveva annunciato, Carnot dice qui che tutte le operazioni sopra descritte possono essere eseguite in senso e ordine inverso affermando la reversibilità del suo ciclo che può quindi funzionare assorbendo lavoro meccanico per produrre calore a bassa temperatura (macchina frigorifera): Il risultato della prima serie di operazioni era stato la produzione di una certa quantità di potenza motrice e il passaggio del calorico da A a B; il risultato della serie inversa è il consumo della potenza motrice prodotta ed il ritorno del calorico da B ad A. Questa reversibilità è pensata con l’analogo che può realizzare una macchina idraulica: se si fornisce lavoro meccanico all’acqua, essa può essere sollevata fino al livello superiore(10).
Visto dall’esterno, il ciclo diretto di Carnot si realizza come se una certa quantità di calorico fosse passata dalla sorgente calda alla sorgente fredda. In tale passaggio si è prodotta una certa quantità di lavoro meccanico poiché la fase di compressione avviene, in media, a delle temperature e delle pressioni inferiori a quelle della fase di espansione.
Vi sono, naturalmente, osservazioni da fare. Si tratta di guardare almeno di sfuggita ad una macchina reale in confronto a quella che propone Carnot. Intanto si dovrà tener conto della sorgente calda che non è mai illimitata e ciò vuol dire che, quando viene utilizzato del calore, la temperatura si abbassa con la conseguenza che l’assorbimento di calore dalla sorgente calda non è mai isotermo. Più vicina alla realtà è l’idea di una sorgente di calore fredda. Basta pensare all’aria ed agli oceani. E’ quindi pensabile una compressione isoterma come descritta nel ciclo di Carnot. Altri sono le differenze tra macchina reale e macchina di Carnot: impossibilità di isolamento totale della camera del cilindro (e quindi di realizzare trasformazioni perfettamente adiabatiche); presenza di attriti; perdite varie; comportamento non lineare del fluido di lavoro; … Ebbene, ciò che in definitiva sostiene Carnot è che, assegnata una differenza di temperatura e una quantità di calore, nessun ciclo può generare più potenza motrice del ciclo ideale reversibile. Si ha quindi un riferimento non superabile per la prestazione di una macchina. Vi è ora da fare una considerazione. Quanto sostiene Carnot permette solo di scrivere delle disuguagliane e le disuguaglianze male si prestano alla trattazione mediante il calcolo differenziale. Questo problema sarà risolto da Clapeyron la cui elaborazione permetterà di scrivere delle uguaglianze. Per realizzare la migliore macchina termica, dicevo, occorrerà lavorare in modo da renderla sempre più vicina a quella di Carnot mediante trasformazioni isoterme ed adiabatiche e quindi lavorando sui componenti tecnici di essa. Oltre a ciò, come più volte detto, occorrerà disporre di sorgenti di calore a temperature differenti (maggiore è tale differenza, migliore sarà la prestazione compatibilmente, anche qui, con la tecnologia di cui si dispone) entro le quali avere un flusso di calore senza dispersioni. In tali condizioni la macchina è reversibile e non si può immaginare alcuna macchina che sia più efficiente di una macchina reversibile (in definitiva il rendimento di una macchina reale è sempre inferiore di quello di una macchina di Carnot reversibile). A tale proposito, e l’argomento ci riporta al moto perpetuo, dice Cardwell:
La dimostrazione che una macchina la quale funzioni con il ciclo divisato da Carnot sia la macchina più efficiente possibile è semplicissima. Se immaginiamo, per ipotesi, che vi sia una macchina ancor più efficiente, allora dobbiamo soltanto immaginare che questa macchina venga usata per far funzionare in senso inverso quella di Carnot e vedremo subito che il risultato sarebbe quello di restituire al corpo caldo più calore di quanto ne è stato derivato ossia, ahimè, il risultato sarà quello di far funzionare … una macchina più che perfetta! Ma in tal caso, dato che il calore si conserva sempre, la conseguenza deve essere questa: il calore si accumulerà nel corpo caldo e questo implica la possibilità di ottenere un moto perpetuo. Ma questa è un’idea, come fece osservare anche Carnot, che ripugna tanto alla scienza quanto al buon senso.
Carnot comunque pensava che i pregi delle macchine termiche dovessero essere anche altri, andando oltre la semplice ricerca del massimo risparmio di combustibile. Ce lo dice in chiusura delle Réflexions:
Non bisogna illudersi di poter mai mettere a profitto, nelle applicazioni pratiche, tutta la potenza motrice dei combustibili. Anzi cercare di avvicinarsi a questo risultato potrebbe comportare più danni che guadagni, se nel tentativo si finisse per trascurare altri importanti requisiti. Il risparmio di combustibile è solo una delle condizioni che una macchina a fuoco deve soddisfare; in molte circostanze, anzi, si tratta di una condizione secondaria, che ha un peso marginale rispetto alla sicurezza, alla solidità, alla durevolezza della macchina, ai limiti dello spazio disponibile, al basso costo d’impianto ecc.
E’ a questo punto utile chiedersi cosa fece Carnot negli 8 anni che separano le Réflexions dalla sua morte. La cosa è discussa per ipotesi, con molta attendibilità, da Fox. Il problema centrale è la teoria del calore. Carnot, dopo la pubblicazione del suo lavoro, si andò convincendo che la teoria del calorico non funzionava e che era più convincente quella sostenuta da Boyle, Euler e, vicino ai suoi tempi, da Rumford. Il calore doveva avere a che fare con una qualche agitazione termica delle molecole costituenti i corpi. In uno dei pochi frammenti degli scritti di Carnot pervenutici e ritrovati posteriormente alla sua morte, probabilmente scritto tra il 1824 ed il 1826, leggiamo delle cose che dovettero risultare un vero dramma per Carnot. Egli scrive:
Il calore non è altro che potenza motrice o piuttosto movimento che ha cambiato di forma, un movimento delle particelle dei corpi. Ovunque vi sia distruzione di potenza motrice, vi è nello stesso tempo produzione di calore in quantità esattamente proporzionale a quella della potenza motrice distrutta. E viceversa, ovunque vi sia distruzione di calore, vi è produzione di potenza motrice.
Si può dunque sostenere la seguente tesi generale: la potenza motrice è una quantità costante della natura che, a rigore, non è né prodotta né distrutta. In realtà essa cambia di forma, generando vari tipi di movimento, senza mai essere annullata.
Questo principio si deduce, per così dire, solo dalla teoria meccanica. il ragionamento ci insegna infatti che non può mai aversi perdita di forza viva o, che è lo stesso, di potenza motrice, se i corpi interagiscono senza entrare in contatto diretto, insomma senza veri urti.
Cerchiamo di capire allora perché ho usato la parola dramma. Lo faccio con le parole di Fox:
Con ogni probabilità, durante gli otto anni che gli restarono da vivere, Carnot si sentì deluso e frustrato, non tanto dall’insuccesso del libro quanto dalla sempre più chiara consapevolezza degli errori in esso contenuti. Già al momento della I redazione dell’opera, egli aveva cominciato a nutrire dubbi sulla sua teoria del calore e oggi noi sappiamo, grazie alle sue annotazioni, che prima di morire non solo prese le distanze dall’idea di calorico, ma arrivò a quella che ora riconosciamo come una versione ristretta del principio di conservazione dell’energia. Carnot in realtà giunse perfino a calcolare un valore per l’equivalente meccanico del calore, valore corrispondente a 3,7 joule per caloria, notevolmente vicino a quello di 4,2 accettato ai nostri giorni. Certo il lettore moderno è portato a dare grande risalto a una siffatta anticipazione delle conclusioni cui Joule e altri arriveranno solo negli anni quaranta dell’Ottocento. Ma io sarei incline a vedervi piuttosto un indizio della tragedia che ha segnato gli ultimi anni della vita di Sadi. Ammesso, come sembra, che egli avesse abbandonato l’ipotesi della conservazione del calore, che cosa si salvava delle Riflessioni? Per noi oggi la risposta è chiara: praticamente tutto. Ma gli stessi due insigni fisici che ne diedero dimostrazione, Lord Kelvin e Clausius, agli inizi trovarono il problema di assai ardua risoluzione.
A mio parere, anzi, Sadi non pubblicò più nulla dopo il 1824 proprio a causa delle contraddizioni che riscontrava tra il contenuto delle Riflessioni e le sue nuove vedute circa le relazioni tra calore e lavoro. Posto di fronte a tali contraddizioni, preferì tornare a quelle attività non scientifiche per le quali aveva sempre manifestato una viva curiosità. Dopo tutto, il suo atteggiamento era sempre stato quello del dilettante: non dell’ingegnere o del fisico di professione, ma della persona colta, con interessi molteplici, estesi ben al di là della fisica e della tecnologia.
LA NOTA MATEMATICA DI CARNOT
Ho appena accennato al fatto che Carnot utilizzò l’analisi matematica solo in una nota al testo delle Réflexions. E’ utile soffermarsi su questa nota perché con essa si può seguire il pensiero che ha guidato Carnot.
L’intero problema ruotava intorno ai calori specifici a pressione ed a volume costante dei gas. Carnot aveva sostenuto che essi aumentano entrambi via via che la densità del gas diminuisce, ma la loro differenza non varia. E in nota, per non dare eccessiva importanza alla cosa al fine non attaccare direttamente Poisson e Laplace che sostenevano cose diverse, specificava che, da osservazioni sperimentali di Gay Lussac e Welter, risultava che il rapporto tra calore specifico a pressione costante e quello a volume costante [il g che abbiamo già incontrato, ndr] varia molto poco con la densità del gas. In base a quanto si è appena visto, costante deve restare la differenza, non il rapporto. Ma è vero che anche il rapporto subisca piccole variazioni. Egli quindi assumeva per g, relativo all’aria, il valore (267 + 116)/267 = 1,44 (ricavato in modo non specificato) vicino a quello trovato da Gay Lussac e Welter che valeva 1,3748.
La lunga nota si apre con la dichiarazione del suo scopo (per semplicità espositiva cambio alcune espressioni e simboli):
Se si ammette la costanza del calore specifico di un gas quando il suo volume resta costante, ma varia la sua temperatura [cioè cv(t) = costante], l’analisi potrebbe condurre a stabilire una relazione tra il lavoro ed il livello termometrico. Vedremo ora in qual modo; l’occasione sarà inoltre propizia per mostrare come vadano espresse in linguaggio algebrico alcune delle leggi enunciate in precedenza.
Carnot prosegue:
Sia L la quantità di lavoro prodotta dall’ espansione di una quantità data d’aria che passa dal volume di un litro al volume di V litri, a temperatura costante. Se V aumenta della quantità infinitesima dV, L aumenterà della quantità dL, che, per la natura del lavoro, sarà uguale all’incremento dV del volume moltiplicato per la forza di espansione che il fluido elastico possiede in quel momento. Sia P questa forza di espansione, si avrà l’equazione
dL = PdV.
Con questa premessa e facendo uso della legge di Mariotte ricava per dL l’espressione:
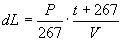
da cui, integrando ed imponendo le condizioni per ricavare la costante d’integrazione, si trova:
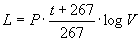
e cioè il lavoro fatto dall’espansione dell’aria lungo l’isoterma t per una variazione di volume da 1 litro a V litri.
Se ora facciamo gli stessi calcoli relativi all’isoterma t + dt, il lavoro fatto sarà:
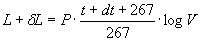
Sottraendo da questo il lavoro dell’altra isoterma si trova:
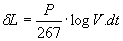
Se chiamiamo con q la quantità di calore della sorgente, impiegata per mantenere costante la temperatura del gas quando si espande, avremo che δL rappresenta il lavoro sviluppato nella caduta di q da t + dt a t.
A questo punto Carnot introduce la quantità u, lavoro sviluppato dalla caduta di una unità di calore dalla temperatura t a 0°C, che deve essere una funzione della sola temperatura, cioè u = F(t) (si noti che questa u corrisponde al rendimento che noi indichiamo oggi con h. Per essere precisi la relazione avrebbe dovuta essere u = F(Δt) ma la cosa non influisce perché Carnot fissa una temperatura a 0°C. Questa posizione corrisponde ad assumere che il rendimento dipende solo dal salto di temperatura non dipendendo, ad esempio, dal fluido operativo. Inoltre vuol dire che Carnot assume q come funzione di stato). Passando dall’isoterma t alla t + dt la u si incrementa diventando u + du = F(t + dt). La differenza di questa espressione con la precedente per u, fornisce:
du = F'(t).dt
che rappresenta evidentemente il lavoro prodotto dalla caduta di una unità di calore da t + dt a t. Se allora abbiamo la quantità di calore q invece di una sua unità, l’espressione precedente diventa:
q.du = q.F'(t).dt.
A questo punto osserviamo che avevamo già trovato un’espressione che ci dava il lavoro che si origina dalla caduta di q da t + dt a t, ed era δL. Sarà allora:
q.du = δL
da cui, ricordando quanto già ricavato, per q si trova:
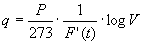
Carnot passa ora a calcolarsi il calore specifico a volume costante del suo fluido operativo, l’aria. Se s è la quantità di calore necessaria per portare l’aria dal volume di un litro e dalla temperatura di 0°C, al volume V ed alla temperatura t, allora la differenza tra s e q (che indichiamo con U) rappresenta la quantità di calore necessaria per portare la temperatura di un litro d’aria da 0° a t ed è funzione della sola t. Ponendo T = P/267.F'(t), si ha:
s = q + U = T logV + U
e, differenziando rispetto a t, otteniamo il calore specifico a volume costante dell’aria:
ds/dt = T’.logV + U’
e se, come nelle ipotesi iniziali, il calore specifico a volume costante, cioè ds/dt, è costante al variare della temperatura, allora le due quantità T’ ed U’ presenti nella relazione precedente dovranno essere indipendenti da t. Inoltre, se il calore specifico è a volume costante, vuol dire che esso non varia al variare del volume (che invece può variare al variare della temperatura). Da quanto detto, Carnot ricava la seguente conclusione:
Se si suppone il calore specifico costante a tutte le temperature […], la quantità ds/dt sarà indipendente da t ; e, al fine di soddisfare l’ultima equazione scritta per due valori particolari di V, sarà necessario che T’ ed U’ siano indipendenti da t: avremo dunque T’ = C, quantità costante.
Essendo T = C, si possono moltiplicare ambedue i membri per dt ed integrare. Si trova:
T’.dt = C.dt → T = C.t + C1
dove C1 è una costante. Ricordando ora quanto avevamo posto, e cioè T = P/267.F'(t), abbiamo che:
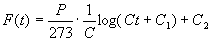
da cui integrando si trova:
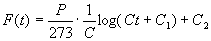
Considerando che F(t) = 0 per t = 0 e cambiando nome alle costanti, si ha:
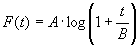
Ricordando che F(t) è ciò che oggi conosciamo come il rendimento η di una macchina termica, con questo risultato, dice Carnot, saremmo in condizione di valutare il lavoro sviluppato da una qualunque caduta di calore. Ma il risultato è vincolato dall’ipotesi di costanza del calore specifico di un gas a volume costante, ipotesi non ancora verificata soddisfacentemente dall’esperienza. Da ciò consegue che tale risultato lo si può accettare solo per un intervallo ristretto di temperature.
E’ indispensabile osservare che il fattore 1/C che incontreremo quando parlerò di Clapeyron, coincide con la F(t) di Carnot.
PRIMA ELABORAZIONE ANALITICA DELLE RÉFLEXIONS: CLAPEYRON
Come già accennato, il lavoro di Carnot passò inosservato e lo restò per 10 anni, finché non fu ripreso daBenoît Paul Émile Clapeyron (1799 – 1864), che fu, dopo aver frequentato il Collège de Juilly tra il 1808 ed il 1814, alunno dell’École Polytechnique tra il 1815 ed il 1818 (quando Carnot ne era uscito nel 1814) e quindi per due anni studente dell’École des Mines. Nel 1820 si recò a San Pietroburgo, nella Russia zarista, per insegnare alla Scuola dei Trasporti, dove nel 1823 gli fu assegnato un corso di Meccanica applicata (con capitoli dedicati ai motori temici ed all’idraulica). Qui si occuperà di questioni ingegneristiche, come la costruzione di ponti e di ferrovie, ma anche di questioni teoriche come i problemi connessi con l’elasticità dei materiali e quelli relativi alle macchine termiche. La rivoluzione del 1830 in Francia rese difficili i rapporti diplomatici con la Russia e Clapeyron, di convinzioni repubblicane, tornò in Francia (1831) dove fu nominato membro del Corps royal des Mines e, a partire dal 1844, insegnante all’École nationale des ponts et chaussées (fu progettista supervisore della prima ferrovia francese che collegava Parigi a Versailles e quindi di quella che collegava Parigi a Saint Germain). Iniziò ad occuparsi delle questioni più attuali, tra cui i problemi connessi con il calore. Egli, dopo aver studiato il calore latente nei cambiamenti di stato dei corpi puri, pubblicò sul Journal de l’École Royale Polytechnique, la sua Mémoire sur la puissance motrice de la chaleur (nel 1837 tradotta in inglese e nel 1843 in tedesco). Il lavoro è stato pubblicato nel 1834 ma sembra fosse già pronto nel 1832, l’anno della morte di Carnot, ma non pubblicato perché nella commissione che decideva per la pubblicazione vi era un Poisson decisamente contrario. In esso vengono riprese esplicitamente le Réflexions con la medesima ammissione di conservazione della quantità di calore Q che, quando contenuta in un gas o vapore, deve essere una funzione di stato e cioè funzione solo della pressione P e volume V. Riguardo alla natura del calore, rimanendo nel vago sulla sua natura microscopico, dice Clapeyron:
Una quantità di azione meccanica ed una quantità di calore che può passare da un corpo caldo a uno freddo sono quantità della stessa natura, e che è possibile sostituirle l’una con l’altra.

In questa memoria, Clapeyron presentò i lavori di Carnot, mostrando tra l’altro che il suo ciclo era chiuso, scritti in modo che non fossero più disprezzati dagli addetti ai lavori. Il tutto era tradotto in modo analitico e sostenuto da grafici su un piano pressione-volume (piano di Clapeyron). Da notare che il voler rendere visibile il ciclo su un piano derivava dalla conoscenza che Clapeyron aveva dell’indicatore di Watt(11).
Occorre ora osservare che in Clapeyron vi è una sorta di timore ad usare il calore Q perché non riusciva a comprenderlo come funzione matematica. Si avvicina però ad esso utilizzando un simbolismo matematico che rende Q funzione di pressione P, volume V, con la consapevolezza dello stretto legame che P e V hanno con la temperatura t, attraverso le leggi dei gas note. Per le sue elaborazioni, infatti, Clapeyron utilizzò la legge di Boyle – Mariotte, secondo la quale il prodotto della pressione per il volume di un gas ad una data temperatura è costante [P.V = costante], e le leggi di Volta – Gay Lussac, le quali ci forniscono l’andamento della pressione e del volume al variare della temperatura [P = Po/267(t + 267); V = Vo/267(t + 267)]. Mettendo insieme queste leggi Clapeyron ricavò per primo quella che oggi conosciamo come equazione di stato dei gas, un’equazione che lega pressione, volume e temperatura:
P.V = R.(t + 267)
con:
R = PoVo /(t0 + 267)
Scriveva Clapeyron:
I differenti stati nei quali una data massa gassosa può esistere sono caratterizzati da volume, pressione, temperatura e quantità assoluta di calore in essa contenute; se due di queste quattro quantità sono note, le altre due sono determinate.
Questa legge ci fornisce l’opportunità di rappresentare rigorosamente le isoterme del ciclo di Carnot su un piano P-V e le isoterme in tale piano saranno delle iperboli. Fissata cioè una temperatura centigrada, le equazioni delle iperboli saranno date da PV = costante. Per ciò che riguarda le adiabatiche la cosa era più complessa e Clapeyron le tracciò approssimativamente. Seguiamo la traccia dei suoi ragionamenti.
Egli considera, nel piano P-V, le due isoterme e le due adiabatiche che costituiscono il ciclo di Carnot. Considera queste curve per un incremento infinitesimo di temperatura, nell’ambito cioè di sicura validità delle ipotesi di Carnot (piccola variazione di temperatura, come osservato alla fine del paragrafo sulla nota matematica). Considera quindi due isoterme A’B’ (alla temperatura t + dt) e BA (alla temperatura t) e le adiabatiche AA’ e B’B che chiudono il ciclo. Il ciclo completo sarà AA’BB’ e risulterà infinitesimo. L’area di tale ciclo viene approssimata da Clapeyron all’area di un parallelogramma con lati AB ed A’B’ (paralleli all’asse V e quindi con differenza d’ordinate dP) e BB’ ed AA’ (paralleli all’asse P e con differenza d’ascisse dV). Aiutiamoci con un disegno.
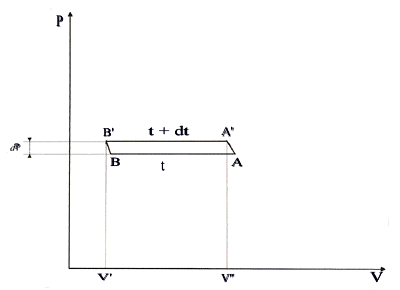
Per calcolare l’area del parallelogramma occorre calcolarsi dP (differenziando l’ultima legge scritta tenendo conto che, nell’approssimazione fatta, il volume è costante):
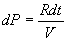
Moltiplicando questa espressione per la variazione di volume dV (che non dipende dalla temperatura), si trova l’area richiesta:
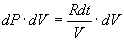
A questo punto interviene la quantità di calore q che cade da t + dt a t. Clapeyron considera che il lavoro infinitesimo dP.dV (ottenuto dal ciclo in considerazione) è dovuto al fatto che vi è identità tra la quantità di calore q’ spesa sull’isoterma A’B’ ed il calore q restituito lungo l’isoterma BA; a tale lavoro infinitesimo è quindi originato dal passaggio di una medesima quantità di calore q dall’isoterma t + dt all’isoterma t.
La quantità di calore q è parte infinitesima del calore Q in gioco in un ciclo non infinitesimo e quindi sarà data dal differenziale totale di Q rispetto alle P e V in gioco, legate tra loro dall’equazione PV = costante. Abbiamo allora:
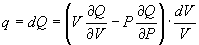
Se vogliamo ora conoscere il lavoro infinitesimo, dP.dV, per unità di di calore trasferito, dQ, dobbiamo operare il quoziente dP.dV/dQ (che rappresenta il rendimento infinitesimo del ciclo), ottenendo:
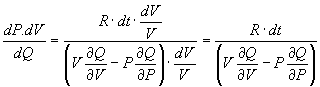
Clapeyron dice, senza giustificazioni sufficienti, che il denominatore di questa espressione deve essere una funzione della temperatura t e quindi del prodotto P.V. (12)
Se il denominatore dQ è funzione di t, il calore Q dovrà essere un’equazione differenziale alle derivate parziali del tipo:
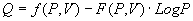
oppure del tipo:
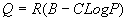
dove B e C sono funzioni della temperatura, da determinare. In particolare, Clapeyron riteneva che C fosse legata al calore latente per unità di volume. Nel suo complesso questa relazione non era corretta perché basata su dati sperimentali non accuratamente ricavati da Delaroche e Bérard(13). Essa non forniva la corretta relazione esistente tra pressione e calori specifici (all’epoca era praticamente impossibile avere informazioni sperimentali esatte su questo punto). C’è da osservare che il rapporto tra il lavoro utile che la macchina riesce a compiere ed il calore totale assorbito dal sistema, cioè il rendimento, per Clapeyron si riduce a dt/C. Dice Clapeyron:
La funzione C ha molta importanza(14); essa è indipendente dalla natura del gas, ed è funzione della sola temperatura; essa è essenzialmente positiva e serve da misura per la quantità massima di lavoro che può sviluppare il calore
inoltre la funzione C:
lega insieme tutti i fenomeni prodotti dal calore su corpi solidi, liquidi e gassosi; sarebbe auspicabile che esperienze molto accurate, come quelle sulla propagazione del suono nei gas a differenti temperature, determinassero questa funzione con ogni precisione possibile; essa servirebbe per determinare molti altri aspetti importanti della teoria del calore, rispetto ai quali l’esperienza non conduce che a delle approssimazioni insufficienti, o sui quali essa non ha ancora scoperto nulla.
Clapeyron riuscì a calcolare C per varie temperature e, dal suo andamento, a capire che l’effetto prodotto dal calore diminuisce alle alte temperature, anche se in una maniera molto lenta. Ciò rappresentava una conferma della teoria di Carnot secondo la quale il lavoro prodotto dal passaggio di una unità di calore attraverso una differenza di temperatura di un grado, diminuisce con l’aumento della temperatura. Ma C non era l’unica funzione da determinare. Vi era anche la B, a proposito della quale dice Clapeyron che può variare da un gas all’altro ma è probabile che sia la medesima per i gas semplici. Con i dati sperimentali disponibili ed un gran lavoro di elaborazione matematica, Clapeyron disegnò, come mostrato in figura, il ciclo di Carnot.
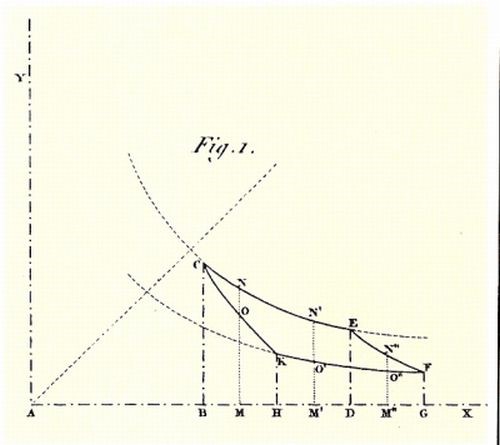
Ciclo di Carnot, realizzato da Clapeyron (in ascisse vi è il volume ed in ordinate la pressione; l’isoterma EC è a temperatura t1, quella FK è a temperatura t2). Per quel che riguarda le adiabatiche si osservi solo che, a partire dall’equazione di Poisson (PVg = costante), si ricava facilmente la loro maggiore pendenza rispetto alle isoterme, osservando che l’esponente g è un numero sempre positivo e maggiore dell’unità.
Analogamente a quanto mostrato per il ciclo infinitesimo, una caratteristica importante di questo diagramma è che l’area sottesa dal ciclo così disegnato, rappresenta direttamente il lavoro meccanico prodotto durante il ciclo(15) (basta solo osservare che un’area su un piano P-V è dimensionalmente un lavoro):
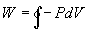
Calcolando questo integrale, Clapeyron stabilisce che il rendimento di una macchina di Carnot si può esprimere nella forma seguente
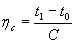
dove ηc è il rendimento, t1 è la temperatura dell’isoterma alla temperatura della sorgente calda e t2quella della sorgente fredda, C è quella funzione della temperatura della quale ho detto. E’ d’interesse osservare che le successive misure di Henri Victor Regnault (1810 – 1878) e le elaborazioni di William Thomson, il futuro Kelvin (1824 – 1907), che lavorò con Regnault, hanno permesso di stabilire che 1/C ha lo stesso significato di J/T, dove J è l’equivalente meccanico di Joule e T è la temperatura assoluta (1/C corrisponde al rendimento F(t) calcolato da Carnot). Si può osservare, in modo molto qualitativo, che il rendimento risulta indipendente dal fluido operativo, dipendente dalla differenza di temperature tra le due sorgenti e tanto maggiore quanto maggiore è la differenza tra le due temperature. Più in generale Clapeyron ebbe il merito di enunciare esplicitamente a livello macroscopico il principio di equivalenza tra il passaggio di una quantità di calore e il lavoro prodotto, enunciato che in Carnot era implicito quando discuteva del rendimento teorico di una caloria.
Come si può a margine osservare, il ciclo di Clapeyron è chiuso mentre non lo sembrava quello di Carnot. E’ lo stesso Carnot che dice: Nell’ipotesi di un ridottissimo scarto tra le temperature di A e B […] essendo i movimenti del pistone assai piccoli durante le operazioni 3 e 5 [le adiabatiche, ndr], queste avrebbero potute essere soppresse senza influenza sensibile sulla produzione di potenza motrice. In effetti, poiché variazioni minime di volume possono solo produrre piccolissime variazioni di temperatura, le suddette variazioni di volume sono trascurabili rispetto a quelle delle operazioni 4 e 6 [le isoterme, ndr] in cui l’ampiezza è aumentabile a piacere.
Questo ragionamento è ineccepibile. Diventa errato quando lo si estrapola ad un ciclo non più infinitesimo anche se, per fortuna, alla fine, i risultati non solo pratici ma anche analitici gli danno ragione sul contributo delle due adiabatiche (ma non sulla reversibilità del ciclo che con l’uso di isocore in luogo di adiabatiche risulta irreversibile).
Vediamo in breve come stanno le cose.
Leggendo Carnot ci si rende conto che egli trascura coscientemente il contributo delle adiabatiche per calcolare il rendimento del suo ciclo. Qui sembra risulti evidente l’influenza del padre Lazare ed il suo movimento geometrico, un metodo sintetico (introduzione e successiva soppressione di variabili ausiliarie) per sostituire il calcolo differenziale. Sadi non è in grado di calcolare con esattezza l’espressione di una adiabatica. Il calcolo differenziale assume in lui la funzione di uno strumento potente ma pratico di indagine e non certo un qualcosa di sublime come era considerato da tutti all’epoca. Non gli interessa la purezza del calcolo, la sua completezza, ma solo il risultato. Carnot lavora quindi con un ciclo infinitesimo ed in tale ciclo, le due adiabatiche sono sovrapponibili, in pratica, a due isocore (osservo che le isocore non permetterebbero al ciclo di essere reversibile ma in un ciclo infinitesimo non pongono questo problema). Inoltre, nel ciclo, le adiabatiche danno contributi opposti alla quantità di lavoro rappresentata dal ciclo e, quindi, si compensano dando un contributo complessivo nullo. Ebbene, queste adiabatiche, ma Carnot non lo dice esplicitamente, sono considerate solo come variabili ausiliarie utili per sviluppare il ragionamento del metodo sintetico e poi soppresse perché inutili, in quanto la loro somma è zero (questo modo di operare farebbe inorridire un purista dell’analisi matematica). Ebbene, pare evidente che Sadi non abbia soppresso le adiabatiche perché, come ho già detto a sufficienza, il suo lavoro non si rivolgeva ai raffinatissimi scienziati analisti e fisico-matematici del suo tempo ma agli operatori sul campo delle macchine termiche. In quest’ottica pratica era inutile il perfezionismo del calcolo, contando solo il risultato. Ciò che ha fatto Clapeyron, che invece come ho anche qui detto lavora con l’analisi più formale proprio per dare dignità al lavoro di Carnot, non può dimenticare le due adiabatiche e, dopo averle calcolate, le considera come curve che chiudono il ciclo.
Clapeyron dette anche contributi ulteriori alla chiarificazione e divulgazione dei lavori di Carnot. Essendosi recato in Inghilterra nel 1836 per acquistare delle locomotive, fece esperienza con le macchine a vapore, più di officina che di laboratorio come egli stesso raccontò, tale da aggiungere contributi alle sue precedenti elaborazioni del 1834. Nel 1842 presentò, all’Accademia delle Scienze di Parigi, un memoria, Mémoire sur le règlement des tiroirs dans les machines à vapeur, il cui fine era proporre delle migliorie al funzionamento del cassetto di distribuzione del vapore in una macchina a vapore(16). Questa memoria gli dette notorietà presso gli ingegneri ed in essa egli non nominò Carnot (forse questo fu il motivo del successo) perché quella teoria era lontanissima dal mondo delle officine in cui si realizzavano macchine a vapore. Forte dell’esperienza nelle officine, Clapeyron tornò a Carnot nel 1851 e nel 1853 e non in una o più memorie ma nelle sue dispense per il corso di macchine a vapore all’École nationale des ponts et chaussées. Ritornò al calcolo di C utilizzando nuovi risultati sperimentali molto accurati di Regnault e abbandonò definitivamente (1853) l’idea di calorico indistruttibile.
Ma già siamo in un’epoca in cui si erano avuti i fondamentali contributi sulla relazione esistente tra lavoro meccanico e calore di Kelvin, Clausius, Joule. Mayer … . Su di essi mi soffermerò in un prossimo articolo.
Roberto Renzetti
NOTE
(1) Suo fratello era Lazare Hippolyte Carnot (1801 – 1886) che fece carriera in politica come accadrà per il figlio di Hippolite, Marie François Sadi Carnot (1837 – 1894) che diventerà Presidente della Repubblica francese (1887 – 1894) e finirà ucciso dall’ anarchico italiano Sante Geronimo Caserio.
(2) Questo lavoro si occupava delle relazioni esistenti tra lavoro e delineava il primo principio della termodinamica. Esso fu pubblicato nel 1878 da suo fratello Hippolyte, che lo integrò con notizie biografiche su Sadi, Notice biographique sur Sadi Carnot. Il tutto sarà pubblicato negli Atti della R Academia delle scienze di Torino 4 (1868), 151-170, e successivamente inserito in una edizione delle Reflexions di Gauthiers-Villars (1878). Era troppo tardi perché potesse avere una qualche influenza sugli sviluppi della termodinamica. Per leggere il lavoro inedito di Sadi Carnot si può andare a:
Per leggere gli appunti inediti si può andare a:
Per leggere infine le note biografiche di Sadi, scritte da Hippolyte, si può andare a:
(3) Tratterò diffusamente la nota matematica di Carnot più oltre.
(4) A proposito delle influenze di Clément su Carnot, leggiamo cosa dice Fox:
Solo recentemente, in particolare grazie alla scoperta di due serie di appunti presi nel corso delle conferenze tenute da Clément durante gli anni venti, si è potuto ricostruire il debito di Sadi nei suoi confronti. Questi appunti, se confrontati con il testo redatto da Clément nell’agosto 1819 in collaborazione con Desorrmes, indicano chiaramente che egli lavorava alla elaborazione di una teoria delle macchine termiche nello stesso periodo in cui Carnot cominciava a interessarsi di questo problema. Ma il loro significato va ben al di là di questa coincidenza. Le somiglianze tra l’impostazione di Clément e quella di Carnot, somiglianze che si manifestano sia nella struttura generale che nei dettagli delle loro teorie, suggeriscono in modo cogente che Clément ha esercitato una influenza decisiva su Sadi. Anzitutto nella struttura generale. Le conferenze di Clément e il testo del 1819 che abbiamo appena menzionato sono privi di apparati matematici complessi e, come nelle Riflessioni, i calcoli che vi compaiono, ad esempio quelli relativi al funzionamento di varie macchine, sono puramente aritmetici. Inoltre, al pari di Carnot – e al contrario per esempio di Hachette – Clément si interessa di un modello ideale, non del funzionamento delle macchine reali. Il suo problema coincide dunque con quello affrontato nelle Riflessioni: quale è il rendimento massimo che si può ottenere a partire da una quantità data di calore, fatta astrazione da tutte le difficoltà pratiche? In piena coerenza con questa impostazione, Clément – come Carnot e alcuni altri loro contemporanei – non si cura granché del notevole scarto riscontrabile tra le previsioni teoriche, relative alle macchine a vapore ad alta e media pressione, e le prestazioni reali: il problema di accordare la teoria all’ esperienza non doveva essere, per lui, sollevato in via preliminare, ma lasciato a un’ analisi successiva.
(5) Carnot introduce questa espressione nelle prime pagine del suo lavoro e la precisa in nota nel modo seguente:
Ci serviamo qui dell’espressione “potenza motrice” per designare l’effetto utile che un motore è capace di produrre. Come si sa, la misura di questo effetto, che è assimilabile al sollevamento di un peso a una certa altezza dal suolo, è data dal prodotto del peso per l’altezza a cui si suppone innalzato.
L’unità di misura per questa grandezza utilizzata da Carnot è un metro cubo d’acqua (1000 Kg) sollevato di un metro.
(6) L’enunciato del Secondo Principio della Termodinamica di Kelvin-Planck afferma: è impossibile realizzare una trasformazione il cui unico risultato preveda che tutto il calore assorbito da una sorgente omogenea sia interamente trasformato in lavoro.
(7) In un mulino ad acqua, la ruota fa passare l’acqua da un potenziale ce2/2+gze ad un potenziale cs2/2+gzs. Il lavoro massimo corrisponde quindi al funzionamento senza urti (ce = c’e et cs = c’s) ed è uguale a D(c2/2+gz ). Ogni differenza di velocità provocherà una perdita in rapporto al lavoro massimo.
(8) Anche sul fluido operativo vi è una grande novità introdotta da Carnot: esso può essere qualunque. Ai primi dell’Ottocento non vi era un accordo generalizzato sull’economicità dell’uso del vapore come fluido operativo nelle macchine termiche ma pochi ne ipotizzavano altri per la difficoltà di operare con essi. Nel 1818 da Alexis-Thérèse Petit, che era stato ripetitore di Carnot all’École, era stata avanzata la possibilità di usare aria nelle macchine termiche in quanto questa da alcuni calcoli teorici fatti da Petit, avrebbe garantito una economia di combustibile 4 volte più elevata rispetto al vapore. Ma il vapore aveva un pregio che sembrava insuperabile: facendo bollire acqua a pressione atmosferica, con ordinari aumenti di temperatura, essa si converte in vapore con una espansione in volume di 1800 volte. Se poi un tale vapore lo si costringe un determinato volume, si ottengono facilmente pressioni enormi. Con una macchina termica ad aria, nelle stesse condizioni di pressione e temperatura, si avrebbe un’espansione di circa un terzo con ridotti aumenti di pressione. Ma da questi supposti vantaggi Carnot partì per ribaltare le cose. Leggiamolo nelle parole di Cardwell:
Questa fu la magnifica intuizione di Camot: egli comprese che quello che era stato, fino ai suoi tempi, il grande pregio del vapore acqueo – la sua proprietà di una enorme espansione volumetrica o di un tremendo aumento di pressione mediante un modesto aumento di temperatura ossia la proprietà che aveva reso possibile far funzionare le macchine di Newcomen, di Watt, di Trevithick e di Woolf – doveva dimostrarsi in futuro un difetto. Il solo fatto che la pressione cresceva molto più rapidamente della temperatura implicava necessariamente una conseguenza: sarebbe stato molto più difficile imbrigliare tutto il divario di temperatura corrente tra i mille gradi del carbone ardente e la temperatura dell’acqua fredda o dell’atmosfera. […] Questa forse fu l’intuizione più penetrante e più stimolante di tutta la storia della tecnologia. È arduo trovare qualcosa che le si possa paragonare e che abbia gli stessi pregi. […] Fu l’intuizione di Carnot a portare direttamente alla fabbricazione delle macchine ad aria di altissimo rendimento messe a punto verso la fine del secolo.
tra cui i motori a combustione interna a partire da quello realizzato da Lenoir nel 1859, quindi a quello di Otto che lo scippò ai nostri Matteucci e Barsanti. Tali motori eliminano la necessità della caldaia e del condensatore, in quanto è di normale uso l’atmosfera per scaricare il calore residuo dell’aria (questo sistema di scarico nell’atmosfera era conosciuto da Carnot perché utilizzato nelle macchine a vapore ad alta pressione di Trevithick). L’insieme di queste proprietà permise di realizzare macchine sempre più piccole e trasportabili (ad esempio, permise la realizzazione della locomotiva a vapore che, appunto, usa l’atmosfera come condensatore).
E Carnot scriveva:
Uno degli inconvenienti più gravi del vapore è la necessità di impiegare, ad alte temperature, contenitori di resistenza straordinaria. Questi non sono invece indispensabili nel caso dell’aria, per la quale non esiste un rapporto diretto tra forza elastica e temperatura. L’aria sembrerebbe dunque più adatta del vapore a realizzare la potenza motrice di cadute del calorico nei livelli elevati di temperatura, mentre in quelli inferiori il vapore acqueo è forse più adeguato. Si potrebbe anche concepire la possibilità di far agire lo stesso calore successivamente sull’aria e sul vapore acqueo. Basterebbe, a questo scopo, mantenere l’aria, dopo il suo impiego, a una temperatura elevata e, anziché espellerla subito nell’atmosfera, farle avvolgere una caldaia a vapore, come se provenisse direttamente da un focolare.
L’impiego dell’aria per lo sviluppo della potenza motrice del calore presenterebbe, in pratica, difficoltà molto grandi, ma forse non insormontabili; se si riuscisse a superarle, offrirebbe senza dubbio una notevole convenienza nei confronti del vapore acqueo.
Vi è un altro aspetto che va discusso brevemente e relativo al fatto che il libro di Carnot non fu letto. L’affermazione che Carnot fa e cioè che, indipendente dal tipo di isoterma (compressione o espansione), il calore assorbito o emesso è indipendente dalla natura del gas, avrebbe dovuto provocare delle reazioni di riprovazione che invece non vi furono. Ciò è per Fox la dimostrazione che i fisici non avevano letto quel libro e lo avevano guardato con supponenza e benevolenza quasi volendo dire, bene bene ma non farci perdere tempo con questi trattatelli divulgativi di cose stranote. Ed a riprova c’è un fatto significativo. Quanto sostenuto da Carnot, venne dimostrato sperimentalmente nel 1828 da Dulong. Quest’ultimo comunicò i suoi risultati all’Accademia delle Scienze senza citare il nome di Carnot. E non si trattava di voler sostenere una qualche priorità, perché 4 anni prima in quella stessa Accademia era stato presentato il lavoro di Carnot e, anche se il passo specifico non era stato citato, il dubbio a chi annunciava la nuova scoperta poteva venire e con il dubbio la paura di una brutta figura visto che l’uditorio era più o meno lo stesso ed il libro di Carnot qualcuno lo avrebbe potuto aver letto.
(9)Non riporto qui i grafici del ciclo per non andare oltre quanto fece Carnot. Ma chi vuol seguire il ciclo con le notazioni introdotte da Clapeyron nel 1834 e con altri concetti come la temperatura assoluta introdotta ancora successivamente, può farlo leggendo il mio l’articolo Macchine termiche e cicli termodinamici.
(10) E’ ciò che ordinariamente avviene nel funzionamento delle pompe idrauliche. Non serve comunque andare ad esemplificare con prodotti tecnologici relativamente recenti. Il sistema era noto fin dalla remota antichità per sollevare l’acqua dai fiumi e farla servire, ad esempio, per irrigazione dei campi. La figura
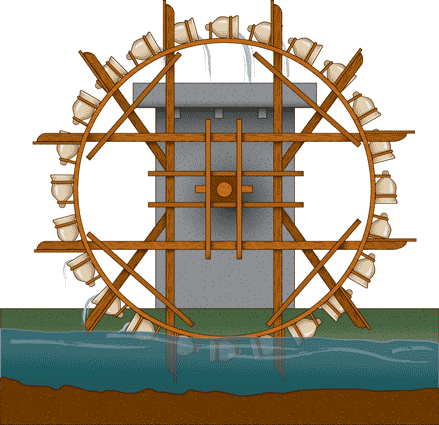
illustra un tale sistema chiamato noria (il modello di figura è di origine persiana). La stessa energia dell’acqua corrente del fiume mette in moto la ruota idraulica. Ad essa sono fissate dei recipienti che, mano a mano che avviene la rotazione della ruota, si riempiono d’acqua dal fiume, acqua che poi lasciano cadere in un recipiente a livello superiore, recipiente che potrà poi essere connesso con dei canali per irrigazione. Nel caso in cui l’acqua si dovesse prelevare da un lago, occorrerebbe far ruotare la ruota mediante applicazione di lavoro meccanico (sforzo muscolare).
(11) L’indicatore di Watt è un meccanismo che lo stesso Watt pensò. Mentre il pistone fa i suoi movimenti nel cilindro, vi è un sistema meccanico (un piccolo cilindro in cui scorre un pistone con cui è solidale una matita; il moto del pistone è originato dalla pressione che gli viene trasmessa dalla camera in cui vi è il fluido operativo della macchina ed è regolato da una molla) collegato alla camera in cui vi è il fluido che disegna materialmente su della carta il ciclo termodinamico che si va realizzando su un piano P-V. Il lavoro utile è quello disponibile sull’albero della motrice ed è un po’ minore di quello che si misura nel cilindro per mezzo
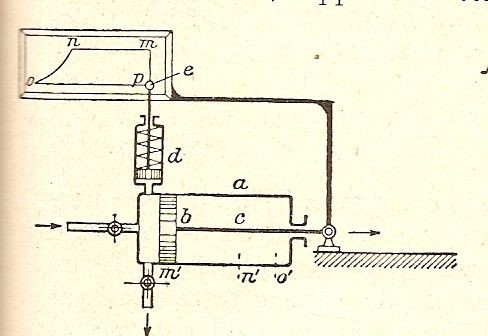
L’indicatore di Watt mentre disegna il diagramma del ciclo realizzato dal pistone in moto alternativo nel cilindro.
dell’indicatore della pressione, a causa delle perdite dovute all’attrito degli organi di trasmissione. Con l’indicatore suddetto si fanno disegnare alla macchina dei diagrammi, le cui ascisse sono proporzionali alle corse dello stantuffo (e quindi al volume utile della camera in quell’istante) e le ordinate corrispondenti alle pressioni del vapore, cosicché l’area che ciascuno racchiude rappresenti il detto lavoro.
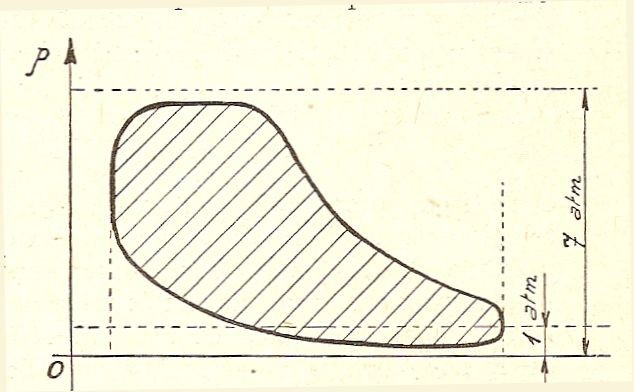
Il diagramma sul piano P-V fornito dall’indicatore di Watt.
L’indicatore della pressione è un cilindretto che si fa comunicare con una delle basi del cilindro, supponiamo con quella superiore. Il vapore che s’introduce in questa parte preme contro il pistone dello strumento, mentre alla sua corsa si oppone la forza elastica di una molla, la cui deformazione è proporzionale alla pressione effettiva. Allo stantuffo è unita un’asticella fornita all’estremità di una matita, la punta della quale poggia su un foglio di carta; la matita traccia sul foglio in moto un diagramma; la cui area, come si è detto, misurerà il lavoro compiuto dal pistone del cilindro in un movimento d’andata e di ritorno.
(12) La cosa sarà mostrata da M. Ferdinand Reech (1805 – 1884) nella sua Théorie générale des effets dynamiques de la chaleur del 1854.

(13) Vi è da osservare che siamo in pieno periodo positivista che suona come una sorta di condanna per l’elaborazione teorica. Serviva ad ogni istante un confronto con l’esperienza a rischio di non vedersi considerato il lavoro. E’ quanto, ad esempio, successe a Sadi Carnot.
(14) La C sarà utilizzata da Kelvin per ottenere il rapporto tra la temperatura assoluta e l’equivalente meccanico della caloria. Con tale funzione Clapeyron andrà oltre ricavando, dalla relazione Q = R(B – C LogP), la legge che mette in relazione la compressione e la dilatazione, a temperatura costante, di un volume di gas con la quantità di calore assorbita o liberata. Inoltre riesce a determinare in accordo con i dati sperimentali, la differenza tra i calori specifici dei gas a pressione e volume costante, sempre con una dipendenza da C:
(15) Per una discussione più completa su quanto qui detto si può vedere la nota 3 del mio articolo Macchine termiche e cicli termodinamici.
(16) Si veda in proposito il mio Macchine termiche e cicli termodinamici, citato.
BIBLIOGRAFIA
(1) Sadi Carnot – La potenza del fuoco – Bollati Boringhieri 1992.
(2) Robert Fox – Introduzione a La potenza del fuoco di Sadi Carnot – Bollati Boringhieri 1992.
(3) Fabio Sebastiani – I fluidi imponderabili – Dedalo 1990.
(4) Donald S. L. Cardwell – Tecnologia, scienza e storia – il Mulino 1976.
(5) Charles Singer (a cura di) – Storia della tecnologia – Boringhieri 1964.
(6) AA. VV. – Scienziati e tecnologi (dalle origini al 1875) – Mondadori 1975.
(7) René Taton (diretta da) – Storia generale delle scienze – Casini 1965.
(8) S. S. Wilson – Sadi Carnot – Le Scienze n° 158, Ottobre 1981.
(9) Mario Gliozzi – Storia della fisica – in Storia delle Scienze, UTET 1965.
(10) http://neveu.pierre.free.fr/enseign/thermo/chap1.htm
(11) A. Baracca, A. Rossi – Materia e Energia – Feltrinelli 1978.
(12) Ilya Prigogine, Isabelle Stengers – La Nuova Alleanza – Einaudi 1993
(13) Thomas S. Kuhn – La tensione essenziale – Einaudi 1985.
(14) http://www.history.rochester.edu/steam/carnot/1943/ . In questo sito in lingua inglese vi è molto materiale su Sadi Carnot. Tra esso vi sono le Reflexions e la vita di Carnot scritta dal fratello Hippolyte.
(15) P. Redondi – L’accueil des idées de Sadi Carnot et la technologie française de 1820 à 1860 – Vrin, Paris 1980.
Categorie:Fisica e Storia della Fisica
Rispondi