ATOMI: Il principio di Pauli. Orbitali atomici. Campo self-consistente. Le regole di Hund ed il principio di aufbau. Il modello atomico attuale.
Abbiamo, a questo punto, quasi tutte le carte in mano per costruire un atomo.
Aiutati dall’esperienza andiamo allora a vedere come si dispongono gli elettroni di un atomo.
Fin’ora abbiamo volutamente trattato l’atomo senza far riferimento al numero degli elettroni in gioco.
Cominciamo col dire che ogni elettrone in un atomo è caratterizzato dai quattro numeri quantici che abbiamo or ora visti. Poiché, poi, ogni elettrone tende in natura allo stato di energia minore (cioè al livello energetico più basso) e questo è per l’atomo con un solo elettrone il livello con numero quantico principale n=1 e con numero quantico secondario l=0 (cioè il livello 1s), si potrebbe pensare che tutti gli elettroni dell’atomo siano normalmente nel livello 1s. Ma ciò è in completo contrasto con l’esperienza.
In molti anni infatti si raccolsero una infinità di dati sul comportamento degli atomi portandoli dal livello ad energia più basso ai successivi livelli energetici. Mediante la spettroscopia si studiava il comportamento di questi atomi, si catalogavano i risultati, senza riuscire a sapere come stessero in realtà le cose. Sta di fatto che l’esperienza contraddiceva quanto abbiamo poco fa detto: gli elettroni nello stato di energia più bassa di un atomo, non si muovevano tutti sul primo livello energetico.
Nel 1925 il tedesco W.Pauli trovò la chiave del problema e, come spesso succede (si ricordino le ipotesi di Bohr), era una chiave incredibilmente semplice, una chiave che ha aperto una infinità di porte e che ha spiegato gran parte dei fenomeni atomici fino ad allora oscuri.
Pauli enunciò una regola (il Principio di Pauli) che, appunto, sconcerta per la sua semplicità: in un atomo non vi possono essere due elettroni con gli stessi numeri quantici, cioè su un livello energetico vi possono essere al massimo due elettroni e ve ne sono due se questi elettroni hanno spin opposti. Cerchiamo di vedere ciò in altre parole.
La fisica definisce come “stato” una fissata quaterna di numeri quantici: dati cioè contemporaneamente un n, un l, un m ed un ms si ha un determinato stato.
Ebbene, per il principio di Pauli, un dato stato può essere assegnato ad un elettrone solo.
Si può ancora dire che in un atomo tutti gli elettroni sono diversi del punto di vista del loro comportamento.
Alla luce di questo principio (che ha avuto moltissime conferme e nessuna smentita, che solo da relativamente poco tempo ha t rovato una giustificazione teorica) vediamo di “costruirci” qualche atomo partendo dall’atomo di idrogeno che ha un solo elettrone ed andando avanti.
Consideriamo il livello K. In questo livello il numero quantico principale è n=1. Applicando quanto abbiamo appreso studiando i numeri quantici ed il principio di Pauli per il livello K si hanno queste due sole possibilità:

Si vede subito allora che su questo livello non possono trovarsi più di due elettroni i quali risultano diversi nel numero quantico ms di spin.
L’idrogeno, quindi, avrà il suo unico elettrone sul livello K. L’elio avrà i suoi due elettroni ancora sul livello K:
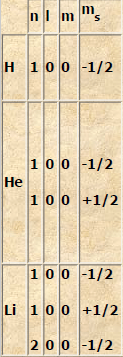
Il litio con tre elettroni (tabella precedente), completato il livello K con due di essi, troverà il suo terzo elettrone sul livello L (è come se il terzo elettrone non fosse capace di entrare nello stato n=1 quando questo ha già due elettroni).
Osserviamo a parte che per indicare simbolicamente gli atomi finora visti si usano le seguenti notazioni:
H 1s ; He 1s2 ; Li 1s2 2s
dove il numero che precede la lettera indica il numero quantico principale, la lettera (in questo caso s) indica il numero quantico secondario mentre il numero in alto a destra della lettera indica il numero di elettroni che si trovano in quel livello energetico.
Considerando ad esempio il boro (B), che ha 5 elettroni, si trova la scrittura seguente:
B 1s2 2s2 2p
indicando con questo che il boro ha due elettroni nel livello 1s, due nel livello 2s, uno nel livello 2p.
Ritornando a quanto dicevamo qualche riga indietro, dovrebbe essere ormai chiaro come si sistemano gli elettroni in un atomo.
Per maggior chiarezza riportiamo nella tabella seguente gli stati quantici successivi degli elettroni che entrano a far parte di un atomo (tavola 4)
Elettone n l Livello m ms Strato
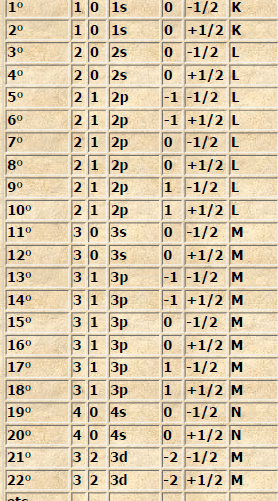
[nella prima colonna è indicato l’elettrone in oggetto; nella seconda è indicato il numero quantico principale n che compete al dato elettrone; nella terza è riportato il numero quantico secondario l del dato elettrone; nella quarta è riportato il livello o orbitale in cui ci troviamo nell’atomo in considerazione; nella quinta vi è il numero quantico magnetico m; nella sesta il numero quantico di spin ms; nell’ultima è riportato lo strato a cui appartiene l’elettrone].
Una rappresentazione simbolica dei primi atomi che si incontrano nella tavola periodica degli elementi dà:

Si potrebbe così continuare fino all’ultimo elemento della tavola periodica (l’uranio) che ha una distribuzione di elettroni nei livelli e sottolivelli come riportato di seguito (non si sono distinte le orientazioni dei vari orbitali):
U 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 4f14 5s2 5p6 5d10 5f3 6s2 6p6 6d 7s2
Nella Tavola 5 abbiamo riportato uno schema riassuntivo di tutte le possibili combinazioni dei numeri quantici tra loro, mentre sella Tavola 6 riportiamo la distribuzione degli elettroni per tutti gli atomi degli elementi della tavola periodica.

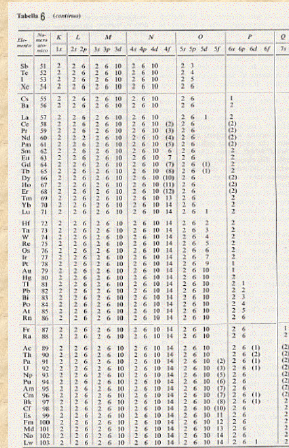
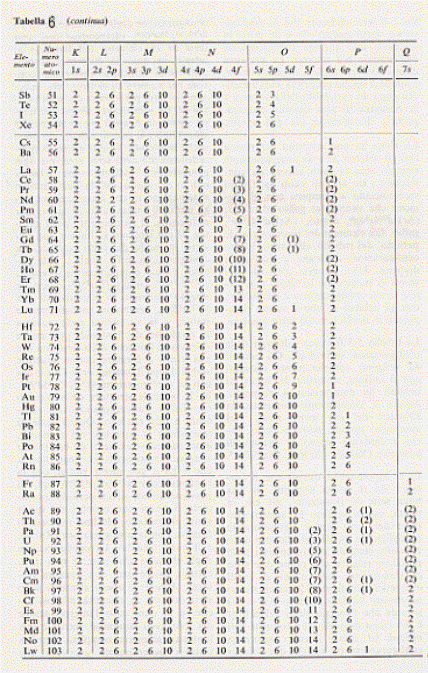
Per far si che il nostro lavoro sia meglio compreso, cerchiamo di renderci conto del come sono distribuite le energie dei livelli energetici intorno al nucleo di un atomo.
Dobbiamo considerare un diagramma, il Diagramma di Grotrian, che ci rende ben conto di questa distribuzione di energie.
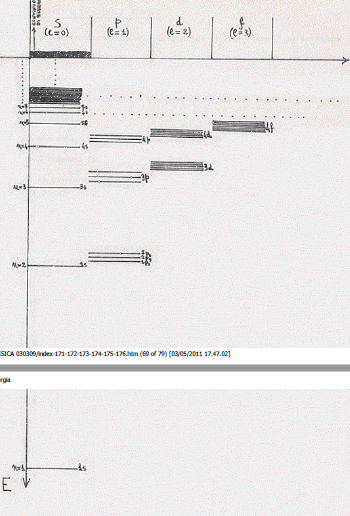
Nel diagramma della prossima figura (diagramma di Grotrian) l’asse delle ordinate riporta il valore delle energie possedute dagli elettroni che si trovan intorno al nucleo di un atomo. Tenendo conto che le energie quando c’è attrazione vengono considerate negative, mentre, quando c’è repulsione, vengono considerate positive, tracciamo l’asse delle ordinate rivolto verso il basso.
L’asse delle ascisse corrisponderà allora allo zero della nostra energia; far arrivare cioè un elettrone fino a questo zero di energia significa fornire all’elettrone un’energia tale da farlo sfuggire dall’atomo, un’energia tale, cioè, da togliere un elettrone o più dall’atomo, da ionizzare l’atomo. L’asse delle ascisse è quindi il livello energetico corrispondente alla ionizzazione dell’atomo. Poiché il livello di energia che corrisponde allo stato fondamentale (non eccitato) dell’atomo è relativo ad n = 1 e poiché mano a mano che si aumenta l’energia aumenta n e ci si allontana dal nucleo, al livello di ionizzazione corrisponderà un valore n = ∞ .
A proposito di questo diagramma ci sono poi da osservare alcune cose che non giustificheremo teoricamente ma che daremo per scontate.
1) Per ogni valore di n vi sono n2 livelli energetici: cioè, per n = 1 si ha n2 = 1 livello energetico (l’1s); per n = 2 si hanno n2 = 4 livelli energetici (2s, 2px , 2py , 2pz); per n = 3 si avranno n2 = 9 livelli energetici e così via.
2) Nel caso dell’atomo di idrogeno tutti gli n2 livelli energetici relativi ad un certo valore di n hanno la stessa energia di n (sono degeneri), per cui ad n = 1 corrisponde un livello, ad n = 2 ancora un livello, e così via.
3) Le righe, che in questo diagramma ci rappresentano i livelli energetici, non sono equidistanti ma vanno ad infittirsi mano a mano che ci si avvicina al livello di ionizzazione a cui compete, come abbiamo detto, una energia E=0, e si vanno ad infittire con una legge che risulta inversamente proporzionale ad n2 . Il primo livello, cioè n=l, dista dal secondo di 1/n2 = 1/1; il secondo livello (n=2) dista dal terzo di 1/n2 = 1/22 = 1/4; il terzo dista dal quarto di 1/9; il quarto dal quinto di 1/16; e così via.
4) Partendo dal nucleo fino ad arrivare al livello di ionizzazione le energie dei livelli elettronici sono quantizzate, sono cioè discrete. Questi livelli mentre sono molto distanziati in prossimità del nucleo, mano a mano che ci si allontana da esso tendono ad infittirsi. Superando questo livello di energia di ionizzazione (E = 0) ci sono talmente tanti livelli e così fitti che all’atto pratico l’elettrone può stare dovunque perché in questo punto trova sempre un livello a sua disposizione. Oltrepassando quindi il livello E=0 si ha in pratica un continuo di energie e l’elettrone, una volta che gli sia stata fornita energia, può vagare come e dove vuole (elettrone libero)
Vediamo ora, alla luce di quanto abbiamo detto, come è fatto questo diagramma:
Come sono fatti gli orbitali atomici
Abbiamo introdotto i numeri quantici che ci sono serviti per introdurre il principio di Pauli; abbiamo poi parlato della distribuzione dei livelli elettronici in un atomo. A questo punto rimane da vedere come sono fatti gli orbitali atomici, ricollegandoci a quanto andavamo dicendo prima di parlare dei numeri quantici.
Riassumendo, per descrivere la struttura elettronica di un atomo, si utilizzano i seguenti fatti:
1) la funzione d’onda ψ associata ad ogni singolo elettrone;
2) la ψ modulo quadro che misura, la densità della nuvola di carica dell’elettrone;
3) i numeri quantici n, m, l, ms ;
4) le energie associate ai singoli orbitali.
In definitiva: la funzione d’onda ψ è l’orbitale atomico e la densità di probabilità di trovare l’elettrone in questo orbitale ci è data da ψ modulo quadro; ogni elettrone ha associati quattro numeri quantici e, per il principio di Pauli, in un atomo non vi possono essere due elettroni con tutti e quattro i numeri quantici uguali o, che è lo stesso, su di un orbitale vi possono essere due elettroni solo se questi hanno spin opposti; così come i livelli energetici della teoria di Bohr-Sommerfeld, anche gli orbitali hanno energie caratteristiche (in un orbitale se vi sono orbitali diversi con identiche energie, questi orbitali sono chiamati degeneri); tra orbitali diversi possono avvenire transizioni di elettroni (se la transizione avviene da un orbitale ad energia più bassa ad uno ad energia più alta si ha assorbimento di un fotone hn; per la transizione inversa si ha emissione di un fotone di energia hn) e queste transizioni hanno luogo solo tra determinati orbitali così come ci dicono alcune regole (che non abbiamo studiato per non appesantire il discorso) dette di selezione; la somma delle energie di tutti gli orbitali atomici occupati da elettroni ci fornisce l’energia elettronica totale dell’atomo in questione. Nelle figure seguenti sono riportate le superfici limite dei tre orbitali 2p (già visti) e dei 5 orbitali 3d (abbiamo già visto che gli s sono sferici), superfici che sono state trovate andando a considerare i punti in cui la ψ è costante (i segni + o – che si trovano in figura indicano le regioni in cui ψ è positiva o negativa; dobbiamo avvertire, comunque, che il + ed il – non debbono essere in alcun modo pensati legati ad una qualche carica elettrica).

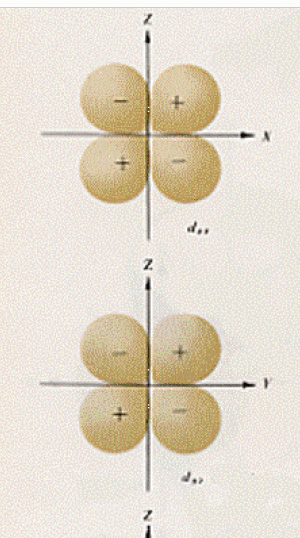
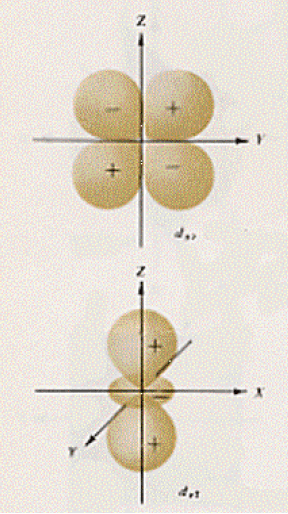
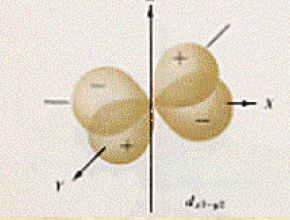
Disegnati questi orbitali si può restare in imbarazzo osservando i nodi, per esempio degli orbitali 2p. Infatti ci si può chiedere come un elettrone che si trovi su quel determinato orbitale possa passare da una parte all’altra di un nodo. Il problema ha anche qui una soluzione semplice: il modello dell’atomo fornito dalla meccanica quantistica non descrive come un elettrone si muove (la sua traiettoria o altri particolari) ma solo la probabilità per un elettrone di trovarsi in una determinata posizione.
La traiettoria è un concetto collegato con la fisica classica e non ha quindi senso parlarne in questo nuovo tipo di meccanica, nella meccanica quantistica.
Oltre a ciò va detto che quando troviamo disegnato un orbitale in cui una certa zona è ombreggiata più marcatamente di un’altra, in questa zona più scura si ha maggiore probabilità di trovare l’elettrone e questo fatto può essere inteso anche nel senso che l’elettrone passa una parte maggiore del suo tempo in quella zona.
E’ bene, prima di chiudere questo argomento, fare delle considerazioni complementari sulla probabilità di trovare elettroni sui vari livelli energetici od orbitali che siano. Colleghiamo cioè quanto abbiamo ora detto alla rappresentazione grafica della ψ e della ψ modulo quadro.
Riferiamoci all’atomo di idrogeno e consideriamo la figura seguente relativa agli orbitali 1s, 2s, 2px (disegnati ora non più con le superfici limite ma con la densità di probabilità elettronica) ed alle rispettive ψ e ψ modulo quadro.
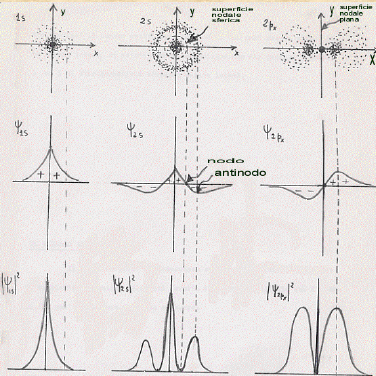
Come si può vedere: in (a) è stata riportata la densità di probabilità elettronica, in (b) la funzione d’onda elettronica ψ, in (c) la probabilità ψ modulo quadro di trovare l’elettrone ad una certa distanza x dal nucleo.
Nelle figure sono anche state riportate le superfici nodali che corrispondono all’Insieme di punti in cui l’elettrone non può trovarsi. L’orbitale 1s ha una superficie nodale all’infinito (in pratica ad 1÷2 Å dal nucleo) l’orbitale 2s ha, oltre alla superficie nodale all’infinito, una superficie nodale sferica rappresentata in sezione tratteggiata, l’orbitale 2px ha, oltre alla superficie nodale all’infinito, una superficie nodale piana corrispondente al piano passante per il nucleo e perpendicolare all’asse x. In corrispondenza ad una superficie nodale la funzione d’onda ψ cambia segno (o fase), mentre la probabilità ψ modulo quadro di trovare l’elettrone si annulla.
Considerando, come abbiamo fatto, anche le superfici nodali all’infinito, dalla figura si può vedere, e mostrare più in generale, che il numero totale delle superfici nodali è uguale al numero quantico principale n, mentre il numero delle superfici nodali passanti per il centro dell’atomo (per il suo nucleo) è uguale al numero quantico secondario l. E’ questa una scoperta di grande portata, dovuta alla meccanica quantistica. I numeri magici n ed l della teoria di Bohr-Sommerfeld acquistano ora un significato fisico ben preciso. Tra l’altro, poiché il numero delle superfici nodali non può essere altro che un numero intero, si ritrova anche una spiegazione del perché i numeri n ed l di Bohr-Sommerfeld dovevano essere interi.
Il modello atomico attuale
Il presente stato di conoscenza sulla costituzione di un atomo ad un elettrone contiene elementi forniti dai vari modelli fin qui discussi. Si può riassumere nel modo seguente:
a) Al centro dell’atomo c’è un nucleo in cui è concentrata la gran parte della massa dell’intero atomo; il nucleo ha una carica positiva uguale a quella di tutti gli elettroni ed ha le dimensioni di 10-12 cm.
b) Ad una certa distanza dal nucleo c’è una zona in cui si ha una certa probabilità, diversa da zero, di trovare un elettrone estremamente piccolo che possiede il resto della massa dell’atomo (1/1800) ed una carica negativa.
c) L’elettrone occupa una posizione che può non essere conosciuta con precisione, benché la sua probabile posizione possa essere calcolata.
d) Informazioni completa sull’elettrone, compresa la sua posizione più probabile, possono essere ricavate risolvendo l’equazione di Schrödinger.
e) L’elettrone possiede sia energia potenziale di origine elettrostatica, sia energia cinetica; la somma di queste energie è minore dell’energia potenziale di un elettrone libero. L’elettrone è così trattenuto vicino al nucleo in una zona di potenziale chiamata buca di potenziale. L’energia totale che esso può assumere è limitata ad alcuni valori particolari che sono determinati univocamente da alcune costanti fondamentali e da alcuni parametri (i numeri quantici) che escono fuori dalla soluzione dell’equazione di Schrödinger e dalla sua distanza media dal nucleo.
f) Nel passare da un livello energetico ad un altro, l’elettrone emette od assorbe energia, usualmente nella forma di un’onda elettromagnetica (o di un fotone).
La dettagliata, completa e fortunata descrizione dell’atomo ad un solo elettrone è uno dei più grandi trionfi della fisica contemporanea.
Nel fornire una descrizione dell’atomo a più elettroni cominciamo con il mantenere le varie caratteristiche dell’atomo ad un elettrone.
Oltre a queste introduciamo il principio di esclusione di Pauli il quale afferma che in uno stesso atomo non possono trovarsi due elettroni precisamente simili.
Una tale descrizione è ampiamente verificata in tutti i suoi dettagli da una quantità di esperienze.
Su quest’atomo a più elettroni dobbiamo comunque dire qualcosa di più, soprattutto in vista di quanto ci servirà per la discussione delle molecole.
Modello del campo self-consistent di un atomo a più elettroni.
Certo che l’atomo di idrogeno è veramente semplice da descrivere: si deve considerare solo l’interazione tra un nucleo (positivo) ed un elettrone (negativo). Quando però intorno ad un nucleo vi sono più elettroni le cose si complicano molto. Infatti, oltre l’attrazione cui è soggetto ogni singolo elettrone da parte del nucleo, occorre considerare anche la reciproca repulsione tra gli elettroni (che sono tutti carichi negativamente) e, conseguentemente, non è possibile considerare il moto di un elettrone se non in dipendenza da quello di tutti glialtri oltreché dal nucleo.
Questo problema, problema a molti-corpi (sul quale torneremo parlando delle molecole), è, a tutt’oggi, insoluto. Per dare soluzioni che siano in accordo con i fatti sperimentali occorre far ricorso a metodi approssimati. Uno di questi è il metodo del campo self-consistent, per la prima volta introdotto dal fisico britannico D.R. Hartree nel 1928 e sviluppato negli anni successivi dallo stesso Hartree e da altri (nel 1932, con i lavori di J.C. Slater e J. Mc Dougall; nel 1933 con due articoli di Hartree; ancora nel 1933 con un articolo di Hartree e M.M. Black; sempre nel 1933 da altri lavori di F.W. Brown, J.H. Bartlett, C.G. Dunn; infine nel 1934 da un lavoro di C.C. Torrance). Vedremo ora questo metodo.
Consideriamo un elettrone di un atomo a più elettroni. Come abbiamo detto esso è soggetto all’azione dei campi elettrici di ciascun altro elettrone, oltreché del nucleo. Ebbene, il metodo del campo self-consistent consiste nel trattare l’elettrone in considerazione come se fosse soggetto al campo elettrico del nucleo e a quello ottenuto come media di tutte le possibili posizioni degli altri elettroni. In definitiva, si considera l’elettrone soggetto al campo del nucleo ed al campo originato come effetto medio di tutti gli altri elettroni (non ha più quindi importanza conoscere istante per istante le coordinate spaziali degli altri elettroni). La cosa importante è che l’effetto complessivo del campo del nucleo e di quello medio degli elettroni è, con buona approssimazione, un campo che ha simmetria sferica (è come se si dovesse trattare il moto di un elettrone intorno ad un unico nucleo, con una carica elettrica opportuna). Quest’ultima eventualità comporta che si potranno considerare gli orbitali atomici per un atomo a più elettroni proprio allo stesso modo in cui abbiamo considerato gli orbitali atomici per l’atomo di idrogeno (che è ad un elettrone). In particolare, si conserva la classificazione di questi orbitali in s, p, d, f, …
Le regole di Hund ed il principio di aufbau
Dato allora un qualsiasi nucleo atomico, dovendo mettere intorno ad esso degli elettroni per costruire l’atomo relativo, qual è il criterio con cui, successivamente, gli elettroni debbono essere sistemati intorno al nucleo dato ?
A questa domanda si può rispondere con il principio di aufbau (la parola «aufbau» è tedesca e significa costruzione) integrato con le regole di Hund (dal nome del fisico tedesco che le ricavò da studi spettroscopici nel 1925).
Cominciamo con il dire che, per quanto ci serve in questo paragrafo, rappresenteremo un orbitale con un quadratino (il quadratino sostituisce qui i trattini che abbiamo incontrato nel diagramma di Grotrian) accompagnato dall’indicazione relativa(1s, 2s, 2p,…) ed indicheremo un elettrone con una piccola freccia (diretta verso l’alto o verso il basso a seconda che lo spin dell’elettrone valga, rispettivamente, + 1/2 e -1/2).
Con questo simbolismo il diagramma di Grotrian che abbiamo visto diventa quello mostrato nella figura seguente:

gli orbitali che possono essere occupati da elettroni (orbitali permessi), dovremo quindi introdurre tutti gli elettroni che abbiamo a disposizione per un dato atomo in questi orbitali.
Come ?
Si introducono uno alla volta i vari elettroni negli orbitali permessi a partire dall’orbitale a più bassa energia (1s) e via via riempiendo gli orbitali ad energia crescente. Nel far questo si deve tener conto del principio di Pauli e quindi in un dato orbitale (in un dato quadratino) al massimo vi possono essere due elettroni con spin opposti (vi possono essere due freccette una rivolta verso l’alto e l’altra rivolta verso il basso).
Fin qui il principio di aufbau. Le regole di Hund ci aiutano poi a sistemare gli elettroni in orbitali di tipo p, d ed f che sono equivalenti dal punto di vista energetico e diversi per orientazione spaziale (si pensi agli orbitali 2p che consistono in un orbitale 2p).
Enunciamo le due regole di Hund prima di passare a vedere il loro funzionamento con delleesemplificazioni:
1) in orbitali che differiscono per orientazione spaziale, pur essendo equivalenti in energia, gli elettroni preferiscono sistemarsi, quando è possibile, uno per orbitale (riempiti gli orbitali 1s e 2s, se si hanno per esempio altri tre elettroni a disposizione questi si disporranno uno sul 2px , uno sul 2py ed uno sul 2pz, piuttosto che riempire prima, ad esempio, il 2px e quindi sistemare l’ultimo a disposizione nel 2py ); quanto abbiamo detto, in base al simbolismo introdotto per gli orbitali, equivale a dire che gli elettroni, nelle condizioni suddette, preferiscono sistemarsi uno per quadratino;
2) in orbitali che differiscono per orientazione spaziale, pur essendo equivalenti in energia, gli elettroni che in base alla regola precedente hanno preferito, quando possibile, distribuirsi uno per orbitale, hanno ancora la preferenza a disporsi con spin paralleli (riempiti gli orbitali 1s e 2s i tre elettroni successivi che, in base all’esempio precedente, si erano distribuiti uno nel 2px , uno nel 2py ed uno nel 2pz , li troviamo tutti disposti con lo spin rivolto, ad esempio, verso l’alto come mostrato nel seguente disegno

Si osservi a parte che l’esempio fatto è quello relativo all’azoto che ha, per l’appunto, 7 elettroni).
Costruiamoci allora con aufbau, Pauli ed Hund, qualche atomo cominciando dall’idrogeno, che ha un solo elettrone, fino ad arrivare al silicio (Si) che ha 14 elettroni (si osservi che il quinto elettrone è stato messo nel 2px ma poteva, indifferentemente trovar posto nel 2py o nel 2pz ) . Fino al Boro abbiamo applicato solo aufbau e Pauli. Dall’elemento successivo, il carbonio, incominciamo a prendere in considerazione contemporaneamente le due regole di Hund.
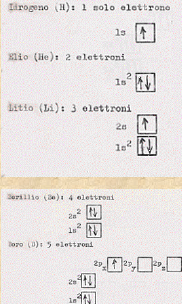
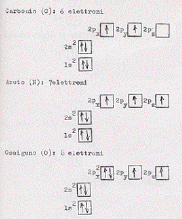
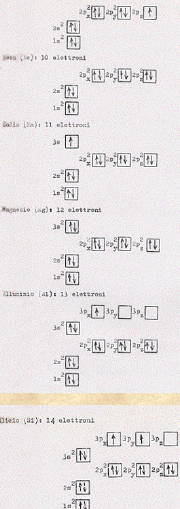
E’ allora chiaro come si prosegue con il fosforo che ha 15 elettroni fino all’uranio che ne ha 92. Ed è ovvio che quanto qui detto è analogo a quanto visto nella Tavola 6 a cui, ora, è meglio ridare un’occhiata.
E’ utile riportare di seguito, a conclusione del capitolo sugli atomi, la tavola periodica degli elementi:
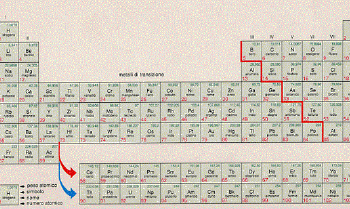
E passiamo ora, nella seconda parte (a partire dall’articolo successivo), allo studio delle molecole e dei legami molecolari.
Categorie:Atomi e Molecole
Rispondi